Síndrome de dilatación-vólvulo gástrico en el perro (II/II): actualización clínica en la cirugía, el manejo posoperatorio y las medidas preventivas
Resumen breve
Tras la estabilización médica inicial del síndrome de dilatación-vólvulo gástrico (DVG), la intervención quirúrgica representa un paso decisivo en el manejo del paciente. En esta segunda parte del artículo, se describen con detalle los aspectos prácticos de la resolución quirúrgica del DVG, los elementos clave del manejo posoperatorio y las principales estrategias preventivas.Índice de contenidos
Introducción
Tras la estabilización médica inicial del síndrome de dilatación-vólvulo gástrico (DVG), la intervención quirúrgica representa un paso decisivo en el manejo del paciente. Esta debe permitir no solo la recolocación del estómago y la valoración de los daños tisulares, sino también la realización de una gastropexia eficaz que minimice el riesgo de recidiva1-4. En esta segunda parte del artículo, se describen con detalle los aspectos prácticos de la resolución quirúrgica del DVG, como recomendaciones técnicas para la desrotación del estómago, la evaluación y resección de tejido no viable y las distintas opciones de gastropexia. También se abordan los elementos clave del manejo posoperatorio, como el control del dolor, la monitorización de complicaciones frecuentes y el soporte nutricional. Finalmente, se describen las principales estrategias preventivas, que incluyen la gastropexia profiláctica en perros de razas predispuestas y distintas recomendaciones sobre alimentación y manejo, con el objetivo de reducir el riesgo de aparición del síndrome.
Tratamiento quirúrgico
Aunque se haya conseguido una descompresión gástrica efectiva, no debe iniciarse la cirugía si el paciente presenta inestabilidad hemodinámica5. Una vez estabilizado, el objetivo del tratamiento quirúrgico es reposicionar el estómago en su lugar fisiológico, inspeccionar la viabilidad del tejido gástrico, del bazo, y del resto de órganos abdominales que se hayan podido ver afectados y, en caso de que exista una lesión necrótica, plantear la resección de esta, si resulta viable. Por último, realizar una gastropexia con el objetivo de fijar el estómago al lado derecho de la pared abdominal para evitar recidivas1-3,5-8. Si el estómago no ha podido ser descomprimido completamente, se recomienda preparar al paciente en decúbito lateral, con el objetivo de reducir el riesgo de oclusión venosa2. La zona a rasurar y preparar de forma aséptica debe abarcar desde la mitad del tórax hasta el pubis7. En caso necesario, la laparotomía media puede extenderse desde la apófisis xifoides hasta el pubis5.
Desrotación del estómago
En caso de que la rotación gástrica persista en el momento de la cirugía (Figura 1), la primera estructura que se observa al acceder a la cavidad abdominal es el omento mayor, que normalmente cubre la zona del estómago dilatado5,7.
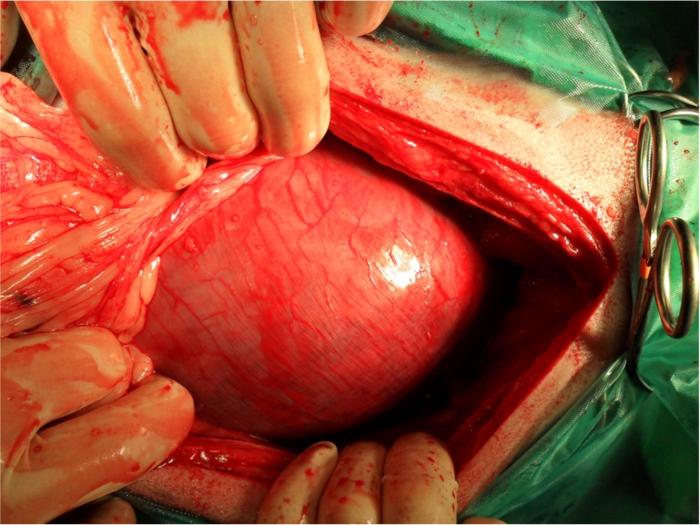
Figura 1. Imagen intraquirúrgica de estómago dilatado y torsionado al acceder a la cavidad abdominal mediante laparotomía por línea media. Se ha retirado el omento momentáneamente para ver el compromiso de la pared gástica, donde se observa congestión.
Para desrotar el estómago se debe realizar el movimiento inverso. Para ello, el cirujano debe posicionarse en el lado derecho del paciente, localizar el antro pilórico que está colocado anormalmente en el lado izquierdo5, dorsal o ventral según sea el grado de rotación. Con la mano izquierda, se ejerce presión sobre el fundus al mismo tiempo que se tracciona con cuidado el antro pilórico para llevarlo a su posición anatómica, hacia el lado derecho del paciente5.
A pesar de que algunos estudios describen la trocarización o la realización de una minigastrotomía intraquirúrgica para facilitar la descompresión y desrotación7, otros autores no recomiendan estas prácticas porque aumenta la posibilidad de derrame de contenido gástrico a la cavidad abdominal, permite la salida del gas contenido en el estómago a la cavidad abdominal y favorece el desarrollo de sepsis5. Los autores optan, en caso de ser necesaria, por la realización de una descompresión intraquirúrgica mediante la introducción de una sonda orogástrica por parte del personal no estéril, lo que permite, además, ayudar a localizar el cardias y verificar si la desrotación se ha realizado de forma correcta2,5.
Determinación de la viabilidad de tejido
Posterior a la recolocación del estómago en su posición anatómica normal, se debe de proceder a inspeccionar el resto del abdomen y, especialmente, evaluar la reperfusión del tejido gástrico y del bazo2.La zona de la curvatura mayor y el fundus es la más comúnmente afectada por áreas de necrosis, debido a dilatación y a la ruptura de las arterias gástricas cortas2,5,7(Figuras 2 y 3).
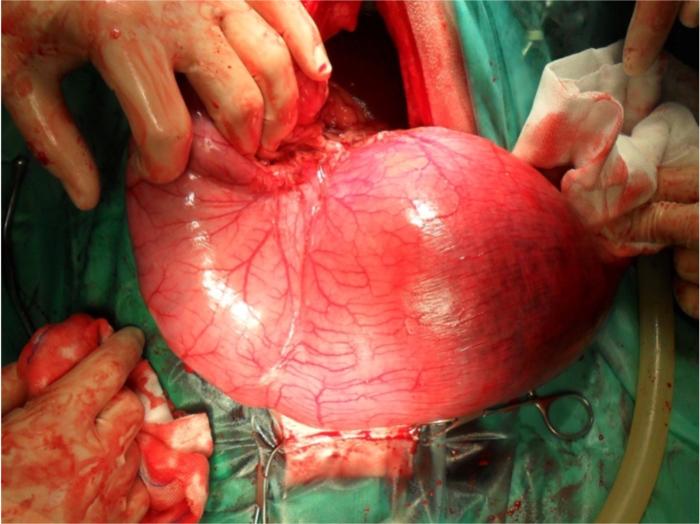
Figura 2. Imagen intraquirúrgica en la que se observa congestión de la pared gástrica en el inicio de la curvatura mayor del estómago.
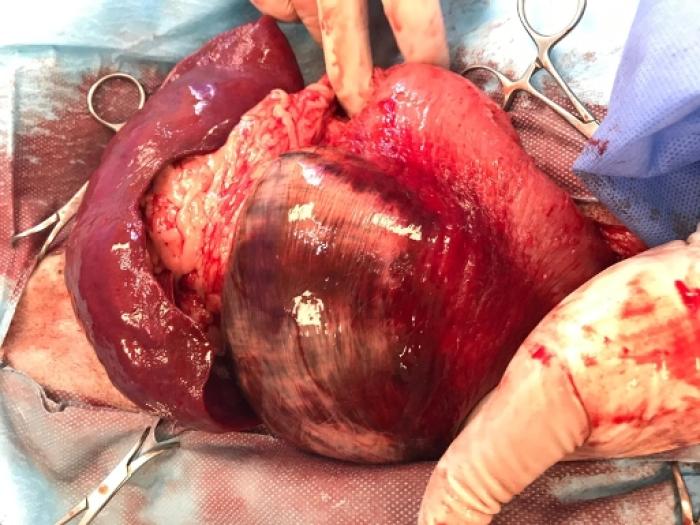
Figura 3. Imagen intraquirúrgica en la que se observa necrosis extensa de la pared gástrica (Fuente: Rosario Ruano y Gustavo Ortiz).
Los criterios subjetivos para evaluar la viabilidad de la pared gástrica son su grosor, valorado mediante palpación, el color de la superficie de la serosa, la evidencia de perfusión tisular y el peristaltismo2,7,9. Un grosor de la pared más fino de lo normal, o una coloración gris-verdosa o negruzca, son signos de falta de viabilidad del tejido2. Un estudio experimental concluyó que la interpretación subjetiva de un cirujano en la valoración de la viabilidad del tejido gástrico demostró tener una fiabilidad del 85 %; sin embargo, una interpretación incorrecta de los hallazgos macroscópicos puede conllevar una posterior perforación o dehiscencia de las zonas de gastrectomía2,9. Por otro lado, se han llevado a cabo estudios en búsqueda de datos objetivos para predecir la viabilidad del tejido gástrico, incluyendo el uso de fluoresceína, gammagrafía y flujometría de láser Doppler2,7,10-13. Estudios más antiguos determinaron que las dos primeras técnicas no proporcionaban resultados satisfactorios para de la viabilidad del tejido, mientras que el uso de flujometría de láser Doppler proporcionaba resultados similares a los hallazgos subjetivos del cirujano2,7,10-12. Sin embargo, un estudio reciente evidencia que el uso de la fluorescencia en el infrarrojo cercano (NIRF) en tiempo real permite una identificación más precisa de áreas no viables del tejido gástrico y una toma de decisiones quirúrgicas más rigurosa, recomendando su implementación13. A pesar de estos hallazgos, en la actualidad esta técnica no está disponible de forma habitual en la práctica veterinaria, entre otros motivos, por una limitación de coste económico.
Gastrectomía parcial e invaginación gástrica
En caso de confirmarse, la existencia de zonas necróticas en la pared gástrica puede optarse por su resección o invaginación2,5.
Para realizar una gastrectomía parcial, el estómago debe aislarse del resto de la cavidad abdominal empleando un tercer campo con paños o compresas humedecidas2. Los autores recomiendan la colocación de unas suturas de tracción para evitar el derrame de contenido gástrico2. Los vasos del área de lesión se deben sellar mediante ligaduras o dispositivos de sellado vascular2. El tejido se extirpa con unas tijeras, incidiendo sobre tejido sano, que debe sangrar activamente al seccionarse2. El defecto se cierra con un patrón de dos capas empleando sutura monofilamento reabsorbible 2/0 o 3/0, primero la mucosa con un patrón simple continuo y posteriormente la seromuscular con un patrón invertido continuo o interrumpido2. Los autores optan en ocasiones por no emplear patrones de sutura de reinversión (Figura 4).
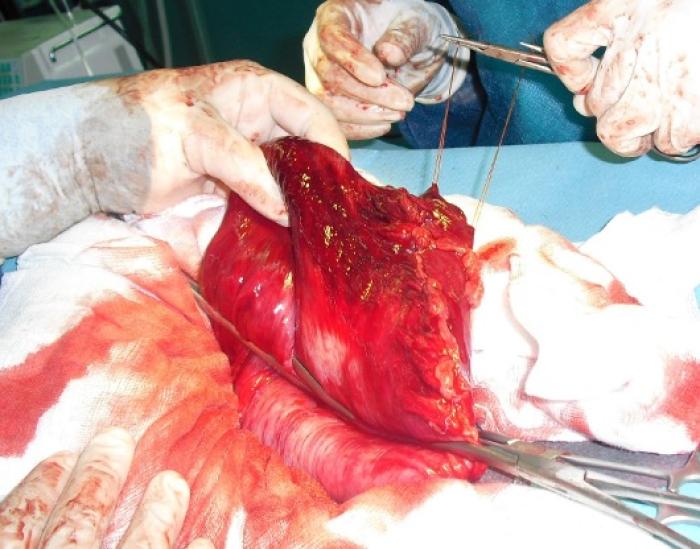
Figura 4. Colocación de pinzas de Doyen por debajo del área a resecar en una dilatación torsión gástrica (Fuente: Dra. JD Carrillo).
La gastrectomía parcial también se puede realizar con grapadoras lineales (p. ej., grapadora de anastomosis gastrointestinal o toracicoabdominal)2,7,14. Aunque estos dispositivos resulten en un mayor coste, permiten el cierre de la luz gástrica antes de la resección, reduciendo el riesgo de contaminación y disminuyendo el tiempo quirúrgico1,2. El uso de grapadoras se asocia de forma significativa con un menor porcentaje de complicaciones y mortalidad que el descrito para un cierre tradicional5,14. Los autores recomiendan su uso, en caso de disponer del dispositivo y las cargas, y de que el propietario haya aceptado el coste extra que supone su uso.
La invaginación se ha propuesto como alternativa a la gastrectomía parcial15. Para realizar esta técnica, se coloca un patrón de sutura continua simple o invertida y un segundo patrón de sutura invertida, siempre en tejido sano, para aposicionar el tejido sano sobre el necrótico, sin penetrar en la luz gástrica2. De este modo, el tejido necrótico se invierte hacia el interior del estómago, donde será autodigerido por la acción de los jugos gástricos5. Este procedimiento es más rápido y reduce el riesgo de fuga1,2, pero diversos estudios describen la aparición de úlceras gástricas con relevancia clínica asociada a esta técnica15, incluso 21 días tras el procedimiento, requiriendo una resección quirúrgica16. También se han descrito la formación de abscesos gástricos y el desprendimiento de grandes cantidades de tejido hacia la luz17. Por estos motivos, el uso de esta técnica está en desuso1, y los autores prefieren la resección del tejido afectado, frente a la invaginación.
Evaluación esplénica
En pacientes con DVG, la esplenectomía se realiza únicamente en caso de torsión esplénica o necrosis del bazo, o si hay evidencia de trombosis vascular2,18,19. En estos pacientes, el bazo suele encontrarse desplazado hacia la zona ventral derecha del abdomen7, congestivo y aumentado de tamaño debido a la congestión venosa, incluso en la ausencia de torsión del pedículo18 (Figura 5).
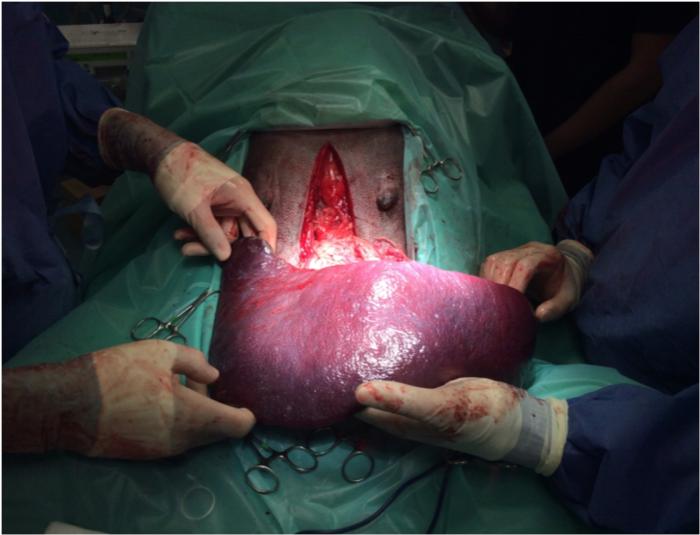
Figura 5. Esplenomegalia por síndrome de dilatación-vólvulo gástrico en el perro.
En condiciones normales la consistencia es firme, y puede presentar placas sideróticas o depósitos de fibrina, que se deben considerar hallazgos no patológicos18,19. Se debe de inspeccionar el pedículo vasculary determinar si se debe extirpar en el mismo procedimiento de resolución de la DVG. En casode torsión esplénica, el bazo estará congestivo con coloración muy oscura o negra, con el pedículo retorcido18,19(Figura 6).
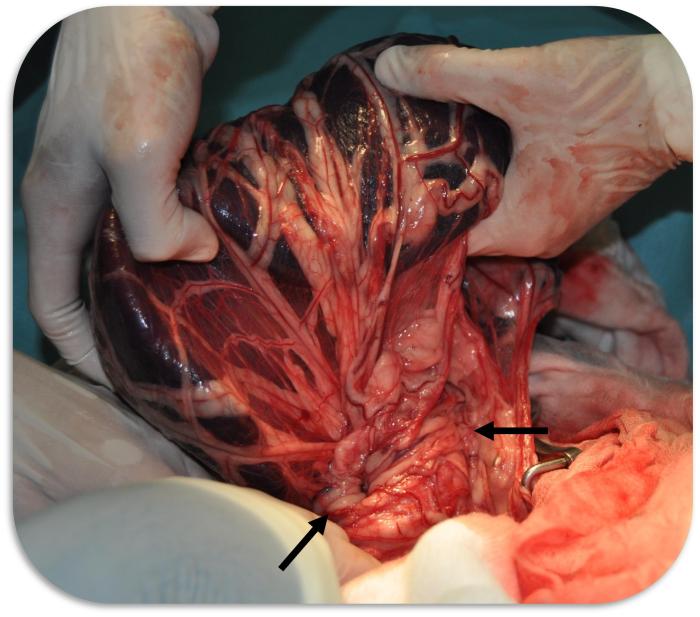
Figura 6. Imagen intraoperatoria durante la cirugía de un perro con dilatación-torsión gástrica, en la que puede observarse la torsión del hilio esplénico (Fuente: Dra. JD Carrillo).
En estos casos, se recomienda realizar ligaduras manuales o emplear dispositivos de sellado de vasos para su extirpación, en vez de dispositivos de grapado18. No se debe tratar de destorsionar el órgano, ya que implicará la liberación de sangre secuestrada, trombos, microtrombos y productos de desecho celular (radicales libres, factores de necrosis tumoral) al torrente sanguíneo18,19.
Gastropexia
La gastropexia consiste en la fijación permanente del antro pilórico del estómago al lado derecho de la pared abdominal2. Este procedimiento es esencial en todos los pacientes que hayan sufrido DVG para evitar recidivas7,25,27 y se recomienda de forma profiláctica en pacientes sanos más susceptibles de sufrir esta condición3,4,5,20,25. Su eficacia ha demostrado reducir la recurrencia de DVG de un 80 % a menos del 5 %20. Existen diversas técnicas quirúrgicas posibles: gastropexia incisional, en cinturón, circuncostal, gastrocolopexia, asistida por laparoscopia e íntegramente laparoscópica, entre otras2,5,7,20,25. Aunque se han realizado estudios para determinar diversos grados de éxito, ninguna se considera técnica de referencia5. No obstante, se debe tener en cuenta que la localización en la que se realice la unión es fundamental para evitar complicaciones, como la obstrucción parcial del flujo de salida del píloro2,5,21. Es importante tener en cuenta que la gastropexia no elimina por completo el riesgo de dilatación gástrica, ya que se ha descrito una recurrencia en aproximadamente el 5 al 11 % de los pacientes tras la realización de este procedimiento5. Algunos autores han asociado la gastropexia profiláctica a un posible aumento en el riesgo de sufrir una torsión mesentérica posterior como otra posible complicación grave; sin embargo, los beneficios de prevenir DVG, una enfermedad más común y grave, justifican mantener su recomendación24.
Hasta hace diez años la gastropexia en cinturón era la técnica más comúnmente empleada1. No obstante, con el tiempo, la gastropexia incisional fue ganando popularidad hasta convertirse en la técnica de elección en la mayoría de los casos, debido a su mayor simplicidad y rapidez de ejecución1,20. Esta es, de hecho, la técnica utilizada por los autores. A pesar de esta preferencia, no se han encontrado diferencias significativas entre ambas técnicas en términos de supervivencia o recidiva1.
Para la realización de una gastropexia incisional, previamente, se debe unir el estómago manualmente a la pared abdominal para estimar el lugar anatómico adecuado para la unión2,5. Debe ser fijado en una posición que reproduzca, en la medida de lo posible, su localización anatómica y orientación fisiológica normal, en general lateral o ventrolateral a 2-3 cm caudal a la última costilla, y evitando cualquier tensión excesiva en los tejidos2,5. Los autores recomiendan colocar un punto inicial que aproxime el estómago a la pared abdominal con sutura monofilamento absorbible 0 o 2/0. A continuación, se realiza mediante una incisión seromuscular de 4-5 cm en el antro pilórico, paralela o perpendicular, sin penetrar la mucosa2,5 (Figura 7), seguida de una segunda incisión a través del peritoneo y en el músculo transverso del abdomen, en el lado derecho de la pared abdominal, de la misma longitud que la incisión realizada en el estómago2,5. Para una correcta visualización, se recomienda emplear retractores de Balfour para retraer y evertir el músculo de la pared abdominal o también se pueden empelar pinzas de campo2 (Figura 8).
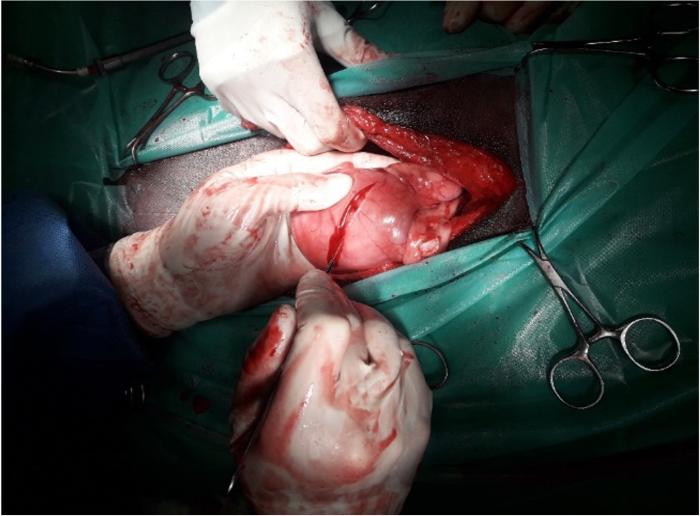
Figura 7. Imagen intraquirúrgica de incisión seromuscular de alrededor de 4 cm en el estómago, para posteriormente realizar la gastropexia.
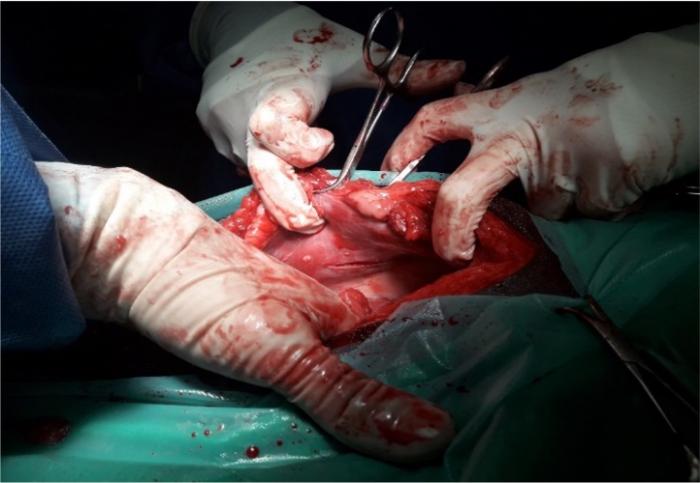
Figura 8. Imagen intraquirúrgica de eversión de la pared abdominal del lado derecho, haciendo uso de pinzas de campo, para realizar una segunda incisión a través del peritoneo.
Las incisiones de la pared abdominal y de la pared gástrica se suturan con un patrón simple continuo monocapa, empleando material de sutura monofilamento reabsorbible 2/0 o 0, preferiblemente de larga duración como la polidioxanona, comenzando con los bordes craneodorsales de la incisión2,5 (Figura 9). Al concluir el procedimiento, se aconseja omentalizar la zona de la gastropexia5.
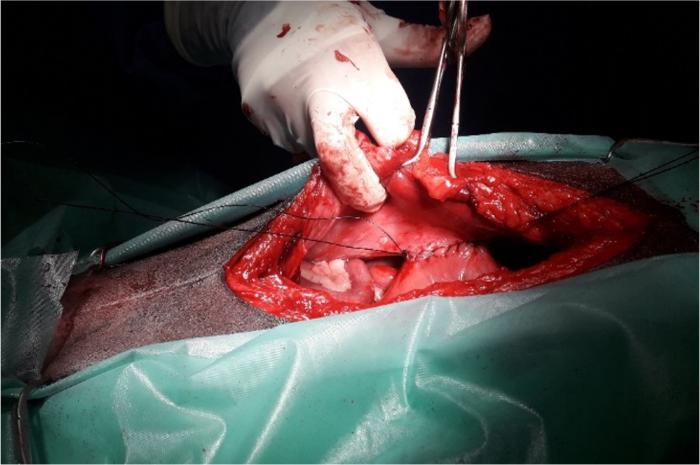
Figura 9. Imagen intraquirúrgica de realización de la gastropexia. Unión de las incisiones en pared gástrica y abdominal con sutura monofilamento reabsorbible (polidioxanona) realizando un patrón simple continuo monocapa. Se coloca un punto inicial que aproxime el estómago a la pared abdominal, y a su vez se mantienen los cabos largos, sujetos con una pinza vascular (mosquito), que nos permiten traccionar y exponer mejor la zona a suturar.
Por otra parte, también se ha descrito una técnica de gastropexia permanente empleando grapadora automática, con buenos resultados a largo plazo2,5,22.
A su vez, aunque las técnicas mediante laparotomía son las más adecuadas en casos de urgencia, las técnicas de mínima invasión pueden considerarse en procedimientos profilácticos con pacientes estables, e incluso realizarse asociadas a otros procedimientos como ovariectomías laparoscópicas, orquiectomías en criptórquidos o toma de muestras para biopsia de otros órganos4,21,29. Las técnicas de mínima invasión más estudiadas son la gastropexia íntegramente laparoscópica o la asistida por laparoscopia2,4,22,26-28.
Para la gastropexia íntegra por laparoscópica, el cirujano principal se debe colocar a la izquierda del paciente, con el monitor de laparoscopia enfrentado en el lado opuesto25 (Figura 10).
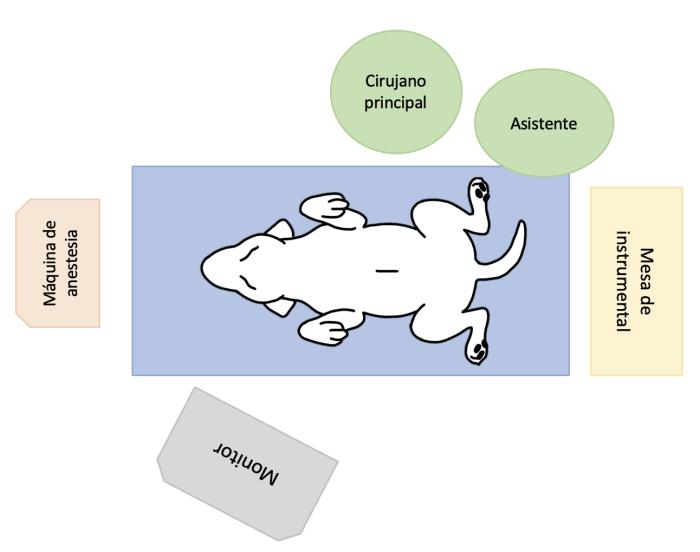
Figura 10. Esquema de organización del instrumental y personal de quirófano para la realización de una gastropexia íntegra por laparoscopia.
Se realiza una técnica de tres puertos colocados en la línea media ventral2,25,27. El primer puerto se coloca en línea alba, 1 cm caudal al ombligo, y se genera un neumoperitoneo mediante la insuflación de dióxido de carbono (CO2), sin exceder una presión de 10-12 mmHg. El puerto de instrumentos se puede colocar a 3-4 cm caudal al xifoides y el último puerto entre ambos, medial a la zona planeada para la gastropexia, aunque estas posiciones pueden variar en función del tamaño del paciente2,25,27(Figura 11).
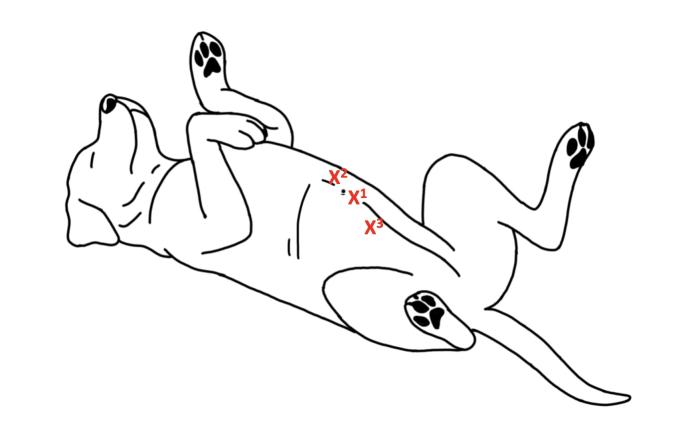
Figura 11. Esquema que muestra la localización de los puertos de laparoscopia para la técnica de tres puertos en la gastropexia íntegra por laparoscópica.
Cuando todos los puertos están colocados, se reduce la presión a 6-8 mmHg25. La óptica se introduce a través del puerto central y se coloca una sutura de sujeción en el estómago, atravesando la pared abdominal a 2-3 cm caudal a la última costilla y a 5-8 cm lateral a la línea media2,25,27. Esta sutura se inserta a través del antro pilórico, atravesando el grosor completo del estómago, y se devuelve a través de la pared abdominal adyacente2,25,27. Se retirará al finalizar el procedimiento. Los autores recomiendan una aguja de gran longitud para facilitar la realización de este paso (nylon 2/0 de 38 mm montada en una aguja de corte inverso de 3/8 círculo25). Posteriormente, se realiza una incisión de 2-5 cm en el músculo transverso del abdomen, en el lugar planeado para la gastropexia, y otra incisión de la misma longitud en las capas serosa y muscular del estómago en la misma orientación, empleando tijeras laparoscópicas o gancho de coagulación monopolar laparoscópico2,25,27. Ambas incisiones se anteponen con sutura intracorpórea, pasando la aguja de manera percutánea, adyacente al lugar donde se va a realizar la gastropexia2,25. El primer punto se coloca en el antro pilórico y se ancla a la pared abdominal, en posición paracostal a 2-3 cm de la última costilla, y se realizan dos líneas de sutura en patrón simple continuo25,30. Se debe tener en cuenta que, al realizar la sutura, se debe disminuir la presión del neumoperitoneo para reducir la tensión y asegurar que el estómago queda correctamente anclado a la pared abdominal, en una posición adecuada73. Uno de los aspectos más exigentes de esta técnica es el anudado de la sutura intracorpórea, por lo que el uso de suturas barbadas unidireccionales es adecuado, ya que permite anclarse de forma segura a los tejidos evitando la realización de la incisión en pared gástrica y realizando únicamente la incisión en la pared abdominal25,30. Ha demostrado ser un procedimiento seguro y eficaz, con complicaciones mínimas y manejables respecto a otras técnicas31. En la actualidad, el uso la sutura barbada es el más extendido para este procedimiento y es la que emplean los autores, realizando una incisión de 4 cm.Esta sutura genera suficiente trauma en el tejido como para promover la adhesión al músculo transverso del abdomen, aunque solo se realice esta incisión30. No se ha determinado todavía cuál es el número de puntos de sutura necesarios para producir una gastropexia segura, pero, a pesar de que se ha mostrado que una incisión de 4 cm es genera una adherencia más fuerte que una de 2 cm, estudios indican que una incisión de 2 cm es suficiente para evitar el vólvulo gástrico empleando esta técnica30,32.
Para realizar la técnica asistida por laparoscopia, el cirujano principal se debe colocar a la derecha del paciente, con el monitor de laparoscopia enfrentado en el lado opuesto25 (Figura 12).
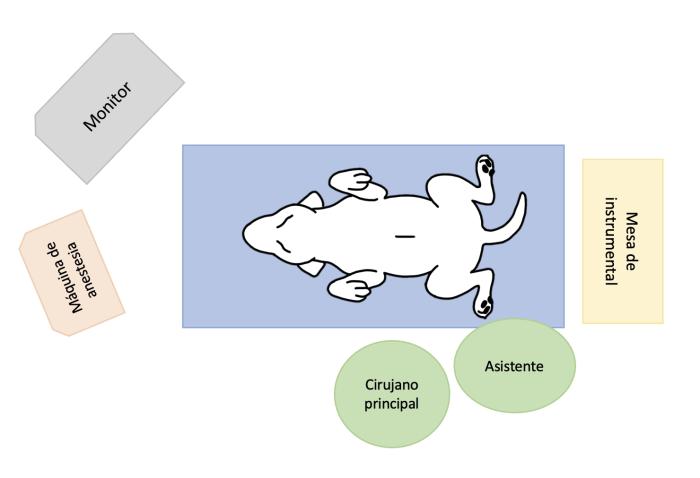
Figura 12. Esquema de organización del instrumental y personal de quirófano para la realización de una gastropexia asistida por laparoscopia.
De forma inicial se coloca el puerto donde seguidamente se introducirá la óptica en la línea media, 2-3 cm caudal al ombligo, y un segundo puerto de trabajo al margen derecho del músculo recto del abdomen, unos 3-5 cm caudal a la última costilla2,25,26,28(Figura 13).
Figura 13. Esquema que muestra la localización de los puertos de laparoscopia para la gastropexia asistida por laparoscópica.
Se establece un neumoperitoneo de la misma manera que en la técnica anterior25. Tras identificar la porción del estómago que se incorporará a la unión, se introducen unas pinzas laparoscópicas de Babcock o DuVall (10 mm) por el puerto de trabajo para agarrar el antro pilórico y retraerlo hacia la pared abdominal, en el lado derecho2,25,26,28. Una vez el antro pilórico esta correctamente sujeto con las pinzas, se evacúa el neumoperitoneo25. Se realiza una incisión en la pared corporal de aproximadamente 3-5 cm de longitud, se colocan suturas de sujeción en el músculo transverso del abdomen para evitar su retracción, y también en el antro pilórico2,25,26,28. Se realiza otra incisión de la misma longitud sobre las capas serosa y muscular del estómago y se suturan a los bordes del músculo transverso del abdomen con dos líneas de sutura simples continuas2,25,26,28. Finalmente, se retiran las suturas de sujeción y se cierran las capas musculares, subcutáneo y piel de forma convencional2,26,28. Al finalizar la gastropexia, tanto íntegramente laparoscópica como la técnica asistida, se debe reestablecer brevemente el neumoperitoneo para verificar una óptima posición del estómago y la ausencia de otras complicaciones mediante exploración laparoscópica25. Por último, se retiran los puertos y se cierran las incisiones de forma convencional25.
La biomecánica de la gastropexia asistida por laparoscopia ha mostrado tener una fuerza de adhesión similar a la de otras técnicas realizadas mediante laparotomía (incisional, en cinturón y circuncostal)2,26 y, a pesar de no identificarse diferencias marcadas en cuanto a dolor posoperatorio, es una técnica más rápida de realizar y produce una respuesta inflamatoria significativamente menor en los pacientes33. Las complicaciones más asociadas a esta técnica, en especial en relación con la incisión paramediana son: la formación de seromas, infección del sitio quirúrgico, dehiscencia o cicatrización excesiva, aunque cabe destacar que son complicaciones menores en más del 96 % de los casos34. Otros estudios han comparado la gastropexia asistida por laparoscopia con la íntegra por laparoscópica y han determinado que la asistida se realiza en un tiempo más corto y necesita un equipo menos especializado, pero la recuperación es más rápida en aquellos sometidos a una intervención íntegramente laparoscópica2,27. Algunos autores han estudiado ambas técnicas en combinación con ovariectomía laparoscópica en el mismo procedimiento y han descrito que los procedimientos laparoscópicos totales se realizan en un tiempo significativamente más largo, pero sin implicar una diferencia en el control analgésico o en la recuperación posoperatoria. Estos autores, recomiendan que la elección para realizar un procedimiento u otro se deben basar en las características del caso clínico y en la experiencia del cirujano29.
Monitorización y tratamiento posquirúrgico
El manejo posquirúrgico del paciente con DVG comprende el control analgésico, el mantenimiento de un correcto estado hemodinámico y el tratamiento de las secuelas que haya podido generar la disminución en la perfusión sistémica y los daños por reperfusión5,6. Esto puede incluir el tratamiento de desequilibrios electrolíticos, arritmias ventriculares, ulceraciones gastrointestinales, fallo renal agudo, peritonitis, coagulación intravascular diseminada (CID), síndrome de respuesta inflamatoria sistémica (SIRS por las siglas en inglés de systemic inflammatory response syndrome)2,6,7 y síndrome de disfunción multiorgánica (MODS por las siglas en inglés de multiple organ dysfunction syndrome)5,35. Generalmente, la peritonitis se asocia a perforaciones gástricas previas a la cirugía o a una resección incompleta del tejido necrótico, lo cual requiere una reintervención con resección adicional2. La monitorización de los parámetros de coagulación permite una detección precoz de CID2, valorando en este caso la administración de heparina2,7. Es importante realizar un seguimiento del valor hematocritoy de albúmina durante el posoperatorio7. La alimentación se inicia dentro de las 12 a 24 horas posteriores a la cirugía2,7. En casos complejos, puede ser necesario el uso de soporte nutricional con el uso de sondas nasoesofágicas5 o tubos de esofagostomía.
Se debe mantener la fluidoterapia con cristaloides isotónicos a un ritmo de mantenimiento, junto con deshidratación del paciente y pérdidas durante un mínimo de 24 horas5 y, posteriormente, reajustar en base a la monitorización de constantes vitales y al estado de hidratación del paciente. El control de electrolitos y la monitorización electrocardiográfica también son fundamentales. La aparición de arritmias en el posoperatorio suele darse entre las 12-36 horas7, en caso de aparición deben de tratarse tal y como se ha descrito en el apartado posterior de estabilización médica.
Otro apartado esencial posquirúrgico, es garantizar un control analgésico multimodal en pacientes con DVG1. Los analgésicos de elección son los opiáceos agonistas puros del receptor µ, como la metadona o el fentanilo1,5. Se puede valorar la combinación de opioides con ketamina o lidocaína en infusión continua intravenosa5. En pacientes con DVG no se ha demostrado un beneficio en el uso de antiinflamatorios no esteroideos (AINE) y, debido a las alteraciones en la perfusión de los órganos responsables de su metabolismo y al riesgo de úlceras gástricas, no se recomienda su uso ni antes ni después de la cirugía5.
Ante la presencia de íleo, la administración de procinéticos (p. ej., metoclopramida) se considera adecuada2,5,7. La presencia de vómitos puede deberse a gastritis isquémica o a la presencia de úlceras gástricas, por lo que debe considerarse el uso de antieméticos de acción central (p. ej., maropitant) y bloqueantes de receptores H2 (p. ej., famotidina) o inhibidores de la bomba de protones (p. ej., omeprazol)2,7, pero únicamente en casos de evidencia de sangrado gastrointestinal o esofagitis por reflujo36. Los autores recomiendan que se den paseos cortos frecuentes tan pronto como el paciente lo permita, ya que favorecen la motilidad gástrica.
En casos en los que no se ha realizado gastrectomía parcial, se recomienda el mantenimiento únicamente de cefalosporinas durante cinco días5. Sin embargo, ante la presencia de necrosis gástrica, perforación o presencia de criterios de sepsis se deben asociar antibióticos como cefalosporinas o amoxicilina-clavulánico a una fluoroquinolona durante una semana5.
Un aumento de creatinina igual o superior al 150 % o 0.3 mg/dl respecto al valor basal o en menos de 48 horas, incluso si el valor permanece dentro del rango de referencia, es indicativo de lesión renal aguda (acute kidney injury; AKI)5,37. El desarrollo de AKI puede deberse a la hipoperfusión durante el estado de shock y a la presencia de microtrombos renales por coagulopatías concomitantes, entre otros5. El uso de coloides durante la resucitación puede exacerbar el proceso38. En estos pacientes, el control de la hidratación y del peso corporal, además de la monitorización de la producción de orina, es fundamental5,37.
Diversos estudios han tratado de evaluar la utilidad de la lidocaína en el tratamiento preoperatorio con el fin de disminuir la lesión por reperfusión isquémica2,39,40, pero no se han determinado diferencias significativas en la tasa de complicaciones posoperatorias o mortalidad entre aquellos pacientes tratados y no tratados2,40. Sin embargo, hay estudios en los que se observó una disminución significativa en la incidencia de arritmias cardíacas y de insuficiencia renal aguda en pacientes tratados con lidocaína frente a aquellos que no, sugiriendo que la administración temprana de lidocaína intravenosa podría reducir complicaciones y mejorar los resultados en perros con DVG41 (Tabla 1).
| Problema/riesgo posoperatorio | Tratamiento/manejo recomendado |
|---|---|
| Dolor posquirúrgico | Control analgésico multimodal: opioides (metadona, fentanilo), ketamina, lidocaína IV Evitar AINE |
| Hipovolemia / deshidratación / alteraciones hemodinámicas | Fluidoterapia con cristaloides isotónicos a mantenimiento y ajustada a la deshidratación del paciente y pérdidas En hipotensión con respuesta parcial a fluidoterapia de shock: norepinefrina: 0.1-2 µg/kg/min IV |
| Desequilibrio electrolítico | Vigilar y corregir Monitorización ECG Reposición de hipopotasemia La hipomagnesemia puede perpetuar la hipopotasemia |
| Arritmias, taquicardia ventricular | Monitorización continua con ECG Corrección de electrolitos Tratar si supone un compromiso hemodinámico o si frecuencia ventricular mantenida >160 lpm Tratamiento:
|
| Peritonitis | Reintervención quirúrgica si hay perforación o necrosis residual |
| Coagulación intravascular diseminada (CID) | Monitorización de parámetros de coagulación Valorar uso de heparina |
| SIRS / MODS | Manejo de soporte intensivo Fluidoterapia, control de infecciones o sepsis |
| Complicaciones gastrointestinales (vómitos, úlceras, íleo) | Antieméticos (maropitant) Protectores gástricos (omeprazol/famotidina), solo ante evidencia de sangrado o esofagitis |
| Motilidad gastrointestinal disminuida | Procinéticos (metoclopramida) Paseos cortos frecuentes cuando el paciente lo permita |
| Fallo renal agudo (AKI) | Monitorización de creatinina, producción urinaria y peso corporal Ajustar fluidoterapia Protocolo tratamiento AKI |
| Infección / sepsis | Cefalosporinas o amoxicilina-clavulánico asociadas a una fluoroquinolona durante un mínimo de una semana |
| Déficit nutricional | Soporte nutricional con sonda nasoesofágica o tubo de esofagostomía |
Tabla 1. Manejo posquirúrgico de la DVG.
Pronóstico y complicaciones
La mortalidad asociada al síndrome de dilatación-vólvulo gástrico (DVG) en pacientes que reciben tratamiento de emergencia se sitúa actualmente entre el 10 y el 30 %1. Este riesgo es especialmente elevado en perros mayores de 10 años23. En comparación, los casos de dilatación gástrica sin vólvulo presentan un pronóstico considerablemente más favorable7. Por otro lado, en pacientes intervenidos para la desrotación gástrica sin gastropexia, se ha documentado una frecuencia de recidiva de hasta el 80 %7.
Los factores que se han asociado a una mayor mortalidad incluyen la duración de signos clínicos por encima de 6 horas, hiperlactatemia, arritmias cardíacas, gastrectomía o esplenectomía concomitante, peritonitis, sepsis, hipotensión, CID, entre otros1-4,23. Estudios recientes han demostrado que una mayor duración del intervalo entre la presentación clínica y la intervención quirúrgica, siempre que se acompañe de una adecuada estabilización médica en el contexto de una emergencia, se asocia con una reducción en la tasa de mortalidad2,8,42,43. Este hallazgo resalta la importancia del tiempo dedicado al soporte intensivo con fluidoterapia y descompresión gástrica durante el manejo médico inicial2, ofreciendo flexibilidad en la planificación quirúrgica según la disponibilidad de recursos y personal43. Sin embargo, la aplicación de la decisión de una cirugía diferida para GDV debe considerarse con precaución y basada en una individualización de cada caso8. Se requiere más investigación para evaluar los riesgos y beneficios de la estabilización prolongada frente a la rápida y para identificar candidatos para cada enfoque43.
Profilaxis
Los tutores de perros con alto riesgo de desarrollar DVG deberían ser informados y aconsejados sobre pautas de manejo preventivas para evitar esta condición5. Modificaciones en los hábitos de alimentación, como humedecer la comida, administrar raciones más pequeñas repartidas en más tomas a lo largo del día, evitar la ingesta desde una posición elevada y emplear comederos que favorezcan una ingesta más lenta se consideran recursos que ayudan a evitar esta patología5,6. Es conveniente recomendar la gastropexia profiláctica en pacientes jóvenes más susceptibles de sufrir esta enfermedad, siempre advirtiendo de que esta técnica evita la rotación del estómago, pero no su dilatación3,4,6,20,25 (Tabla 2) .
| Área de prevención | Recomendaciones prácticas | Objetivo |
|---|---|---|
| Alimentación |
| Reducir la velocidad de ingesta y el riesgo de aerofagia |
| Hábitos y entorno alimentario |
| Prevenir la distensión gástrica y el vólvulo |
| Profilaxis quirúrgica (gastropexia) |
| Disminuir su incidencia y el riesgo de recurrencia |
Tabla 2. Prevención de la DVG.
Puntos clave
- La DVG es una urgencia potencialmente mortal, que requiere estabilización intensiva y, posteriormente, resolución quirúrgica que incluya la realización de una gastropexia. Aunque se haya conseguido una descompresión gástrica efectiva, no debe iniciarse la cirugía si el paciente presenta inestabilidad hemodinámica.
- El objetivo del tratamiento quirúrgico es reposicionar el estómago, evaluar la viabilidad tisular, reseccionando cualquier lesión necrótica presente y realizar gastropexia, habitualmente mediante técnica incisional.
- La gastropexia también se recomienda de forma profiláctica en pacientes predispuestos a esta enfermedad, pudiendo realizarla mediante técnicas de mínima invasión.
- El manejo posoperatorio exige control analgésico eficaz y estabilidad hemodinámica. La mortalidad oscila entre el 10-30 %, con factores como hiperlactatemia, arritmias, gastrectomía o esplenectomía concomitante, o peritonitis, entre otros, aumentando el riesgo.
- La educación de los tutores sobre medidas preventivas en razas predispuestas es clave para reducir la incidencia de DVG.
Bibliografía
1. Olimpo M, Cillari S, Ferraris EI, Giacobino D, Savarino P, Piras LA, Martinelli G, Morello EM. Gastric Dilatation-Volvulus in Dogs: Analysis of 130 Cases in a Single Institution.Animals. 2025; 15(4):579-595. doi: 10.3390/ani15040579
2. Cornell K. Estómago. En: Tobias KM, Johnston SA, editores. Cirugía veterinaria de pequeños animales, Segunda Edición. Zaragoza (ES): Grupo Asís; 2023. p. 1700-1730.
3. Broome CJ, Walsh VP. Gastric dilatation-volvulus in dogs. N Z Vet J. 2003; 51(6):275-283. doi: 10.1080/00480169.2003.36381.
4. Rosselli D. Updated Information on Gastric Dilatation and Volvulus and Gastropexy in Dogs. Vet Clin North Am Small Anim Pract. 2022; 52(2):317-337. doi: 10.1016/j.cvsm.2021.11.004.
5. Carrillo JD, Escobar MT, Martínez M, Gil-Chinchilla JI, García-Fernández P, Jiménez-Peláez M. Síndrome de dilatación-vólvulo gástrico (DVG). Clin Vet Peq Anim. 2016; 36(3): 163-177.
6. Tolbert KT. Gastric Diseases. In: Côté E, Ettinger SJ, Feldman EC, editors. Ettinger’s Textbook of Veterinary Internal Medicine, Ninth Edition. Philadelphia: Elsevier; 2024. p. 1667-1682.
7. HedLund CS, Fossum TW. Cirugía del estómago. En: Fossum TW, editor. Cirugía en Pequeños Animales, Tercera Edición. Barcelona (ES): Elsevier; 2009. p. 409-433.
8. White RS, Sartor AJ, Bergman PJ. Evaluation of a staged technique of immediate decompressive and delayed surgical treatment for gastric dilatation-volvulus in dogs. J Am Vet Med Assoc. 2021; 258(1):72-79. doi: 10.2460/javma.258.1.72.
9. Matthiesen DT. The gastric dilatation-volvulus complex: medical and surgical considerations. J Am Anim Hosp Assoc. 1983; 19(6):925-932. No tiene doi.
10. Berardi C, Wheaton L, Twardock A, Barbee DD. Nuclear imaging to evaluate gastric mucosal viability following surgical correction of gastric dilatation/volvulus. J Am Anim Hosp Assoc. 1993; 29:239-246.
11. Monnet E, Pelsue D, MacPhail C. Evaluation of laser Doppler flowmetry for measurement of capillary blood flow in the stomach wall of dogs during gastric dilatation-volvulus. Vet Surg. 2006; 35(2):198-205. doi: 10.1111/j.1532-950X.2006.00132.x.
12. Wheaton L, Thacker H, Caldwell S. Intravenous fluorescein as an indicator of gastric viability in gastric dilatation- volvulus. J Am Anim Hosp Assoc. 1986; 22:197-204. No tiene doi.
13. Mullen KM, Regier PJ, Perez-Rodriguez V, Fox-Alvarez WA, Bertran J, Colee J. Use of real-time near-infrared fluorescence to assess gastric viability in dogs with gastric dilatation volvulus: A case-control study. Vet Surg. 2024; 53(4):684-694. doi: 10.1111/vsu.14067.
14. Clark GN, Pavletic MM. Partial gastrectomy with an automatic stapling instrument for treatment of gastric necrosis secondary to gastric dilatation-volvulus. Vet Surg. 1991; 20(1):61-68. doi: 10.1111/j.1532-950x.1991.tb00307.x.
15. MacCoy DM, Kneller SK, Sundberg JP, Harari J. Partial invagination of the canine stomach for the treatment of infarction of the gastric wall. Vet Surg. 1986; 15(3):237-245. No tiene doi.
16. Parton AT, Volk SW, Weisse C. Gastric ulceration subsequent to partial invagination of the stomach in a dog with gastric dilatation-volvulus. J Am Vet Med Assoc. 2006; 228(12):1895-900. doi: 10.2460/javma.228.12.1895.
17. Fossum TW, Hedlund CS. Gastric and intestinal surgery. Vet Clin North Am Small Anim Pract. 2003; 33(5):1117-1145. doi: 10.1016/s0195-5616(03)00053-6.
18. Ritcher MC. Bazo. En: Tobias KM, Johnston SA, editores. Cirugía veterinaria de pequeños animales, Segunda Edición. Zaragoza (ES): Grupo Asís; 2023. p. 1551-1564
19. Fossum TW. Cirugía del bazo. En: Fossum TW, editor. Cirugía en Pequeños Animales, Tercera Edición. Barcelona (ES): Elsevier; 2009. p. 624-634.
20. Allen P, Paul A. Gastropexy for prevention of gastric dilatation-volvulus in dogs: history and techniques. Top Companion Anim Med. 2014; 29(3):77-80. doi: 10.1053/j.tcam.2014.09.001.
21. Sutton JS, Steffey MA, Bonadio CM, Marks SL. Gastric malpositioning and chronic, intermittent vomiting following prophylactic gastropexy in a 20-month-old great Dane dog. Can Vet J. 2015; 56(10):1053-1056.
22. Hardie RJ, Flanders JA, Schmidt P, Credille KM, Pedrick TP, Short CE. Biomechanical and histological evaluation of a laparoscopic stapled gastropexy technique in dogs. Vet Surg. 1996; 25(2):127-133. doi: 10.1111/j.1532-950x.1996.tb01388.x.
23. Beck JJ, Staatz AJ, Pelsue DH, Kudnig ST, MacPhail CM, Seim HB 3rd, Monnet E. Risk factors associated with short-term outcome and development of perioperative complications in dogs undergoing surgery because of gastric dilatation-volvulus: 166 cases (1992-2003). J Am Vet Med Assoc. 2006; 229(12):1934-1939. doi: 10.2460/javma.229.12.1934.
24. Fruehwald CM, Spector DI, Daniel TE. Association of mesenteric volvulus in police working dogs with and without a prior prophylactic laparoscopic gastropexy. J Am Vet Med Assoc. 2024; 262(6):1-5. doi: 10.2460/javma.23.11.0620.
25. Corriveau KM, Runge JJ, Rawlings CA. Laparoscopic and Laparoscopic-Assisted Gastropexy Techniques. In: Fransson BA, Mayhew PD, editors. Small Animal Laparoscopy and Thoracoscopy, First Edition. Iowa?: Wiley-Blackwell; 2015. p. 125-133.
26. Rawlings CA, Foutz TL, Mahaffey MB, Howerth EW, Bement S, Canalis C. A rapid and strong laparoscopic-assisted gastropexy in dogs. Am J Vet Res. 2001; 62(6):871-875. doi: 10.2460/ajvr.2001.62.871.
27. Mayhew PD, Brown DC. Prospective evaluation of two intracorporeally sutured prophylactic laparoscopic gastropexy techniques compared with laparoscopic-assisted gastropexy in dogs. Vet Surg. 2009; 38(6):738-746. doi: 10.1111/j.1532-950X.2009.00554.x.
28. Rawlings CA, Mahaffey MB, Bement S, Canalis C. Prospective evaluation of laparoscopic-assisted gastropexy in dogs susceptible to gastric dilatation. J Am Vet Med Assoc. 2002; 221(11):1576-1581. doi: 10.2460/javma.2002.221.1576.
29. Leonardi F, Properzi R, Rosa J, Boschi P, Paviolo S, Costa GL, Bendinelli C. Combined laparoscopic ovariectomy and laparoscopic-assisted gastropexy versus combined laparoscopic ovariectomy and total laparoscopic gastropexy: A comparison of surgical time, complications and postoperative pain in dogs. Vet Med Sci. 2020; 6(3):321-329. doi: 10.1002/vms3.249.
30. Giaconella V, Grillo R, Giaconella R, Properzi R, Gialletti R. Outcomes and Complications in a Case Series of 39 Total Laparoscopic Prophylactic Gastropexies Using a Modified Technique. Animals (Basel). 2021; 11(2):255. doi: 10.3390/ani11020255.
31. Takacs JD, Singh A, Case JB, Mayhew PD, Giuffrida MA, Caceres AV, Fox-Alvarez WA, Runge JJ. Total laparoscopic gastropexy using 1 simple continuous barbed suture line in 63 dogs. Vet Surg. 2017; 46(2):233-241. doi: 10.1111/vsu.12601.
32. Imhoff DJ, Cohen A, Monnet E. Biomechanical Analysis of Laparoscopic Incisional Gastropexy With Intracorporeal Suturing Using Knotless Polyglyconate. Vet Surg. 2015; 44 Suppl 1:39-43. doi: 10.1111/j.1532-950X.2014.12177.x.
33. Haraguchi T, Kimura S, Itoh H, Nishikawa S, Hiyama M, Tani K, Iseri T, Itoh Y, Nakaichi M, Taura Y, Itamoto K. Comparison of postoperative pain and inflammation reaction in dogs undergoing preventive laparoscopic-assisted and incisional gastropexy. J Vet Med Sci. 2017; 79(9):1524-1531. doi: 10.1292/jvms.17-0103.
34. Baron JK, Casale SA, Monnet E, Mayhew PD, Runge JJ, Follette CM, Phipps K, Powell ME, Reczynska AI, Squire NT, Barton BA, Berg J. Paramedian incisional complications after prophylactic laparoscopy-assisted gastropexy in 411 dogs. Vet Surg. 2020; 49 Suppl 1:O148-O155. doi: 10.1111/vsu.13348.
35. Sharp CR, Rozanski EA. Cardiovascular and systemic effects of gastric dilatation and volvulus in dogs. Top Companion Anim Med. 2014; 29(3):67-70. doi: 10.1053/j.tcam.2014.09.007.
36. Marks SL, Kook PH, Papich MG, Tolbert MK, Willard MD. ACVIM consensus statement: Support for rational administration of gastrointestinal protectants to dogs and cats. J Vet Intern Med. 2018; 32(6):1823-1840. doi: 10.1111/jvim.15337.
37. Langston CE, Eatroff AE. Acute Kidney Injury. In: Silverstein DC, Hopper K, editors. Small Animal Critical Care Medicine, Third Edition. St. Louis: Elsevier; 2023. p. 706-712.
38. Balakrishnan A, Silverstein DC. Shock Fluids and Fluid Challenge. In: Silverstein DC, Hopper K, editors. Small Animal Critical Care Medicine, Third Edition. St. Louis: Elsevier; 2023. p. 402-408.
39. Cassutto BH, Gfeller RW. Use of intravenous lidocaine to prevent reperfusion injury and subsequent multiple organ dysfunction syndrome. J Vet Emerg Crit Care. 2003; 13(3):137-148. doi: 10.1046/j.1435-6935.2003.00080.x
40. Buber T, Saragusty J, Ranen E, Epstein A, Bdolah-Abram T, Bruchim Y. Evaluation of lidocaine treatment and risk factors for death associated with gastric dilatation and volvulus in dogs: 112 cases (1997-2005). J Am Vet Med Assoc. 2007; 230(9):1334-1339. doi: 10.2460/javma.230.9.1334.
41. Bruchim Y, Itay S, Shira BH, Kelmer E, Sigal Y, Itamar A, Gilad S. Evaluation of lidocaine treatment on frequency of cardiac arrhythmias, acute kidney injury, and hospitalization time in dogs with gastric dilatation volvulus. J Vet Emerg Crit Care (San Antonio). 2012; 22(4):419-427. doi: 10.1111/j.1476-4431.2012.00779.x.
42. Mackenzie G, Barnhart M, Kennedy S, DeHoff W, Schertel E. A retrospective study of factors influencing survival following surgery for gastric dilatation-volvulus syndrome in 306 dogs. J Am Anim Hosp Assoc. 2010; 46(2):97-102. doi: 10.5326/0460097.
43. Lhuillery E, Velay L, Libermann S, Le Boedec K, Gautherot A, Bonneau L, Mongellas E, Harris K, Etchepareborde S. Outcomes of dogs undergoing surgery for gastric dilatation volvulus after rapid versus prolonged medical stabilization. Vet Surg. 2022; 51(5):843-852. doi: 10.1111/vsu.13763.
 by Multimédica
by Multimédica