Manejo exitoso de un paciente canino con cardiomiopatía dilatada y fibrilación auricular de aparición aguda secundarias al tratamiento con doxorrubicina
Resumen breve
La doxorrubicina es un quimioterápico eficaz en oncología veterinaria, aunque su uso está limitado por su cardiotoxicidad. Este caso describe un perro Golden Retriever de 9 años con linfoma tratado con este fármaco, que desarrolló cardiomiopatía dilatada (CMD) y fibrilación auricular (FA) tras su administración repetida. El paciente presentó debilidad, taquicardia y pulso irregular. Las pruebas diagnósticas evidenciaron cardiomegalia, FA sostenida y disfunción sistólica severa con dilatación…Índice de contenidos

Resumen
La doxorrubicina es un quimioterápico eficaz en oncología veterinaria, aunque su uso está limitado por su cardiotoxicidad. Este caso describe un perro Golden Retriever de 9 años con linfoma tratado con este fármaco, que desarrolló cardiomiopatía dilatada (CMD) y fibrilación auricular (FA) tras su administración repetida. El paciente presentó debilidad, taquicardia y pulso irregular. Las pruebas diagnósticas evidenciaron cardiomegalia, FA sostenida y disfunción sistólica severa con dilatación de las cámaras cardíacas. Se diagnosticó CMD secundaria a doxorrubicina. Se instauró tratamiento con pimobendan, diltiazem, digoxina, benazepril y espironolactona, logrando una mejoría clínica del paciente. En una semana se controló la arritmia volviendo a ritmo sinusal y, a los tres meses, los parámetros cardíacos se normalizaron, permitiendo retirar la medicación. Este caso resalta la importancia de la monitorización cardíaca y demuestra que un diagnóstico y tratamiento precoz pueden revertir los efectos adversos cardíacos.
Introducción
La doxorrubicina es un agente quimioterápico utilizado en oncología humana y veterinaria para el tratamiento de procesos oncológicos (linfoma, hemangiosarcoma, osteosarcoma, etc.)(1,2). Este fármaco genera la formación de radicales libres que dañan la membrana celular y el ADN, alterando su función(3). Su uso se encuentra limitado por su cardiotoxicidad acumulativa, pudiendo provocar disfunción sistólica cardíaca, y producir una cardiomiopatía de fenotipo dilatado, y generar arritmias severas que pueden terminar con la muerte del paciente(1,2). Este efecto se ha descrito como dosis-dependiente, y, por tanto, se debe evaluar su uso de forma individualizada(4). La doxorrubicina tiene el potencial de causar daño miocárdico, lo que lleva a la necrosis del músculo cardíaco, provocando una disminución de la función sistólica y dilatación secundaria de las cavidades, cambios que observaremos mediante ecocardiografía(5). Estos efectos se pueden llegar a producir incluso en casos donde las dosis utilizadas se encuentran dentro de los protocolos clínicamente aprobados(1,6).
La ecocardiografía es un método de diagnóstico por imagen no invasivo capaz de evaluar tanto la anatomía cardíaca, como de evaluar aspectos hemodinámicos, como la función sistólica y diastólica(7). Esta prueba se utiliza ampliamente en medicina veterinaria, y se han descrito valores de referencia para los diferentes rangos de peso y razas de perros(5). No existe consenso sobre la cardiotoxicidad sintomática en perros tratados con doxorrubicina. Aunque la dosis utilizada, el efecto residual y la condición del paciente son factores que influyen en la aparición de estos signos(5).
El objetivo de este caso clínico es mostrar los signos clínicos y cambios en pruebas complementarias asociados a la cardiotoxicidad de la doxorrubicina de forma retardada, mostrando una opción terapéutica para la estabilización y posible reversión de los efectos secundarios. En base a este caso clínico, analizaremos la evidencia científica publicada sobre el tratamiento con doxorrubicina en la especie canina y buscaremos los signos clínicos y cambios en las pruebas complementarias, como en la ecocardiografía o el electrocardiograma de superficie (ECG), que se han observado(5).
Descripción del caso
Paciente canino de raza Golden Retriever, de 31 kg y 9 años. Acude a consulta por debilidad y apatía de aparición aguda. En su historial cabe destacar el diagnóstico previo de linfoma multicéntrico estadio III subestadio A, que entró en remisión a la tercera semana de iniciar el tratamiento.
Se planificó tratamiento con protocolo Winsconsin-Madisson por ser el que suele conseguir un tiempo libre de enfermedad mayor frente a otros protocolos en linfomas de tipo B (Tabla 1).
Tabla 1. Protocolo WM19 para el tratamiento del.linfoma canino.
| Semana 1 | 0.5-0.7 mg/m2 IV Prednisona: 2 mg/kg al día PO |
| Semana 2 | Ciclofosfamida: 200-250 mg/m2 IV/PO Prednisona: 1.5 mg/kg al día PO |
| Semana 3 | Vincristina: 0.5-0.7 mg/m2 IV Prednisona: 1 mg/kg al día PO |
| Semana 4 | Doxorrubicina: 30 mg/m2 IV (1 mg/kg en perros < 15 kg) Prednisona: 0.5 mg/kg al día PO |
| Semana 6 | Vincristina: 0.5-0.7 mg/m2 IV |
| Semana 7 | Ciclofosfamida 200-250 mg/m2 IV/PO |
| Semana 8 | Vincristina: 0.5-0.7 mg/m2 IV |
| Semana 9 | Doxorrubicina: 30 mg/m2 IV (1mg/kg en perros < 15 kg) |
| Semana 11 | Vincristina: 0.5-0.7 mg/m2 IV |
| Semana 12 | Ciclofosfamida: 200-250 mg/m2 IV/PO |
| Semana 13 | Vincristina: 0.5-0.7 mg/m2 IV |
| Semana 14 | Doxorrubicina: 30 mg/m2 IV (1mg/kg en perros < 15 kg) |
| Semana 16 | Vincristina: 0.5-0.7 mg/m2 IV |
| Semana 17 | Ciclofosfamida: 200-250 mg/m2 IV/PO |
| Semana 18 | Vincristina: 0.5-0.7 mg/m2 IV |
| Semana 19 | Doxorrubicina: 30 mg/m2 IV (1mg/kg en perros < 15 kg) |
Previamente a iniciar la terapia con doxorrubicina se realizó un examen ecocardiográfico para descartar cualquier signo de disfunción sistólica o enfermedad cardíaca sub-clínica. El paciente recibió 5 sesiones con este fármaco acumulando un total de 150 mg/m2, que se encuentra dentro de los valores clínicamente seguros del fármaco.
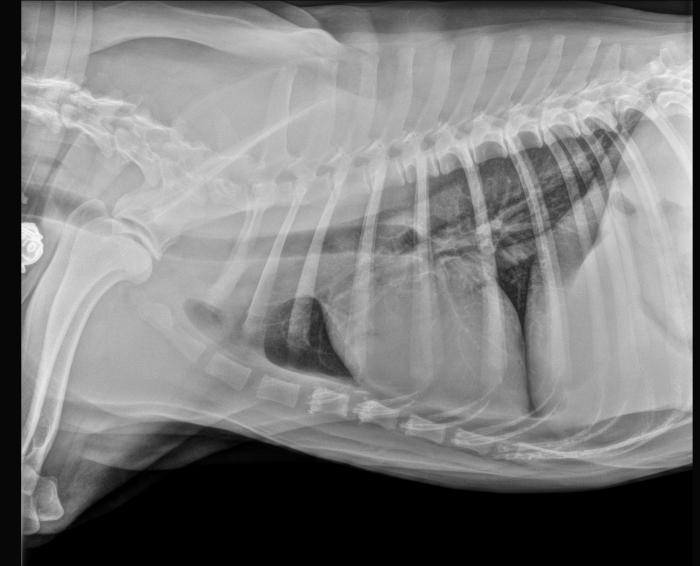
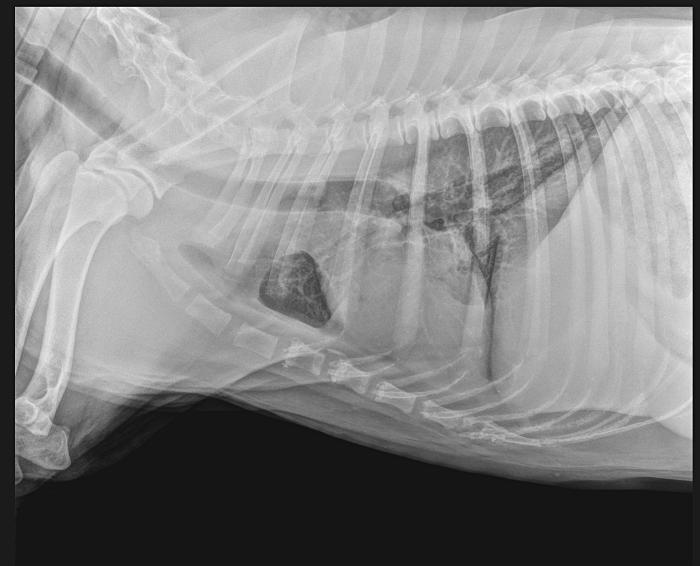
En la exploración física el día de consulta el paciente muestra dificultad para caminar y mantenerse en estación. Mucosas pálidas y pulso femoral irregular y débil. En la auscultación se detectó un ritmo irregularmente irregular con una frecuencia cardíaca de 230 latidos por minuto (lpm) y un soplo en zona de proyección mitral pansistólico grado IV/VI e hipotensión arterial sistémica evaluada mediante un medidor oscilométrico.Se realizaron pruebas complementarias, comenzando por radiografías torácicas donde el único hallazgo reseñable fue la presencia de cardiomegalia (Figura 1).
El ECG reveló la existencia de una fibrilación auricular (FA) de alta penetrancia ventricular sostenida con frecuencia cardíaca de hasta 215 lpm (Figura 2).
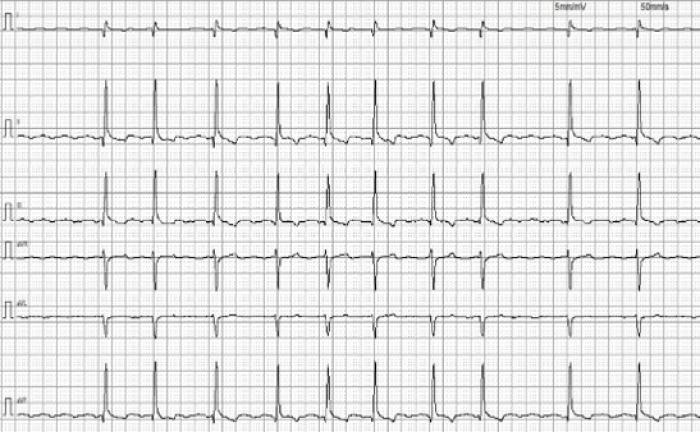
Figura 2A-B. ECG de superficie en el momento del episodio cardíaco. A) ECG 6 derivaciones, 5 mm/mV y 50 mm/s. B) ECG en derivación II, 5 mm/mV y 50 mm/s.
En la ecocardiografía nos encontramos hipertrofia excéntrica del ventrículo izquierdo (Figura 3), disfunción sistólica marcada e insuficiencia mitral concéntrica moderada con dilatación del atrio izquierdo (Tabla2).
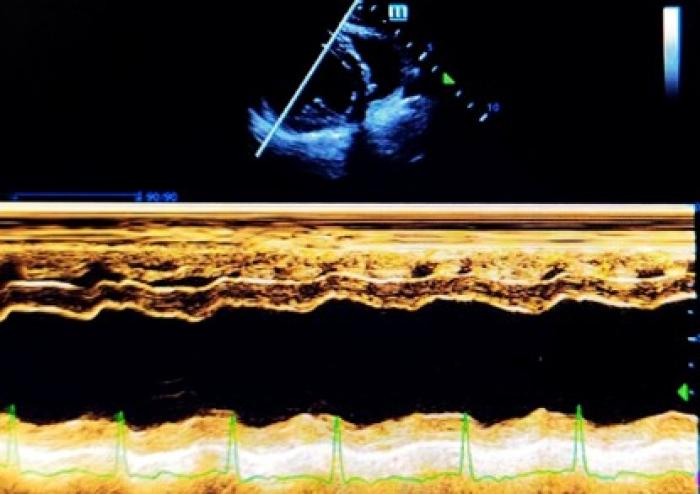
Tabla 2. Evolución de los principales parámetros ecocardiográficos del paciente.
| Parámetro | Pre Doxorrubicina | Post Doxorrubicina | Post tratamiento cardíaco |
|---|---|---|---|
| FA | 38.2 % | 27.3 % | 34.64 % |
| FE | 66.9 % | 49.7 % | 64.1 % |
| LVIDdN Cornell | 1.4 | 1.79 | 1.55 |
| LA/Ao | 1.37 | 1.8 | 1.4 |
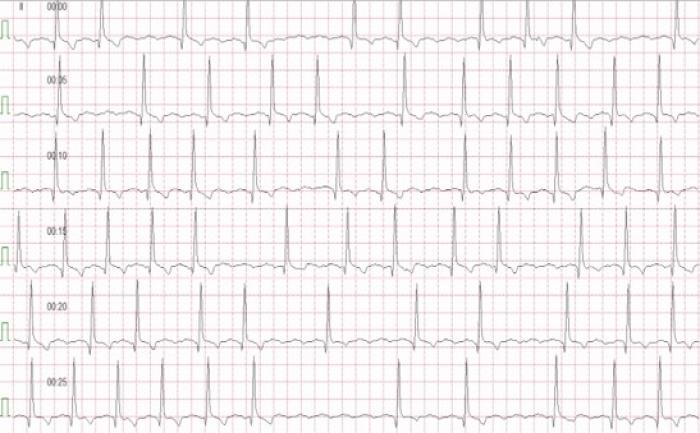
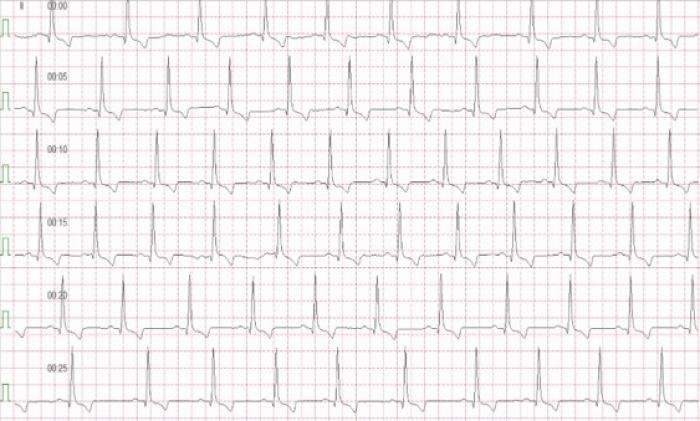
Las demás pruebas como la analítica sanguínea no mostraron alteraciones relevantes. Se diagnóstico una cardiomiopatía de fenotipo dilatado en estadio B2 con FA secundaria, todo debido probablemente al tratamiento con doxorrubicina. Iniciamos el tratamiento hospitalario con pimobendan 0.15 mg/kg intravenoso, diltiazem 1.5 mg/kg vía oral (VO) y digoxina 0.003 mg/kg VO. El paciente mostró mejoría clínica a las pocas horas de iniciar el tratamiento pudiendo caminar y encontrándose en una actitud más activa. Se decidió dar el alta hospitalaria al paciente con: pimobendan 0.25 mg/kg VO cada 12 h (BID), diltiazem 1.5 mg/kg VO cada 8 h (TID), digoxina 0.003 mg/kg VO BID, benacepril 0.25 mg/kg VO BID y espironolactona 2 mg/kg VO cada 24 h. Se revisó al paciente a las 24 h tras el alta observando una disminución notable de la frecuencia cardíaca, a pesar de que continuaba presentando FA, y mejoría de los valores ecocardiográficos (ver Tabla 2). A los 7 días la FA desapareció dando lugar a un ritmo sinusal con arritmia sinusal respiratoria (Figura4) y continuó con la mejoría de los valores ecocardiográficos (Figura5) y radiológicos (Figura6).
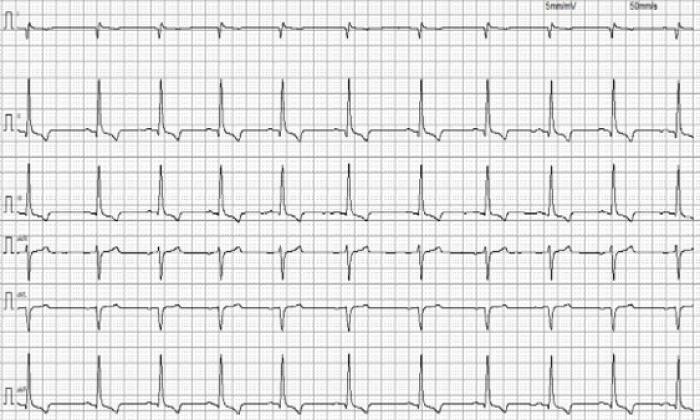
Figura 4A-B. ECG de superficie a los 7 días del episodio. A) ECG 6 derivaciones, 5 mm/mV y 50 mm/s. B) ECG en derivación II, 5 mm/mV y 50 mm/s.
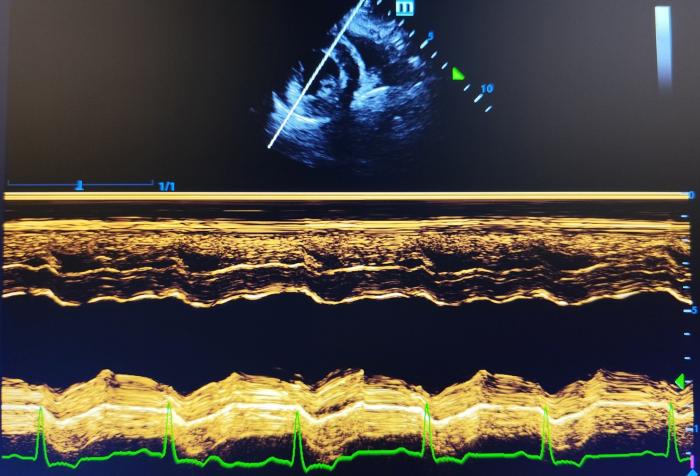
Se decidió retirar el tratamiento con digoxina y diltiazem. Tres meses tras el episodio, continua sin arritmias patológicas y los valores ecocardiográficos son compatibles con la normalidad (ver Tabla 2), retirándose el tratamiento farmacológico.
Discusión
La doxorrubicina (DOX), es una antraciclina ampliamente utilizada en tratamientos oncológicos en perros, es conocida por su efecto cardiotóxico, que causa daño celular que conduce a la dilatación cardíaca y pérdida de función(8), pudiendo producir incluso la muerte tanto en perros como en humanos(9,10), generalmente tras dosis repetidas.Los hallazgos clínicos de cardiotoxicidad incluyen arritmias y disminución de la función sistólica por disminución de la contractilidad miocárdica, lo que da lugar a una cardiomiopatía con fenotipo dilatado (CMD) (1), que se caracteriza por la hipertrofia excéntrica del ventrículo izquierdo. La CMDes una causa habitual de insuficiencia cardíaca congestiva en perros(11) que se produce al aparecer la disfunción diastólica ventricular por aumento de las presiones de llenado(12). Los signos clínicos y las formas de presentación son variables(11), aunque con la disponibilidad de pruebas como la ecografía, la capacidad para diagnosticar de forma precoz la CMD está aumentando(13,14).
La disminución de la contractilidad conduce a una reducción significativa del volumen de eyección ventricular y, por tanto, a hipotensión arterial sistémica. Esto se manifiesta clínicamente con debilidad muscular, intolerancia al ejercicio, síncope o incluso shock cardiogénico(15,16).
Las causas de la CMD incluyen agentes tóxicos (p. ej., doxorrubicina), infecciosos (p. ej., parvovirus, leishmania), nutricionales (deficiencia de taurina o L-carnitina), genéticos como en el caso de pacientes de razas como el Dóberman Pinscher o el Bóxer, o idiopáticos(12). La CDM afecta con mayor frecuencia a perros de razas grandes como los Dóberman Pinscher o Bóxer ya comentados, u otras razas como el Gran Danés, Pastor Alemán, Lebrel Irlandés, Lebrel Escocés, Terranova, San Bernardo y Labrador Retriever, que muestran una mayor prevalencia(12).
La presencia de eventos adversos cardiovasculares asociados al tratamiento con doxorrubicina está ampliamente descrito, donde la prevalencia se estima entre 4 y 18 % de los pacientes(18) incluso sin sobrepasar la dosis máxima recomendada de entre 180-240 mg/m2(2,6,17,18). Desarrollando fallo cardíaco congestivo y arritmias severas hasta en el 8.6 % de ellos(18)y pudiendo llegar a causar la muerte del paciente(2). En un estudio se evaluó la cardiotoxicidad de la DOX en 39 perros de razas con alta prevalencia de CMD: 33 perros del grupo no afectado (13 Cocker Spaniel Americano, 12 Bóxer, 5 Gran Danés y 1 de cada una de las razas Lebrel Irlandés, Dóberman y Terranova) y 6 perros del grupo que desarrollaron signos clínicos cardíacos (4 Bóxer, 1 Gran Danés y 1 Cocker Spaniel Americano)(1). Las razas caninas con alto riesgo de CMD presentaron una incidencia de cardiotoxicidad clínica del 15.4 %(1).Se observó que la cardiotoxicidad generalmente se desarrolla dentro de los 6 meses posteriores a la finalización del tratamiento, pero se ha observado episodios incluso tras varios años después del tratamiento con DOX(19-21).
Los efectos adversos detectados pueden ir desde la disminución leve de la función sistólica y aparición de eventos arritmogénicos leves como bloqueos atrio-ventriculares de 1er grado o bloqueos de rama, sin efectos hemodinámicos. Hasta la aparición de CMD y arritmias severas como taquicardias supraventriculares siendo la más habitual la FA, como taquicardias ventriculares, con repercusión hemodinámica severa(16-18). Las alteraciones miocárdicas asociadas a CMD como la fibrosis, isquemia, metabolismo celular alterado y necrosis celular, predisponen al desarrollo de las arritmias(13).
La ecocardiografía es un método no invasivo, y, por lo tanto, seguro para detectar lesiones cardíacas causadas por cardiotóxicidad(22). Pudiendo evaluar tanto el tamaño de las cámaras como la función sistólica mediante diferentes mediciones en el modo 2 D o M(23-29). Una de estas mediciones es la fracción de eyección (FE), que se muestra el porcentaje de sangre expulsada por el ventrículo izquierdo en cada ciclo cardíaco, es un parámetro utilizado para evaluar la función sistólica miocárdica y se demostró en el estudio de Herrera GC et al. de 2025 que estaba reducida en 11 de los 15 pacientes evaluados(5). Se sabe que la doxorrubicina causa varias formas de lesión cardíaca, incluyendo fibrosis miocárdica, atrofia y lisis de miocitos(30). Esta disminución del número de miocitos como su afectación al número de sarcómeros reduce la contractilidad, que es evaluada mediante una disminución de la fracción de acortamiento (FS), lo cual se observó en 8 de los 15 perros analizados(5). Por lo tanto, esta disfunción sistólica se refleja por el descenso de los índices de eyección disminuidos y el volumen sistólico residual aumentado(31). Por estas razones, siempre se debe evaluar la funcionalidad cardíaca y su electrofisiología previo a los tratamientos con doxorrubicina(6,18), pudiendo incluir además del uso de la ecocardiografía, el uso de biomarcadores cardíacos como las troponinas(32).
Aun con estos exámenes previos, se pueden llegar a producir cuadros de toxicidad cardíaca incluso tras tiempo después de la administración del fármaco(1).
Por ello, debemos ser capaces de reconocer las razas predispuestas al desarrollo de CMD, y las alteraciones secundarias al uso de la DOX, ya que los pacientes que muestren efectos adversos pueden necesitar tratamiento de urgencia que apoye la función cardíaca y frene las arritmias con impacto hemodinámico(33).
Habrá que educar a los tutores a reconocer la sintomatología asociada, ya que, estas alteraciones estructurales o electrofisiológicas pueden llegar a ser reversibles si se produce una detección temprana(33). Algunos signos clínicos son más típicos en determinadas razas. Generalmente los primeros signos clínicos detectados son: debilidad, pérdida de peso, anorexia, letargia, intolerancia al ejercicio, disnea, tos, síncopes o distensión abdominal(34).
Se han realizado estudios evaluando a pacientes sometidos a tratamiento oncológico y pacientes sanos, respectivamente(35,36). Sus hallazgos no demostraron cambios ecocardiográficos significativos, como una disminución de la FE y la FS(5), en todos los pacientes por ello la DOX sigue siendo una opción de tratamiento viable para pacientes caninos con procesos oncológicos, dada su eficacia y su bajo coste para los turores(5).
El tratamiento de soporte primario para la CMD será el uso de inotropos positivos como el pimobendán, habiendo sido utilizados en el pasado la amrinona y la milrinona, actualmente en desuso(38-43). En la actualidad, el tratamiento de los pacientes sintomáticos sigue siendo principalmente un tratamiento dirigido a controlar los síntomas de la insuficiencia cardíaca congestiva(37). Basado principalmente en el uso del pimobendán, diuréticos del asa como la furosemida e inhibidores de la enzima convertidora de angiotensina (IECA)(37). El uso de la espironolactona junto con los fármacos ya mencionados está cada vez más extendido debido a sus efectos bloqueadores de los receptores de la aldosterona y su efecto protector frente a la aparición de arritmias supraventriculares (FA)(44). Además del tratamiento de soporte cardíaco, si se observa la presencia de arritmias, los fármacos antiarrítmicos según si presenta arritmias supraventriculares o ventriculares, van a ser la base para la estabilización del paciente(33).
En nuestro caso el tratamiento de la FA con digoxina y diltiazem consiguió no solo controlar la frecuencia cardíaca del paciente a corto plazo, sino la cardioversión a un ritmo sinusal una semana tras el inicio de la arritmia. Esta cardioversión fue posible no solo gracias al tratamiento antiarrítmico, sino también al tratamiento a nivel cardíaco con pimobendán, benacepril y espironolactona. Ya que, al disminuir el volumen atrial, retiramos uno de los pilares necesarios para la aparición de un evento arritmogénico, el sustrato anatómico(45).
En la actualidad no hay ninguna forma de prevenir estos efectos adversos de forma eficaz, ya que se han observado en dosis terapéuticas, en pacientes que habían sido sometidos a exámenes cardíacos previos (ecocardiografía, ECG y medición de biomarcadores cardíacos) con resultados normales. Incluso fármacos como el carvedilol, que se han estudiado para evitar este tipo de efectos adversos, no ha demostrado todavía un efecto cardioprotector eficaz(17). La administración de rosuvastatina, por ejemplo, redujo significativamente el efecto cardiotóxico de la DOX, demostrando ser una opción para futuros estudios en perros(46).
Esta revisión, en base a un caso clínico, confirma el impacto de la DOX en la función cardíaca, revelando la importancia de una monitorización integral, que incluya evaluaciones previas, durante y después del tratamiento quimioterápico, junto con una evaluación del riesgo individualizada para cada paciente.
Por esto, las bases de un manejo exitoso de un paciente con efectos adversos severos secundarios a la DOX son: una rápida detección de la sintomatología por parte de los tutores y coordinación entre los servicios de oncología y cardiología que permita el diagnóstico e inicio del tratamiento de forma precoz. En nuestro caso esto permitió la estabilización del paciente e incluso la reversión completa de las alteraciones cardiovasculares, evitando un final fatal del paciente como se ha observado en la bibliografía(2). No obstante, a pesar de su cardiotoxicidad, la doxorrubicina sigue siendo un tratamiento oncológico valioso debido a su eficacia(5).
Bibliografía
1. Hallman BE, Hauck ML, Williams LE, Hess PR, Suter SE. Incidence and risk factors associated with development of clinical cardiotoxicity in dogs receiving doxorubicin. J Vet Intern Med. 2019;33(2):783-791.
2. Banco B, Grieco V, Servida F, Giudice C. Sudden death in a dog after doxorubicin chemotherapy. Vet Pathol. 2011;48(5):1035-1037.
3. Pereira Neto GB, Andrade J, Sousa MG, Camacho AA. Holter electrocardiography in dogs showing doxorubicin-induced dilated cardiomyopathy. Arquivo Brasileiro de Medicina Veterinária e Zootecnia 2006;58(6):1037–1042.
4. Costa FS, Sobrinho A, Roesler T, Oliveira DC, Borlini DC, Santos WG, et al. Avaliação da função miocárdica em cães e gatos pela técnica de doppler tecidual durante quimioterapia com doxorrubicina–revisão de literatura. Pubvet 2008;2(21).
5. Herrera GC, Soldi LR, Oliveira LM, Paranhos LR, Silva MJB. Impact of Doxorubicin on Cardiac Function in Dogs: Ejection Fraction Changes and Heart Failure Risk. Vet Med Sci. 2025 Sep;11(5):e70497.
6. Gallay-Lepoutre J, Bélanger MC, Nadeau ME. Prospective evaluation of Doppler echocardiography, tissue Doppler imaging, and biomarkers measurement for the detection of doxorubicin-induced cardiotoxicity in dogs: A pilot study. Res Vet Sci. 2016;105:153-159.
7. Boon JA. Veterinary echocardiography. John Wiley & Sons; 2011.
8. Surachetpong SD, Teewasutrakul P, Rungsipipat A. Serial measurements of cardiac troponin I (cTnI) in dogs treated with doxorubicin. Jpn J Vet Res 2016;64(4):221–233.
9. Billingham ME, Mason JW, Bristow MR, Daniels JR. Anthracycline cardiomyopathy monitored by morphologic changes. Cancer Treat Rep 1978;62(6) :865–872.
10. Venable RO, Saba CF, Endicott MM, Northrup NC. Dexrazoxane treatment of doxorubicin extravasation injury in four dogs. J Am Vet Med Assoc 2012;240(3):304–307.
11. Martin MWS, Stafford Johnson MJ, Celona B. Canine dilated cardiomyopathy: a retrospective study of signalment, presentation and clinical findings in 369 cases. J Small Anim Pract. 2009;50(1):23–29.
12. St Goar FG, et al. Left ventricular diastolic dysfunction in dilated cardiomyopathy. J Am Coll Cardiol. 1991;17(7):1528–1536.
13. Koch J, Pedersen HD, Jensen AL. M-mode echocardiographic diagnosis of dilated cardiomyopathy in dogs. J Vet Med A. 1995;42(1-10):599–607.
14. Kittleson MD. Dilated cardiomyopathy in dogs and cats [Internet]. MSD Veterinary Manual. 2024 [cited 2026 Mar 29]. Available from: https://www.msdvetmanual.com/circulatory-system/cardiomyopathy-in-dogs-and-cats/dilated-cardiomyopathy-in-dogs-and-cats
15. Mark D. Kittleson MD, Thomas W. Kienle RD. Small Animal Cardiovascular Medicine. St. Louis: Mosby; 1998.
16. Sisson D, Thomas WP, Bonagura JD. Textbook of canine and feline cardiology: principles and clinical practice. 2nd ed. Philadelphia: WB Saunders; 1999.
17. Pino EHM, Weber MN, de Oliveira LO, et al. Evaluation of cardioprotective effects of carvedilol in dogs receiving doxorubicin chemotherapy: A prospective, randomized, double-blind, placebo-controlled pilot study. Res Vet Sci. 2021;135:532-541.
18. Ratterree W, Gieger T, Pariaut R, Saelinger C, Strickland K. Value of echocardiography and electrocardiography as screening tools prior to Doxorubicin administration. J Am Anim Hosp Assoc. 2012;48(2):89-96.
19. Haq MM, Legha SS, Choksi J, Hortobagyi GN, Benjamin RS, Ewer M, et al. Doxorubicin‐induced congestive heart failure in adults. Cancer 1985;56(6):1361–1365.
20. Bristow MR, Mason JW, Billingham ME, Daniels JR. Doxorubicin cardiomyopathy: evaluation by phonocardiography, endomyocardial biopsy, and cardiac catheterization. Ann Intern Med 1978;88(2):168–175.
21. Moazeni S, Cadeiras M, Yang EH, Deng MC, Nguyen KL. Anthracycline induced cardiotoxicity: biomarkers and “Omics” technology in the era of patient specific care. Clin. Transl. Med. 6: 17. 2017.
22. Hanton G, Eder V, Rochefort G, Bonnet P, Hyvelin J. Echocardiography, a non-invasive method for the assessment of cardiac function and morphology in preclinical drug toxicology and safety pharmacology. Expert opinion on drug metabolism & toxicology 2008;4(6):681–696
23. Calvert CA, Brown J. Clinical findings and survival in Doberman Pinschers with dilated cardiomyopathy. J Am Vet Med Assoc. 1986;189(8):1024–1028.
24. Gooding JP, Robinson WF, Meurs KM. Echocardiographic findings in dogs with dilated cardiomyopathy. Am J Vet Res. 1986;47(2):310–316.
25. Calvert CA. Canine dilated cardiomyopathy. Vet Clin North Am Small Anim Pract. 1992;22(5):1119–1140.
26. Darke PGG. Dilated cardiomyopathy in the dog. J Small Anim Pract. 1992;33(3):104–110.
27. O’Grady MR, Horne R. Clinical features of dilated cardiomyopathy in the dog. J Small Anim Pract. 1992;33(3):115–120.
28. O’Grady MR, Horne R. Arrhythmias in canine dilated cardiomyopathy. J Vet Intern Med. 1995;9(2):75–81.
29. Calvert CA, Pickus CW, Jacobs GJ, Brown J. Signalment, survival, and prognostic factors in Doberman Pinschers with dilated cardiomyopathy. J Vet Intern Med. 1997;11(6):323–326.
30. Mauldin GE, Fox PR, Patnaik AK, Bond BR, Mooney SC, Matus RE. Doxorubicin-lnduced cardiotoxicosis clinical features in 32 dogs. Journal of Veterinary Internal Medicine 1992;6(2):82–88.
31. Morais HA. Dilated cardiomyopathy in dogs. Vet Clin North Am Small Anim Pract. 2000;30(6):1301–1320.
32. Surachetpong SD, Teewasutrakul P, Rungsipipat A. Serial measurements of cardiac troponin I (cTnI) in dogs treated with doxorubicin. Jpn J Vet Res. 2016;64(4):221-233.
33. Ware, WA: Myocardial diseases of the dog. En Ware WA y Bonagura JD (eds): Cardiovascular disease in companion animals: dog, cat and horse, Oxon, CRC Press, 2021: 631-632.
34. Montoya-Alonso JA. Miocardiopatía dilatada canina: aspectos clínicos. Anales de la Real Academia de Ciencias Veterinarias. 2005;13(13):375–402.
35. Tater G, Eberle N, Hungerbuehler S, Joetzke A, Nolte I, Wess G, et al. Assessment of cardiac troponin I (cTnI) and tissue velocity imaging (TVI) in 14 dogs with malignant lymphoma undergoing chemotherapy treatment with doxorubicin. Veterinary and comparative oncology 2017;15(1):55–64.
36. Matsuura K, Shiraishi K, Mandour AS, Sato K, Shimada K, Goya S, et al. The utility of intraventricular pressure gradient for early detection of chemotherapy-induced subclinical cardiac dysfunction in dogs. Animals 2021;11(4):1122.
37. Borgarelli M, Tarducci A, Tidholm A, Häggström J. Canine Idiopathic Dilated Cardiomyopathy. Part II: Pathophysiology and therapy. The Veterinary Journal 2001;162(3):182–195.
38. Kittleson MD, Kienle RD, Brown J, et al. Echocardiographic evaluation of canine dilated cardiomyopathy. J Am Vet Med Assoc. 1985;187(7):699–705.
39. Treadway CR. Dilated cardiomyopathy in dogs. Vet Clin North Am Small Anim Pract. 1985;15(6):1297–1312.
40. Luis Fuentes V, et al. Dilated cardiomyopathy in Doberman Pinschers: clinical and echocardiographic findings. J Small Anim Pract. 1998;39(5):219–225.
41. Lombard CW. Dilated cardiomyopathy in the dog: a review. J Vet Cardiol. 2000;2(2):3–9.
42. Kubo SH, et al. Hemodynamic and clinical features of dilated cardiomyopathy. Circulation. 1992;85(3):1089–1095.
43. Lubsen J, et al. Prognostic factors in dilated cardiomyopathy. Eur Heart J. 1996;17(5):703–709.
44. Laskary A, Fonfara S, Chambers H, O'Sullivan ML. Prospective clinical trial evaluating spironolactone in Doberman pinschers with congestive heart failure due to dilated cardiomyopathy. J Vet Cardiol. 2022 Apr;40:84-98.
45.Santilli R: En Santilli R, Moïse NS, Pariaut R, Perego M (eds): Electrocardiography of the dog and cat. Diagnosis of arrhythmias. Milano, Grupo Asís Biomedia, S.L., 2018: 52-90.
46. Kettana KM, El‑Haggar SM, Alm El-Din MA, El‑Afify DR. Possible protective effect of rosuvastatin in chemotherapy-induced cardiotoxicity in HER2 positive breast cancer patients: a randomized controlled trial. Medical Oncology 2024;41(8):196.
 by Multimédica
by Multimédica