Anestesia en toracoscopia
Resumen breve
La toracoscopia permite un abordaje mínimamente invasivo para procedimientos torácicos diagnósticos y terapeúticos, reduciendo los tiempos de recuperación, dolor postoperatorio y las posibles complicaciones. La monitorización es fundamental especialmente por el riesgo de hipoxemia y la ventilación mecánica imprescindible por los cambios en el intercambio gaseoso. La toracoscopia puede realizarse insuflando CO2, pero generalmente a no más de 3 mmHg o empleando la ventilación unipulmonar.…Índice de contenidos
Resumen
La toracoscopia permite un abordaje mínimamente invasivo para procedimientos torácicos diagnósticos y terapeúticos, reduciendo los tiempos de recuperación, dolor postoperatorio y las posibles complicaciones. La monitorización es fundamental especialmente por el riesgo de hipoxemia y la ventilación mecánica imprescindible por los cambios en el intercambio gaseoso. La toracoscopia puede realizarse insuflando CO2, pero generalmente a no más de 3 mmHg o empleando la ventilación unipulmonar. La ventilación unipulmonar puede lograrse mediante intubación selectiva, bloqueadores endobronquiales o intubación de doble lumen requiriendo siempre de asistencia broncoscópica. La ventilación unipulmonar produce una pérdida del parénquima pulmonar para el intercambio gaseoso y por tanto deben adaptarse los volúmenes de ventilación. El volumen tidal debe reducirse en un 30-50% para evitar barotrauma y la frecuencia respiratoria normalmente se incrementa un 20%. Los cuidados postoperatorios son importantes ya que, aunque los pacientes presenten menos dolor que en una toracotomía, existe riesgo de hipoxemia y también pueden acumular aire o fluido que debe ser retirado. En casos de no conseguir vaciar dicho fluido o aire, o existir un sangrado, debe considerarse la reintervención. Las complicaciones son sobretodo por la técnica toracoscópica y derivadas de la propia ventilación mecánica. Aunque en los últimos años han aumentado las indicaciones de la toracoscopia todavía existen contraindicaciones como son las grandes masas, la ausencia de espacio pleural por bridas, adherencias o aspectos anatómicos del paciente, traumas agudos, fibrosis pulmonar, la inestabilidad hemodinámica del paciente y la falta de destreza del cirujano, ya que requiere que éste haya superado la curva de aprendizaje.
Introducción
La toracoscopia es una técnica mínimamente invasiva a través de la cual se accede a la cavidad torácica a través de incisiones de 5-10 mm, proporcionando la posibilidad de realizar procedimientos tanto quirúrgicos como diagnósticos y reduciendo significativamente la morbilidad haciendo que su uso haya incrementado en las últimas décadas.
Además, la toracoscopia permite una mejor visualización del campo quirúrgico y estructuras de la cavidad torácica, así como la magnificación de éstas, una disminución significativa del dolor postoperatorio con reducción del tiempo de la recuperación del paciente, menores índices de infección y sangrado, menor tamaño de las incisiones y por tanto mejor resultado estético.
Con respecto a los procedimientos que pueden realizarse por toracoscopia son los siguientes (Tabla 1), aunque en determinados casos también pueden llevarse acabo los siguientes procedimientos (Tabla 2).
| Tabla 1. Indicaciones generales de toracoscopia. |
|
| Tabla 2. Indicaciones en casos determinados de toracoscopia. |
|
El posicionamiento del paciente es fundamental en la cirugía toracoscópica ya que en función de la técnica será necesario colocar al paciente en decúbito lateral, esternal o dorsal e incluso puede llegar a ser necesario reposicionar al paciente en algunos procedimientos.
Manejo anestésico
Al igual que en la cirugía laparoscópica, la toracoscopia requiere acceder al tórax a través de unas cánulas o trócares, pero sin embargo puede no requerir de la insuflación de CO2 para conseguir un espacio de trabajo, haciendo que la técnica sea más sencilla. Por predilección de algunos cirujanos o en función del procedimiento, puede llegar a ser necesario introducir cierta cantidad de CO2 en la cavidad pleural, creando una presión pleural positiva.
Esta pérdida de presión pleural negativa pleural implica un grado de colapso pulmonar y pérdida de eficacia en el intercambio gaseoso. Incluso a bajas presiones, p.ej. 3 mmHg, puede producirse una depresión cardiopulmonar significativa, aunque si los periodos son cortos de tiempo los efectos cardiopulmonares no son tan acusados y puede ayudar a mejorar la visualización del campo quirúrgico.
Sin embargo, hay que tener en cuenta que el empleo de estas estrategias está asociado a una mayor morbilidad y complicaciones más graves como se describirán en el apartado de complicaciones.
Todos los pacientes sometidos a toracoscopia deben de disponer de un estudio prequirúrgico que debe incluir hemograma, panel de bioquímica sérica, así como el estudio radiográfíco y ecográfico del tórax. En función del caso puede llegar a ser necesario la realización de TAC, ecografía abdominal, urianálisis, etc.
Premedicación anestésica
En función del estado de nuestro paciente ajustaremos nuestro protocolo anestésico. Tanto los alfa-2 agonistas como la acepromacina a dosis bajas tienen mínimos efectos sobre la vasoconstricción pulmonar hipóxica (VPH), la cual se describirá más adelante, por lo que su empleo a dosis bajas puede ser interesante. Los opioides tienen un efecto mínimo sobre la VPH por lo que combinados con los alfa-2 agonistas o la acepromacina nos pueden ayudar en esta fase.
Inducción anestésica
En este tipo de procedimientos esta fase es muy importante porque es cuando en muchos casos va a realizarse la intubación selectiva para poder llevar acabo la ventilación unipulmonar. En esta fase puede emplearse cualquiera de los fármacos de acción rápida (propofol, alfaxalona o etomidato).
Mantenimiento
Los anestésicos inhalatorios son los que más pueden afectar a la vasoconstricción pulmonar hipóxica de manera dosis dependiente y por tanto su combinación con opioides, ketamina, o lidocaína puede ayudar a reducir su dosis y por tanto la VPH.
El uso de corticoesteroides puede ser beneficioso, aunque no está demostrado clínicamente. De forma experimental se ha demostrado que el mantenimiento con propofol tiene mínimos efectos sobre la vasoconstricción pulmonar hipóxica y podría reducir la respuesta inflamatoria frente al edema por reexpansión.
Recuperación anestésica
Los cuidados postoperatorios tras una toracoscopia son importantes ya que, aunque los pacientes presenten menos dolor que en una toracotomía, sigue existiendo riesgo de hipoxemia que debe ser monitorizado. Todos los pacientes deberían tener implantado un tubo de toracostomía para crear un espacio pleural negativo antes de la recuperación anestésica y así poder monitorizar el espacio pleural para posibles complicaciones postoperatorias como neumotórax, piotórax y hemorragia, sobretodo durante las primeras horas.
Aquellos pacientes con enfermedad pleural de origen desconocido o efusión pericárdica pueden acumular fluido en el espacio pleural y por tanto que sea necesario extraer dicho fluido. El acúmulo de aire tras la toracoscopia debe ser vaciado y en caso de no ser posible retirarlo requerirá de la reintervención del paciente. Por último, si la presencia de sangre en el espacio pleural es significativa, será imperativa la reintervención del paciente.
Monitorización
Durante todo el procedimiento es fundamental llevar acabo una monitorización continua del paciente especialmente por el riesgo de hipoxemia y los cambios en el intercambio gaseoso por la ventilación unipulmonar.
Pulsioximetria
Desde el principio del procedimiento anestésico debe vigilarse la saturación de oxígeno, ya que si desde el comienzo la saturación es baja el riesgo de hipoxemia severa durante la cirugía es más alto. Lo ideal es disponer de la posibilidad de realizar una gasometría arterial para conocer con exactitud el intercambio gaseoso.
Si la saturación de oxígeno se encontrase por debajo del 95% o la PaO2 por debajo de 100 mmHg se deben de tomar medidas para mejorar la oxigenación arterial como son comprobar el tubo endotraqueal, aspirar posibles secreciones, realizar un reclutamiento alveolar y aumentar la PEEP, subir la FiO2 a 1 y aplicar CPAP de 5 cm H20 en el pulmón proclive.
Capnografía
El capnógrafo proporciona información tanto sobre el estado de ventilación como del estado de circulación del paciente. En general no es complicado mantener la normocapnia durante la toracoscopia, aunque se realice una ventilación unipulmonar, pero la diferencia entre el CO2 arterial (PaCO2) y el CO2 alveolar (FeCO2) puede aumentar de los 5 mmHg, que suele encontrarse en condiciones normales a 10 ó15 mmHg. Si esto ocurre indica que el espacio muerto alveolar debe ser corregido para mejorar la eficacia ventilatoria.
Electrocardiografía
Es imprescindible durante todo el procedimiento monitorizar el electrocardiograma para detectar posibles arritmias que puedan desencadenarse durante el procedimiento y en el caso de producirse alguna poder tratarla.
Espirometría
En la actualidad hay distintos monitores que pueden medir el flujo y la presión de los gases durante la ventilación, permitiendo al monitor hacer cálculos de complianza y resistencia pulmonar. Mediante los cambios en la complianza pulmonar y en la resistencia pulmonar se puede valorar la dinámica respiratoria en todo momento y ajustar los parámetros ventilatorios de manera más eficiente.
Temperatura corporal
Es muy importante vigilar la temperatura durante todo el procedimiento ya que la hipotermia disminuye la vasoconstricción pulmonar hipóxica y especialmente si se alarga la intervención pueden perder temperatura rápidamente.
Ventilación mecánica
La toracoscopia debe realizarse bajo anestesia general y disponer de ventilación mecánica ya que, en función de la cirugía, puede ser necesario ajustar la frecuencia respiratoria o el volumen tidal para obtener una buena visualización de las estructuras anatómicas que se están interviniendo. Además, durante la toracoscopia aparecen cambios respiratorios muy importantes que hace que la ventilación mecánica sea imprescindible.
Por otro lado, en determinados procedimientos o situaciones, resulta conveniente realizar el colapso selectivo del pulmón del hemitórax en el que se vaya a trabajar (Figura 1) ya que aumenta el espacio de trabajo y se logra una mejor exposición del área a intervenir. La mejora de la visualización también puede ayudar a evitar el traumatismo iatrogénico a los tejidos que puede producirse cuando la visibilidad se ve afectada.
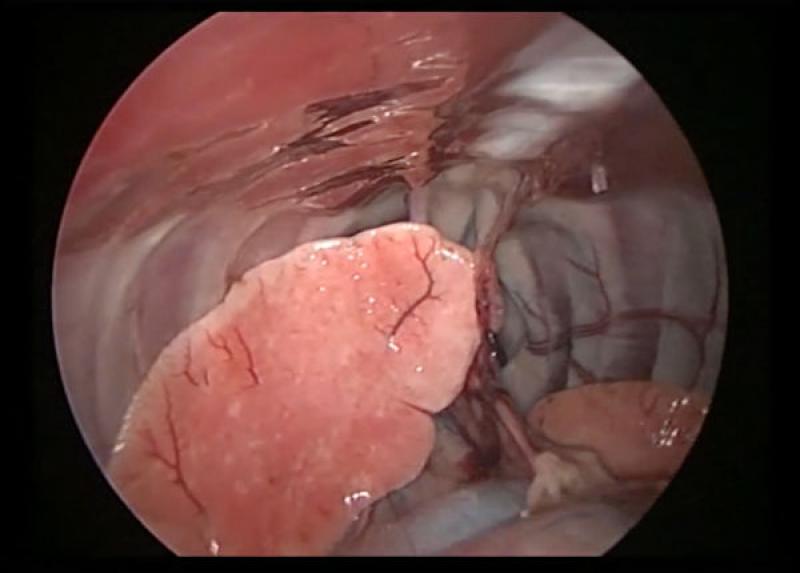
Ventilación unipulmonar
La ventilación unipulmonar, aunque en medicina humana se emplea de forma rutinaria en cirugías torácicas, en veterinaria es poco habitual porque requiere de la intubación selectiva y ventilar a los pacientes con equipamiento más especializado. La ventilación unipulmonar produce una pérdida de parénquima pulmonar para el intercambio gaseoso y por tanto deben adaptarse los volúmenes de ventilación a esta situación.
El volumen tidal debe reducirse en un 30-50% para evitar barotrauma y la frecuencia respiratoria normalmente se incrementa un 20%. El uso de PEEP a 5 cm H2O puede ser útil durante la ventilación unipulmonar y se ha demostrado que aumenta la presión parcial arterial de oxígeno y disminuye el shunt sin afectar de forma significativa al gasto cardíaco. Con respecto a las dimensiones de los tubos endotraqueales, debe de tenerse en cuenta que los bloqueadores bronquiales están diseñados para medicina humana y las diferencias anatómicas de los perros y gatos pueden ser una dificultad añadida para su empleo además de que por tanto no hay disponibilidad para gatos o perros pequeños.
Pueden utilizarse varias técnicas para crear ventilación unipulmonar, como el uso de bloqueadores endobronquiales, la intubación selectiva o la intubación endobronquial de doble lóbulo (Tabla 3). Todos suelen requerir de una implantación asistida mediante broncoscopia (Figura 2). Los más útiles son los tubos de doble luz Robertshaw y los bloqueadores bronquiales.
| Tabla 3. Recomendaciones para mecanismos ventilación unipulmonar. |
| Mecanismo | Perros <10kg | Perros 10-30kg | Perros >30kg | Gatos |
| Intubación selectiva | No | No | Sí | No |
| Intubación endobronquial doble lumen | No | Sí | No | No |
| Bloqueadores bronquiales | Sí | Sí | Sí | Sí |
Los tubos de doble luz Robertshaw tienen dos tubos independientes, con dos balones de neumotaponamiento diferentes para poder trabajar con cada pulmón de forma separada y pueden ser de derecha o de izquierda. A nivel comercial se pueden encontrar los sistemas Portex (Keene, NH), Rüsch (Teleflex Medical) y Research Triangle Park).
Los bloqueadores endobronquiales son relativamente fáciles de posicionar y consisten en un catéter con punta de globo que se ubica dentro del lumen de un tubo endotraqueal estándar. En la mayoría de los modelos, el broncoscopio pasa a través de un bucle de la punta del catéter con punta de balón a medida que se introduce en el lumen del tubo endotraqueal. Esto permite que el catéter con punta de balón sea guiado por el broncoscopio hacia el interior de uno u otro bronquio principal de tal forma que cuando se dilata el balón, se impide que el flujo de gas fresco entre en el bronquio principal derecho o izquierdo, ahora obstruido.
Uno de los bloqueadores bronquiales más empleados es el EZ-Blockerque posee un balón en cada una de las terminaciones de su extremo distal con el fin de alojarlos en ambos bronquios principales, adaptándose a la forma de la carina (Figura 3A y Figura 3B). La principal desventaja del EZ-Blocker es que requiere de diámetros traqueales de al menos 8,7 mm para el bloqueo bronquial colateral consecutivo en paciente canino. No obstante, evita la necesidad de realizar cambios en la posición del paciente o del campo quirúrgico durante la maniobra del colapso bronquial contralateral.
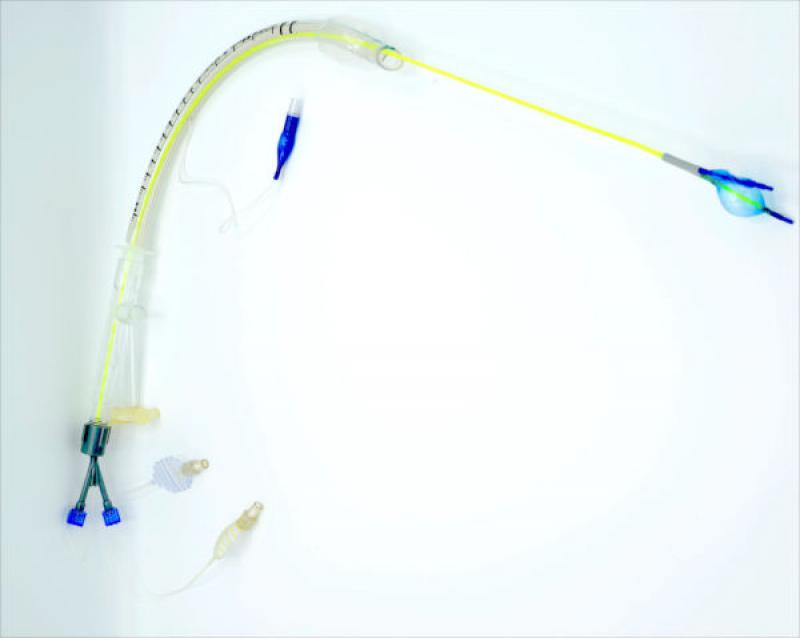
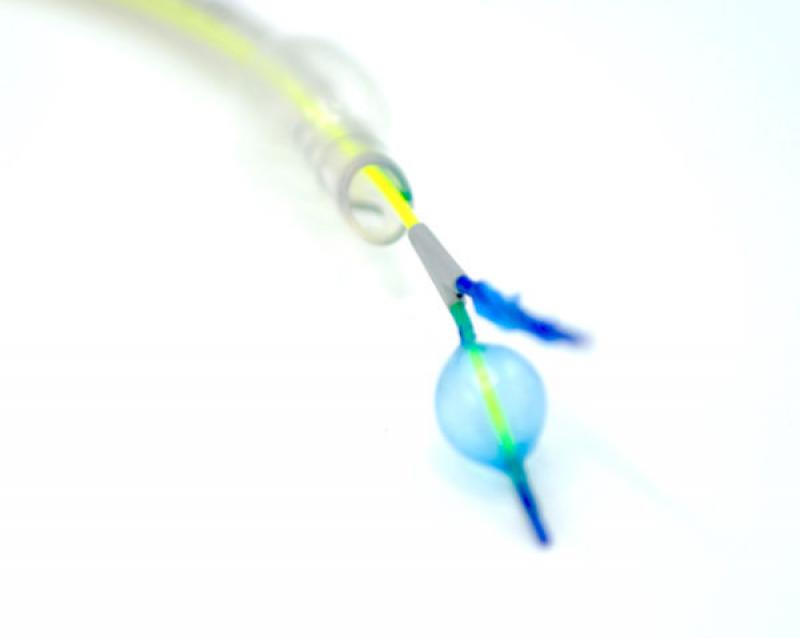
Los tubos endobronquiales de doble lumen son un poco más difíciles de implantar, pero tienen la ventaja de permitir la alternancia de la ventilación pulmonar, que puede ser útil en situaciones en las que ambos lados de la cavidad torácica deban ser exploradas o en los que se desconozca en qué lado se encuentra una lesión.
Siempre que se utilice ventilación unipulmonar se deben anticipar cambios fisiológicos significativos, ya que se produce un desajuste significativo entre la ventilación y la perfusión como resultado de una perfusión de pulmón no ventilado.
En el caso de presentarse una situación de hipoxemia durante la ventilación unipulmonar deben de recordarse las 5 causas principales de hipoxia que son: disminución de la FiO2, hipoventilación, desajuste en la ventilación/perfusión, shunt vascular y problemas en la difusión. En el caso de la ventilación unipulmonar el origen de la hipoxia puede ser por cualquiera de las causas anteriores.
Si la FiO2 es menor a 1 entonces debe incrementarse hasta 1 si fuera necesario. La hipoventilación aumenta los niveles de CO2 y esto puede favorecer la hipoxia al igual que la atelectasia. El empleo de maniobras de reclutamiento puede ayudar a evitar la atelectasia y mejorar la oxigenación. Además, el desajuste en la ventilación/perfusión puede minimizarse con las maniobras de reclutamiento y la PEEP. El shunt vascular puede reducirse al minimizar la vasoconstricción pulmonar hipóxica reduciendo las concentraciones de anestesia inhalatoria al combinarla con inyectables.
En cuanto a los problemas en la difusión, éstos son debidos a que solo se está ventilando un pulmón pero el empleo de presión positiva continua (CPAP) en la vía aérea a 3 cm H2O puede ayudar a minimizar la hipoxia sin interferir con el campo quirúrgico.
En cuanto al modo ventilatorio, la recomendación es emplear el modo de ventilación controlada por volumen ya que proporciona más información sobre la mecánica respiratoria y existe un menor riesgo de hipoventilación. A la hora de programar el ventilador hay que tener en cuenta si ha sido necesario realizar el colapso pulmonar y ventilación unipulmonar o no. En el caso de no ser necesario el colapso pulmonar y la ventilación unipulmonar se puede programar el ventilador de la siguiente manera:
- FiO2: 0,6-0,8
- Volumen tidal: 8-10 ml/kg
- Frecuencia respiratoria: 15-20 rpm
- Ti: 1 segundo
- Tpi: 0,3-0,5 segundos
- Presión meseta: 8-10 cm H2O
- PEEP: < 3 mmHg
En el caso de ser necesario el colapso pulmonar y la ventilación unipulmonar entonces se puede programar el ventilador de la siguiente manera:
- FiO2: 0,6-0,8
- Volumen tidal: 6-8 ml/kg
- Frecuencia respiratoria: 20-25 rpm
- Ti: 0,8-1 segundo
- Tpi: 0,3-0,5 segundos
- Presión meseta: 8-10 cm H2O
- PEEP: 5-8 mmHg
Vasoconstricción pulmonar hipóxica (VPH)
La vasoconstricción pulmonar hipóxica es una respuesta fisiológica que se produce en las áreas del pulmón mal ventiladas (hipóxicas) aumentando la resistencia de los vasos sanguíneos pulmonares y reduciendo la perfusión pulmonar en esa zona. Los estudios han demostrado que no se produce un gran efecto sobre el suministro de
oxígeno en perros sanos durante la ventilación pulmonar unilateral. Este mecanismo tiene una función protectora por lo que debe intentar mantenerse intacto ya que sino podría producirse un aumento de espacio muerto y shunt.
Algunos fármacos pueden alterar la ventilación pulmonar hipóxica como los anestésicos inhalatorios, el propofol, los antiinflamatorios no esteroideos (AINES), la hipocapnia y la hipotermia (Tabla 4).
| Tabla 4. Factores que influyen en la vasoconstricción pulmonar hipóxica. |
| Factor | Efecto sobre VPH | Referencias |
| Aumento PA | ↓ Respuesta VPH | Lejeune et al |
| PEEP o CPAP | ↓ Respuesta VPH | Lejeune et al |
| Hipotermia | ↓ Respuesta VPH | Benumof and Wahrenbrock |
| Alcalosis respiratoria | ↓ Respuesta VPH | Lloyd and Silove et al |
| Alcalosis metabólica | ↓ Respuesta VPH | Lloyd and Silove et al |
| Alfa 2 agonistas | Mínimo efecto | Jernan et al |
| Opioides | Mínimo efecto | Bjertnaes |
| Lidocaína | Mínimo efecto | Bindslev et al |
| Propofol | ↑ Respuesta VPH | Nakayama and Murray |
| Ketamina | Mínimo efecto | Nakayama and Murray |
| Tiopental | Minimo efecto | Bjertnaes, Carlsson et al |
| Anestesia inhalatoria | Dosis dependiente, si 1CAM mínimo efecto | Benumof and Wahrenbrock,Lejeune et al, Lennon and Murray, Lesitsky et al |
| AINES | Cox-1 ↑ Respuesta VPH COX-2 ↓ Respuesta VPH | Lennon and Murray, Kylhammar and Radegran |
Aumento de las resistencias de la vía aérea
Los tubos endotraqueales empleados en la ventilación unipulmonar reducen el diámetro de la vía aérea a la mitad y esto hace que aumente la resistencia al paso de aire. En el monitor del ventilador podremos ver un aumento en la presión pico no pero no en la presión meseta.
Reexpansión del pulmón
La incidencia de complicaciones postoperatorias después de anestesias unipulmonares prolongadas en humana es alta. Durante la anestesia unipulmonar, si el lado colapsado no se reexpande, el pulmón estará hipoperfundido por la vasoconstricción pulmonar hipóxica. Esta reexpansión provoca una respuesta inflamatoria aguda con liberación de sustancias citotóxicas que pueden ocasionar un edema pulmonar o un daño pulmonar.
Se han estudiado distintos métodos para reducir la respuesta inflamatoria, pero sin un consenso generalizado. Los corticoides se han aplicado de manera sistémica y (metilprednisolona) e inhalatoria (budesonida) para mejorar la función pulmonar y reducir la respuesta inflamatoria. La liberación de citoquinas se redujo al emplear presión positiva continua en las vías respiratorias (CPAP) a 5 cmH2O de oxígeno al pulmón colapsado. Sin embargo, debe de tenerse en cuenta que el empleo de la CPAP puede reducir el campo quirúrgico disminuyendo la visualización y por tanto deba ser retirada.
Manejo analgésico
A pesar de que los procedimientos mínimamente invasivos disminuyen el dolor relacionado con la cirugía, puede desencadenarse una respuesta nociceptiva como consecuencia de la introducción de los trócares y la manipulación de estructuras pudiendo aparecer dolor en el postoperatorio.
Los agonistas alfa-2 además de ser sedantes también proporcionan analgesia y se emplean sobretodo en la premedicación, aunque pueden ser utilizados durante la cirugía en infusión continua o incluso durante la recuperación anestésica a dosis bajas para proporcionar un despertar más suave y tranquilo.
Los opioides combinados con los alfa-2 agonistas potencian la sedación y proporcionan una buena analgesia siendo la morfina y la metadona los más empleados. Pueden usarse en el postoperatorio, pero normalmente no son necesarios opioides tan potentes y por tanto con una buprenorfina o tramadol suele ser suficiente.
Los AINEs proporcionan una buena analgesia y pueden emplearse tanto en el periodo preoperatorio como intraoperatorio como en el postoperatorio, pero en pacientes de mayor riesgo anestésico suele reservarse su uso para el intraoperatorio o postoperatorio y lo normal es prolongar su uso 5-7 días.
Los anestésicos locales pueden emplearse en bloqueo incisional, como anestesia interpleural o en bloqueo intercostal o paravertebral. El bloqueo incisional puede realizarse antes o después de la cirugía y normalmente se emplea un anestésico local en la zona donde se van a colocar o se han colocado los trócares de la toracoscopia. La dosis que suele emplearse es de 0,1 ml/kg por punto.
La anestesia interpleural consiste en instilar anestésico local como la bupivacaina al 0,25-0,5% antes del cierre en la cavidad torácica, a una dosis de 1-2 ml/kg, proporcionando analgesia durante 12-24 horas. El bloqueo intercostal o paravertebral se realiza de cada espacio intercostal donde se haya colocado un puerto de trabajo y deben bloquearse también el nervio anterior y posterior. Generalmente se emplea bupivacaina al 0,5% o combinada con dexmedetomidina (1 mcg/ml), que puede garantizar analgesia durante 24 horas.
Complicaciones
Técnica Toracoscópica
La implantación de los trócares es un punto crítico de la toracoscopia debido a que la mayor parte de las complicaciones ocurren en este punto. Las principales complicaciones son las siguientes:
- La lesión de los vasos intercostales que producirá un sangrado abundante que puede requerir de la reconversión a cirugía abierta.
- La lesión del parénquima pulmonar al introducir el primer trócar sobretodo si hay adherencias entre el pulmón y la pared torácica.
- La lesión de los grandes vasos supone una complicación muy grave si no se resuelve a tiempo, aunque es poco frecuente salvo en casos de cirugías para la corrección del cuarto arco aórtico persistente o en resecciones de masas mediastínicas.
- La laceración del parénquima pulmonar durante la cirugía debido a una tracción excesiva del tejido al retraer el pulmón.
- La lesión de los nervios frénicos durante la realización de la pericardiectomía.
- La lesión del epicardio también puede producirse durante la pericardiectomía.
- Tras la realización de una biopsia pulmonar o una lobectomía se puede producir fuga aérea debido a la dehiscencia de la sutura o por un mal manejo del parénquima pulmonar.
- Las principales complicaciones postquirúrgicas son infección de las incisiones, el desarrollo de seroma o enfisema subcutáneo así como metástasis en los puntos de colocación de los trócares.
- La aparición de algunas de estas complicaciones puede suponer la reconversión a cirugía abierta.
Ventilación mecánica
Volutrauma
El uso de elevados volúmenes tidales genera lesiones pulmonares por lo que la estrategia ventilatoria para evitar esto es emplear volúmenes tidales bajos (6-8 ml/kg) y elevadas frecuencias respiratorias (20-25 rpm). Este tipo de estrategias se han empleado en medicina humana y están asociadas con una menor respuesta inflamatoria y menores complicaciones pulmonares postoperatorias.
Atelectrauma
El uso de concentraciones elevadas de oxígeno predispone a la aparición de atelectasias en paciente canino y felino incluso en procedimientos cortos. Las zonas de atelectasia pueden dar lugar a lesiones de tejido. Además, las zonas de atelectasia no se expanden y las partes aireadas del pulmón se expanden más de lo normal pudiendo generar volutrauma en esas regiones. La estrategia es evitar la formación de atelectasias y minimizar el colapso de la vía aérea instaurando PEEP ya que, aunque se empleen elevados volúmenes tidales la adición de PEEP disminuye la lesión pulmonar.
La estrategia alternativa es reducir la concentración de oxígeno inspirado (FiO2) a 0,4 para que se mantenga el nitrógeno en el pulmón y evite la formación de atelectasias. Sin embargo, esto no siempre es posible y aquellos pacientes que necesiten una FiO2 de 1,0 requerirán de la realización de maniobras de reclutamiento alveolar.
Contraindicaciones
A pesar de que en los últimos años han aumentado las indicaciones de la toracoscopia en los últimos años, todavía existen una serie de contraindicaciones en la toracoscopia. La resección de grandes masas por toracoscopia hace que sean difíciles de manejar y para poderlas extraer, puede suponer en ciertos casos tener que ampliar la toracotomía.
La ausencia de espacio pleural por bridas, adherencias o por aspectos anatómicos del paciente como ocurre en razas braquicéfalas puede llegar hacer que no pueda realizarse con seguridad el procedimiento teniendo que reconvertir a cirugía abierta. Además, los traumas agudos de tórax requieren de una actuación rápida y por tanto son difíciles de resolver por toracoscopia.
También la inestabilidad hemodinámica del paciente también hace que esté contraindicado, y en los casos de fibrosis pulmonar está comprometida la correcta reexpansión del pulmón al finalizar la cirugía. Finalmente, la destreza del cirujano es fundamental para poder llevar acabo la toracoscopia ya que para llevar acabo este tipo de abordaje es necesario haber superado una curva de aprendizaje.
Bibliografía
- Bindslev L, Cannon D, Sykes MK. Reversal of nitrous oxide-induced depression of hypoxic pulmonary vasoconstriction by lignocaine hydrochloride during collapse and ventilation hypoxia of the left lower lobe. Br J Anaesth. 1986 Apr;58(4):451-6.
- Bjertnaes LJ. Hypoxia-induced vasoconstriction in isolated perfused lungs exposed to injectable or inhalation anesthetics. Acta Anaesthesiol Scand. 1977;21(2):133-47.
- Bjertnaes L, Hauge A, Kriz M. Hypoxia-induced pulmonary vasoconstriction: effects of fentanyl following different routes of administration. Acta Anaesthesiol Scand. 1980;24(1):53-7.
- Benumof JL, Wahrenbrock EA. Dependency of hypoxic pulmonary vasoconstriction on temperature. J Appl Physiol Respir Environ Exerc Physiol. 1977 Jan;42(1):56-8.
- Benumof JL, Wahrenbrock EA. Local effects of anesthetics on regional hypoxic pulmonary vasoconstriction. Anesthesiology. 1975 Nov;43(5):525-32.
- Boel A. Fransson, Philipp D. Mayhew Small Animal Laparoscopy and Thoracoscopy, Wiley First Edition (2015), 255-268.
- Carlsson AJ, Bindslev L, Santesson J, Gottlieb I, Hedenstierna G. Hypoxic pulmonary vasoconstriction in the human lung: the effect of prolonged unilateral hypoxic challenge during anaesthesia. Acta Anaesthesiol Scand. 1985 Apr;29(3):346-51.
- Casas D.L, Santana AJ, Técnicas de Mínima Invasión en Pequeños Animales, 2018, Ediciones Multimédica, 58-63.
- Daly CM, Swalec-Tobias K, Tobias AH, Ehrhart N. Cardiopulmonary effects of intrathoracic insufflation in dogs. J Am Anim Hosp Assoc. 2002 Nov-Dec;38(6):515-20.
- Dreyfuss D, Soler P, Basset G, Saumon G. High inflation pressure pulmonary edema. Respective effects of high airway pressure, high tidal volume, and positive end-expiratory pressure. Am Rev Respir Dis. 1988 May;137(5):1159-64.
- Faunt KK, Cohn LA, Jones BD, Dodam JR. Cardiopulmonary effects of bilateral hemithorax ventilation and diagnostic thoracoscopy in dogs. Am J Vet Res. 1998 Nov;59(11):1494-8.
- Hemmes SN, Serpa Neto A, Schultz MJ. Intraoperative ventilatory strategies to prevent postoperative pulmonary complications: a meta-analysis. Curr Opin Anaesthesiol. 2013 Apr;26(2):126-33.
- Hogue CW Jr. Effectiveness of low levels of nonventilated lung continuous positive airway pressure in improving arterial oxygenation during one-lung ventilation. Anesth Analg. 1994 Aug;79(2):364-7.
- Ju NY, Gao H, Huang W, Niu FF, Lan WX, Li F, Gao W. Therapeutic effect of inhaled budesonide (Pulmicort® Turbuhaler) on the inflammatory response to one-lung ventilation. Anaesthesia. 2014 Jan;69(1):14-23.
- Kernan, S., Rehman, S., Meyer, T., Bourbeau, J., Caron, N., & Tobias, J. D. (2011). Effects of dexmedetomidine on oxygenation during one-lung ventilation for thoracic surgery in adults. Journal of minimal access surgery, 7(4), 227–231.
- Kylhammar D, Rådegran G. Cyclooxygenase-2 inhibition and thromboxane A(2) receptor antagonism attenuate hypoxic pulmonary vasoconstriction in a porcine model. Acta Physiol (Oxf). 2012 Aug;205(4):507-19.
- Kudnig ST, Monnet E, Riquelme M, Gaynor JS, Corliss D, Salman MD. Cardiopulmonary effects of thoracoscopy in anesthetized normal dogs. Vet Anaesth Analg. 2004 Apr;31(2):121-8.
- Kudnig ST, Monnet E, Riquelme M, Gaynor JS, Corliss D, Salman MD. Effect of positive end-expiratory pressure on oxygen delivery during 1-lung ventilation for thoracoscopy in normal dogs. Vet Surg. 2006 Aug;35(6):534-42.
- Lejeune P, De Smet JM, de Francquen P, Leeman M, Brimioulle S, Hallemans R, Melot C, Naeije R. Inhibition of hypoxic pulmonary vasoconstriction by increased left atrial pressure in dogs. Am J Physiol. 1990 Jul;259(1 Pt 2):H93-100.
- Lejeune P, Vachiery JL, De Smet JM, Leeman M, Brimioulle S, Delcroix M, Melot C, Naeije R. PEEP inhibits hypoxic pulmonary vasoconstriction in dogs. J Appl Physiol (1985). 1991 Apr;70(4):1867-73
- Lennon PF, Murray PA. Attenuated hypoxic pulmonary vasoconstriction during isoflurane anesthesia is abolished by cyclooxygenase inhibition in chronically instrumented dogs. Anesthesiology. 1996 Feb;84(2):404-14.
- Lhermette P, Sobel D, Robertson E, BSAVA Canine and Feline Endoscopy and Endosurgery. Second edition 2020, 218-221, 233-234.
- Lloyd, T.C. Jr. Role of nerve pathways in the hypoxic vasoconstriction of the lung. J Appl Phyysiol 21, 1351-1355 (1966).
- Mayhew PD, Pascoe PJ, Shilo-Benjamini Y, Kass PH, Johnson LR. Effect of One-Lung Ventilation With or Without Low-Pressure Carbon Dioxide Insufflation on Cardiorespiratory Variables in Cats Undergoing Thoracoscopy. Vet Surg. 2015 Jul;44 Suppl 1:15-22.
- Misthos P, Katsaragakis S, Theodorou D, Milingos N, Skottis I. The degree of oxidative stress is associated with major adverse effects after lung resection: a prospective study. Eur J Cardiothorac Surg. 2006 Apr;29(4):591-5.
- Nakayama M, Murray PA. Ketamine preserves and propofol potentiates hypoxic pulmonary vasoconstriction compared with the conscious state in chronically instrumented dogs. Anesthesiology. 1999 Sep;91(3):760-71.
- Park J, Lee HB, Jeong SM. Comparison of the effects of isoflurane versus propofol-remifentanil anesthesia on oxygen delivery during thoracoscopic lung lobectomy with one-lung ventilation in dogs. J Vet Sci. 2018 May 31;19(3):426-433.
- Silove ED, Inoue T, Grover RF. Comparison of hypoxia, pH, and sympathomimetic drugs on bovine pulmonary vasculature. J Appl Physiol. 1968 Mar;24(3):355-65.
- Staffieri F, Franchini D, Carella GL, Montanaro MG, Valentini V, Driessen B, Grasso S, Crovace A. Computed tomographic analysis of the effects of two inspired oxygen concentrations on pulmonary aeration in anesthetized and mechanically ventilated dogs. Am J Vet Res. 2007 Sep;68(9):925-31.
- Staffieri F, De Monte V, De Marzo C, Grasso S, Crovace A. Effects of two fractions of inspired oxygen on lung aeration and gas exchange in cats under inhalant anaesthesia. Vet Anaesth Analg. 2010 Nov;37(6):483-90.
- Tams, T. & Rawlings, C... Small Animal Endoscopy. Elsevier Third Edition 2011; 479, 482-483, 495
- Theroux MC, Olivant A, Lim D, Bernardi JP, Costarino AT, Shaffer TH, Miller TL. Low dose methylprednisolone prophylaxis to reduce inflammation during one-lung ventilation. Paediatr Anaesth. 2008 Sep;18(9):857-64.
- Verhage RJ, Boone J, Rijkers GT, Cromheecke GJ, Kroese AC, Weijs TJ, Borel Rinkes IH, van Hillegersberg R. Reduced local immune response with continuous positive airway pressure during one-lung ventilation for oesophagectomy. Br J Anaesth. 2014
- Wolthuis EK, Choi G, Dessing MC, Bresser P, Lutter R, Dzoljic M, van der Poll T, Vroom MB, Hollmann M, Schultz MJ. Mechanical ventilation with lower tidal volumes and positive end-expiratory pressure prevents pulmonary inflammation in patients without preexisting lung injury. Anesthesiology. 2008 Jan;108(1):46-54.
- Wormser C, Singhal S, Holt DE, Runge JJ. Thoracoscopic-assisted pulmonary surgery for partial and complete lung lobectomy in dogs and cats: 11 cases (2008-2013). J Am Vet Med Assoc. 2014 Nov 1;245(9):1036-41.
 by Multimédica
by Multimédica