Abordaje endovascular al ventrículo derecho doble cámara
Resumen breve
El ventrículo derecho de doble cámara (DCRV) es una enfermedad cardíaca congénita poco común, en la que se produce un impedimento del paso del flujo sanguíneo dentro del ventrículo derecho. Este puede llegar a obstruirse por completo, aunque por lo general produce de forma crónica una insuficiencia cardiaca congestiva y/o la muerte súbita del paciente1,2. Concretamente en nuestro paciente se apreció una membrana con anclaje fibro-muscular al ventrículo derecho, poco frecuente y compatible…Índice de contenidos
Introducción
El ventrículo derecho de doble cámara (DCRV) es una enfermedad cardíaca congénita poco común, en la que se produce un impedimento del paso del flujo sanguíneo dentro del ventrículo derecho. Este puede llegar a obstruirse por completo, aunque por lo general produce de forma crónica una insuficiencia cardiaca congestiva y/o la muerte súbita del paciente1,2. Concretamente en nuestro paciente se apreció una membrana con anclaje fibro-muscular al ventrículo derecho, poco frecuente y compatible con DCRV, al que se sumaron insuficiencia tanto aórtica como pulmonar. Los signos clínicos más característicos son: soplo de grado III-IV/VI, debilidad generalizada, intolerancia al ejercicio, síncope, mucosas pálidas, tos intermitente y ascitis progresiva, pudiendo evolucionar a insuficiencia cardíaca congestiva2-4. Se puede asociar a otras enfermedades congénitas y su diagnóstico se establece en función del examen clínico y la ecocardiografía como prueba de elección en diagnóstico por imagen. El tratamiento se basa en el manejo de la insuficiencia cardíaca congestiva1 y en su resolución quirúrgica si fuese posible bien por técnicas quirúrgicas abiertas o más recientemente técnicas endovasculares.
Caso clínico
Se presenta un paciente canino, Bóxer macho no castrado de casi 6 meses de edad que fue referido al servicio de cardiología del hospital para su evaluación tras ser detectado un soplo sistólico durante un examen rutinario de cachorro. Los propietarios comentaban que el perro no muestra signos aparentes de patología cardiaca, si bien sí denotan un leve retraso en el crecimiento con respecto a sus hermanos. A la exploración se encontraba alerta, con un peso de 16 kg y una condición corporal de 3/6.
La exploración física no muestra alteraciones a nivel de coloración de mucosas, ni tiempo de relleno capilar, pulso femoral normocinético y relación 1:1 con latido cardiaco, no existe distensión aparente de yugulares, ni presencia de pulso en las mimas. A la auscultación pulmonar no existen alteraciones, pero si se pone de manifiesto un soplo sistólico cardiaco con punto de máxima intensidad en hemitórax derecho (grado IV/VI).
El resto del examen clínico junto a las pruebas laboratoriales (hemograma, bioquímica con iones, panel de coagulación) y la ecografía abdominal, no mostraron alteraciones reseñables.
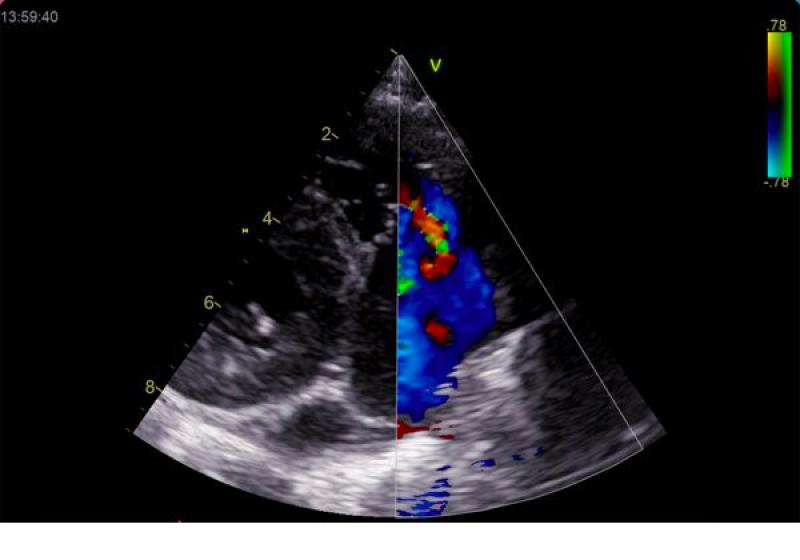
En la ecocardiografía (Figura 1), en el corte paraesternal derecho eje corto, se observó una leve hipertrofia concéntrica ventricular derecha, con válvulas auriculoventriculares derecha e izquierda correctamente ancladas. En corte paraesternal eje corto sobre los músculos papilares se apreció una membrana con leve anclaje muscular en el ventrículo derecho, ocasionando una separación de la cavidad ventricular en dos cámaras y por tanto compatible con un ventrículo derecho doble cámara. El estudio mediante el uso del Doppler color pone de manifiesto un paso de alta velocidad a través de dicho orificio, además de observarse una insuficiencia aórtica y otra en arteria pulmonar.
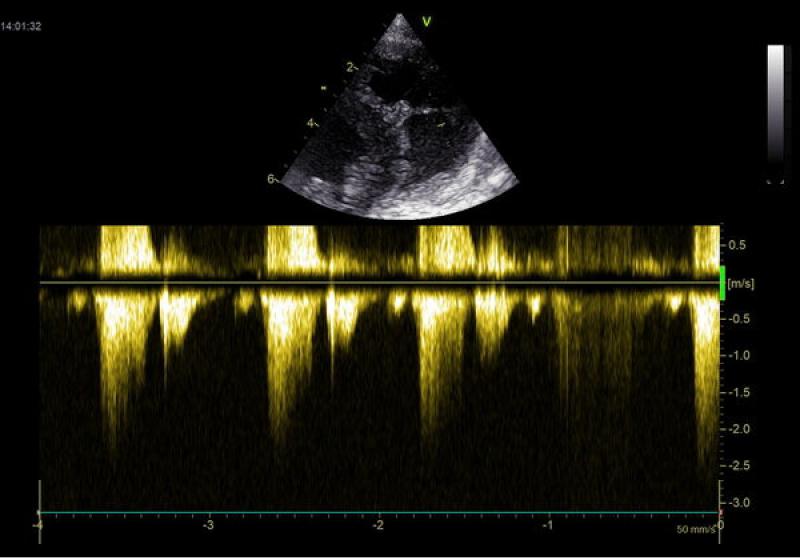
El estudio de Doppler continuo denota una velocidad aumentada en el paso transmembranoso en el ventrículo derecho, siendo esta velocidad de más de 5m/seg (determinando un gradiente de presión de 100 mm/Hg), la valoración de esta velocidad está complicada por la posición anatómica del defecto siendo en todos los cortes imposible una correcta alineación con el haz de ultrasonidos. La insuficiencia pulmonar es de baja velocidad insuficiencia aórtica con flujo transaórtico de 2.1 m/seg (gradiente de presión en 17 mm/Hg) (Figura 2).
Tras estos hallazgos se confirma la existencia de un ventrículo derecho doble cámara y se plantea intervención quirúrgica de valvuloplastia ventricular con técnica de balón simple.
Resolución quirúrguca
Para el abordaje quirúrgico se instaura un protocolo anestésico con metadona (0.3 mg/kg/SC) y dexmedetomidina (0.05 mg/kg/IV) para premedicación; diazepam (0.5 mg/kg/IVL) y propofol (0.2 ml/kg/IVL) para inducción anestésica y fentanilo (0.1 ml/kg/IV) y atropina (0.01 ml/kg/IV) intraoperatorios si hiciese falta. El mantenimiento durante la cirugía se realiza con isofluorano 1.5 %.
Se lleva a cabo un abordaje por yugular derecha mediante la técnica de Seldinger (percutáneo vascular 10 French (Fr)) pasando a arteria pulmonar, ventrículo y atrio derechos mediante catéter de Barenstein (4 Fr) y guía hidrofílica de 0.035 mm. Posteriormente, se lleva a cabo la toma de presiones en arteria pulmonar, ventrículo derecho de alta presión y atrio derecho, siendo imposible la toma de presión de ventrículo derecho baja presión (subpulmonar) por el pequeño espacio que este presentaba, por lo que se opta por realizar la diferencia de gradiente de presión entre VD alta presión versus arteria pulmonar (Tabla 1).
| Tabla 1. Presiones intraoperatorias, antes y después de la valvuloplastia. |
| Presiones | Pre | Post |
| Ventrículo derecho | 68 mmHg | 40 mmHg |
| Arteria Pulmonar | 14 mmHg | 14 mmHg |
Posteriormente, se realiza angiografía selectiva en tracto de salida ventricular derecho, para roap-map de posición y ecografía transesofágica (TEE) como apoyo de imagen durante todo el procedimiento endovascular. Por ecografía TEE se observa la membrana y se valora correctamente la cavidad posterior y anterior a arteria pulmonar, sin embargo, como se comenta no es posible posicionar un catéter de presión en la misma para toma de presiones (Figura 3).
Tras lo anterior, se introduce la guía hasta arteria pulmonar derecha, y se realiza el intercambio catéter Barestein – catéter balón. Se selecciona un catéter de balón de 20 mm (ratio de dilatación 1.3) a 2.5 atmósferas de presión y se posiciona en región de obstrucción, realizando dilataciones efectivas y produciendo la rotura de la membrana, previa angiografía y ecografía transesofágica para posicionar el defecto y visualización de la intervención. Tras las dilaciones efectivas en la toma de presión poscirugía se observa en ecografía TEE la presencia de la membrana fibrosa libre en ventrículo derecho, tras la rotura de la misma producida por las dilataciones (Figura 4).
Tras la realización de la cirugía se procede al cierre de la herida en piel con pegamento tisular y compresión, permitiendo que la yugular derecha quede completamente permeable para posteriores intervenciones de ser necesario. Pasa a hospitalización para monitorización de constantes y despertar, con posterior alta en 24 horas.
El tratamiento ambulatorio aplicado posintervención es:
- Amoxicilina-clavulánico 500 mg: ¾ comprimido por la mañana y ¾ comprimido por la noche, durante 10 días (hasta revisión).
- Cimalgex® 300 mg: 1 comprimido al día, durante 10 días.
- Omeprazol 20 mg: 1 comprimido al día en ayunas, durante 20 días.
La primera revisión del paciente se realiza en 10 días con realización de ecocardiografía, electrocardiograma y valoración de la herida quirúrgica. Posteriormente se realizarán revisiones en un mes para ecocardiografía de control y en 3 meses para ecocardiografía y medición de gradientes de presión. En estas revisiones se observa una disminución de la velocidad a través del defecto, teniendo en la última revisión una velocidad de 2.5 m/seg (Figura 5).
Discusión
El ventrículo derecho de doble cámara es una enfermedad cardíaca congénita, reportada primero en seres humanos (año 1858) y luego en perros5,6 sobre todo de razas grandes. Cabe destacar que se trata de una enfermedad con aproximadamente 40-50 casos notificados en la literatura3. Hasta la fecha, tras la recopilación de varios estudios se ha llegado a la conclusión de que existe una predisposición racial y diferencias entre los distintos géneros, teniendo en cuenta las razas Golden Retriever, Bóxer y Carlinos, con una mayor incidencia en machos7. Nuestro paciente en concreto, en la historia, no hay sospecha de ser descendiente de pacientes con patología cardiaca congénita, pero como bien hemos comentado anteriormente, se trata de un perro de raza Bóxer y es macho, por lo que es coincidente con la literatura revisada.
Se trata de una patología en la que la formación de una membrana fibromuscular divide el ventrículo en dos cámaras, una proximal de elevada presión y otra distal de baja presión6,8,9, defecto que impide el correcto paso del flujo sanguíneo a través del ventrículo, este puede ocasionar a medio-corto plazo una insuficiencia cardiaca congestiva, esta es dependiente del nivel de obstrucción y coexistencia o no de una comunicación interventricular (similar al ventrículo derecho doble cámara). Ya que esta patología se asocia a otras enfermedades congénitas4,7,8 y como hemos visto en la descripción del caso, nuestro paciente presenta asociada una estenosis aórtica en el límite patológico, esta será revisada posteriormente, si bien no existe descripción de coexistencias de ambas patologías en las referencias bibliográficas.
La sospecha de enfermedad en nuestro caso se estableció por la auscultación de un soplo sistólico de eyección en la base derecha, cercano al esternón, que directamente el compañero refirió al servicio de cardiología para la realización de ecocardiografía. Cabe destacar la importancia de la detección de soplo y valoración de esto en los pacientes que presenten soplo de alta intensidad, tengan la edad que tengan. Todos los datos citados en este artículo, así como los nombrados en los diferentes estudios, confirman que para el diagnóstico final se requiere, aparte de los signos clínicos, ecocardiografía y/o angiografía, que mostrarán una hipertrofia ventricular derecha con flujo turbulento en el tracto de salida6,7,10.
Además, el DCRV se caracteriza por presentar gradientes de presión superiores a 20 mmHg (gradiente normal 25/0-5 mmHg), en nuestro paciente este gradiente también estaba severamente aumentado, siendo de 40 mmHg. Si bien al no poder accederse por angiografía a la cámara posterior a la obstrucción, se optó por determinar el gradiente de presión pre-obstrucción versus arteria pulmonar.
En cuanto a la intervención quirúrgica de la patología, se realizó valvuloplastia y dilatación con balón. Se trata de una técnica de la que no existen muchas referencias bibliográficas en perros, por poseer un mayor coste y dificultad técnica, ya que hasta el momento se realiza en pocos hospitales a nivel europeo, aunque si hay referencias en humana que indican un éxito notable. Sin embargo, se prevé un mayor uso en animales, puesto que se trata de un método menos agresivo e invasivo y hasta el momento, se han realizado estudios con tasas de supervivencia mayores a 30 días poscirugía en un 71 % de casos en perros y un 67 % en gatos3.
Una de las técnicas utilizadas es valvuloplastia con balón de corte (cutting ballon) donde el balón presenta unas cuchillas de corte que están diseñadas para plegarse y desplegarse, de manera que las hojas afiladas se encuentren dentro de los pliegues del globo, para evitar daños a estructuras anatómicas durante la intervención, pero se despliegan cuando se hincha a niveles de trabajo lo que permite cortar las estructuras que producen la estenosis. En nuestro paciente se eligió un balón sin este tipo de cuchillas porque ecográficamente se observaba una leve porción muscular y una más evidente porción membranosa, lo que nos lleva a pensar que con una dilatación amplia podríamos tener buenos resultados, evitando de esta forma el uso de “Cutting ballon” cirugía intratorácica3. Se obtuvo muy buen resultado, puesto que, como hemos nombrado con anterioridad, se consiguió una reducción de las presiones del 34 %, siendo de un 40 % el límite deseado en las estenosis pulmonares y que usamos como referencia en este caso, debido a la ausencia de datos suficientes para considerar que éxito debíamos esperar de una técnica con balón simple.
En general, el pronóstico es bueno, con un índice de recidiva muy bajo tras la resección quirúrgica de los fascículos musculares causantes de la obstrucción.
Videos
| Figura 2. |
| Figura 3. |
| Figura 4. |
Bibliografía
- https://www.portalveterinaria.com/actualidad-veterinaria/actualidad/22118/estudio-epidemiologico-y-morfologico-del-ventriculo-derecho-con-doble-camara-en-perros.html
- http://www.vetbook.org/wiki/dog/index.php/Double-chambered_right_ventricle
- Schober KE, Rhinehart J et al. Cutting balloon and high-pressure balloon dilation for palliative treatment of congenital double-chambered right ventricle and primary infundibular stenosis in a Golden retriever dog. Journal of Veterinary Cardiology 2017. https://doi.org/10.1016/j.jvc.2017.10.001
- López-Alvarez J, Dukes-McEwan J et al. Balloon dilation of an imperforate cor triatriatum dexter in a Golden Retriever with concurrent double-chambered right ventricle and subsequent evaluation by cardiac magnetic resonance imaging. Journal of Veterinary Cardiology. 13, 211-218, 2011.
- Fukushima R, Tanaka R et al. Epidemiological and Morphological Studies of Double-Chambered Right Ventricle in Dogs. J. Vet. Med. Sci. 73(10): 1287–1293, 2011.
- Alva, C., Ho, S. Y., Lincoln, C. R., Rigby, M. L., Wright, A. and Anderson, R. A. The nature of the obstructive muscular bundles in double-chambered right ventricle. J. Thorac. Cardiovasc. Surg. 117: 1180–1189. 1999
- L. Mann Douglas, O. Bonow Robert, P. Zipes Douglas, Braunwald Eugene, Libby Peter. Barcelona, España. Editorial Elsevier Saunders. 2016. Págs. 1441-1442.
- Scurtu L, Tabaran F et al. Combined double chambered right ventricle, tricuspid valve dysplasia, ventricular septal defect, and subaortic stenosis in a dog. Scurtu et al. BMC Veterinary Research. 13:367, 2017
- Tanaka R, Shimizu M et al. Surgical management of a double-chambered right ventricle and chylothorax in a Labrador retriever. Journal of Small Animal Practice. 47, 405–408, 2006.
- Martin JM, Orton C et al. Surgical correction of double-chambered right ventricle in dogs. Scientific Reports: Descriptive Report JAVMA, Vol 220, No. 6, March 15, 2002.
 by Multimédica
by Multimédica