Esplenectomía laparoscópica en pequeños animales
Resumen breve
Actualmente la esplenectomía en pequeños animales, descrita en medicina veterinaria tanto en la especie canina como en la felina, se realiza con mayor frecuencia a través de una celiotomía a nivel de línea media, aunque durante los últimos años se ha demostrado la viabilidad de su manejo quirúrgico mediante cualquiera de las distintas alternativas laparoscópicas que se describen en este artículo. Las principales indicaciones para…Índice de contenidos
Resumen
Actualmente la esplenectomía en pequeños animales, descrita en medicina veterinaria tanto en la especie canina como en la felina, se realiza con mayor frecuencia a través de una celiotomía a nivel de línea media, aunque durante los últimos años se ha demostrado la viabilidad de su manejo quirúrgico mediante cualquiera de las distintas alternativas laparoscópicas que se describen en este artículo. Las principales indicaciones para la realización de una esplenectomía total en pequeños animales incluyen cuadros neoplásicos que afecten al bazo, la torsión del pedículo esplénico, esplenomegalias como resultado de enfermedad infiltrativa y/o enfermedad inmunomediada refractaria al manejo médico.
Introducción
El desarrollo de las técnicas laparoscópicas se ha convertido en un enfoque alternativo a la cirugía convencional dentro de las distintas opciones terapéuticas que actualmente están disponibles para su empleo en pequeños animales.
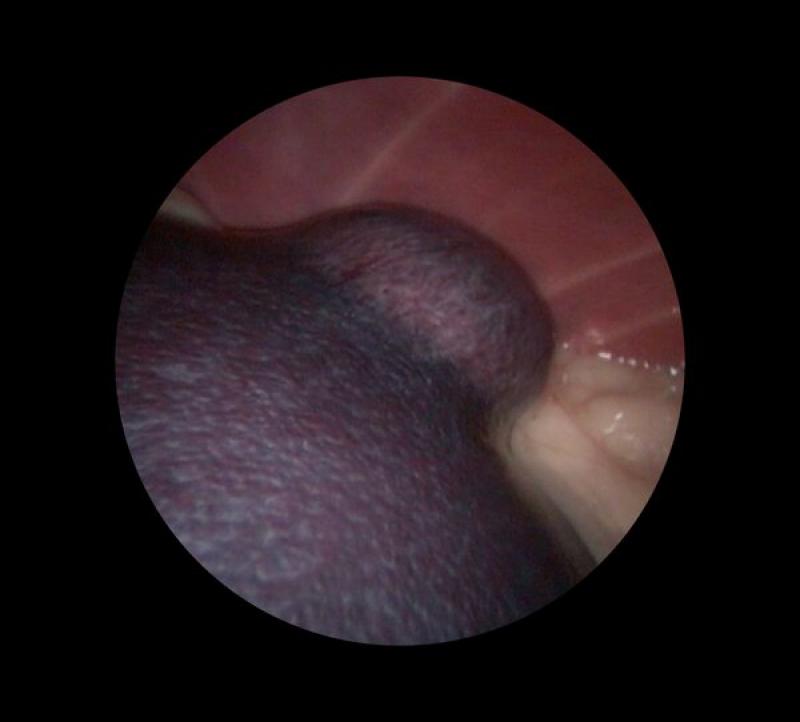
La esplenectomía en pequeños animales es un procedimiento relativamente habitual en el manejo, principalmente, de alteraciones oncológicas que afectan al bazo (Figura 1). Por el contrario, en humanos, las enfermedades hematológicas mediadas por el sistema inmunitario, que no responden al tratamiento médico, así como la anemia hemolítica son las principales indicaciones para la realización de una esplenectomía.
Aun así, y aunque los abscesos esplénicos se consideran infrecuentes en pequeños animales, éstos también son una indicación para la realización de una esplenectomía en pequeños animales, ya que generalmente son secundarios a bacteriemia asociada a sepsis, cuerpos extraños migratorios, torsión esplénica o a enfermedades infecciosas como la toxoplasmosis y la hepatitis infecciosa canina.
Otra circunstancia que se considera una posible indicación para la esplenectomía en pequeños animales es la torsión esplénica, que consiste en la rotación del bazo sobre su pedículo vascular, colapsando la vena esplénica, provocando esplenomegalia congestiva y posteriormente isquemia y necrosis del parénquima.
La torsión esplénica puede ser espontánea o asociada a un síndrome de dilatación-vólvulo gástrico, siendo ésta la presentación más frecuente de la patología en la especie canina.
Aunque la esplenectomía mediante técnica convencional realizada a través de una celiotomía es un procedimiento bien tolerado para el manejo de una gran variedad de patologías esplénicas, el auge en el desarrollo e implementación de las técnicas mínimamente invasivas en la medicina de pequeños animales ha permitido el desarrollo de distintos abordajes laparoscópicos para su realización.
La primera descripción de una esplenectomía laparoscópica que se realizó en un paciente humano se publicó en 1991 y actualmente se considera la terapia estándar de atención para la mayoría de las formas de patologías esplénicas, y solo la coagulopatía no corregida y la hipertensión portal severa se consideran contraindicaciones para su realización en humanos, aunque también se describe a la esplenomegalia masiva como una contraindicación relativa en algunos estudios.
Varios estudios han evaluado los resultados de la esplenectomía mediante celiotomía frente a los de la esplenectomía laparoscópica y se ha demostrado cómo se asocia con una menor morbilidad y estancias hospitalarias más cortas cuando se realiza mediante laparoscopia.
Por otro lado, en los últimos años ha habido un interés creciente respecto a la cirugía de puerto único en humanos, como una modalidad para mejorar la estética y los resultados en los pacientes.
La esplenectomía laparoscópica de puerto único se ha descrito en humanos, aunque en un número relativamente pequeño de casos, pero con resultados generalmente alentadores. Por su parte, en cuanto a pequeños animales, hasta la fecha tampoco se ha reportado su empleo en un número significativo de gatos o perros con patología esplénica, aunque sí se ha demostrado que se trata de una técnica, junto al resto de variantes laparoscópicas descritas, factible en la especie canina.
Selección y preparación del paciente
Como en toda cirugía, es fundamental realizar previamente un estudio prequirúrgico completo, que debe incluir hemograma completo, perfil bioquímico, urianálisis y coagulograma. Esto permitirá identificar el estado real del paciente, así como descartar cualquier alteración que pueda requerir una estabilización previa del mismo, como p. ej. anemia severa, coagulopatías, alteraciones hemodinámicas y/o estados sépticos.
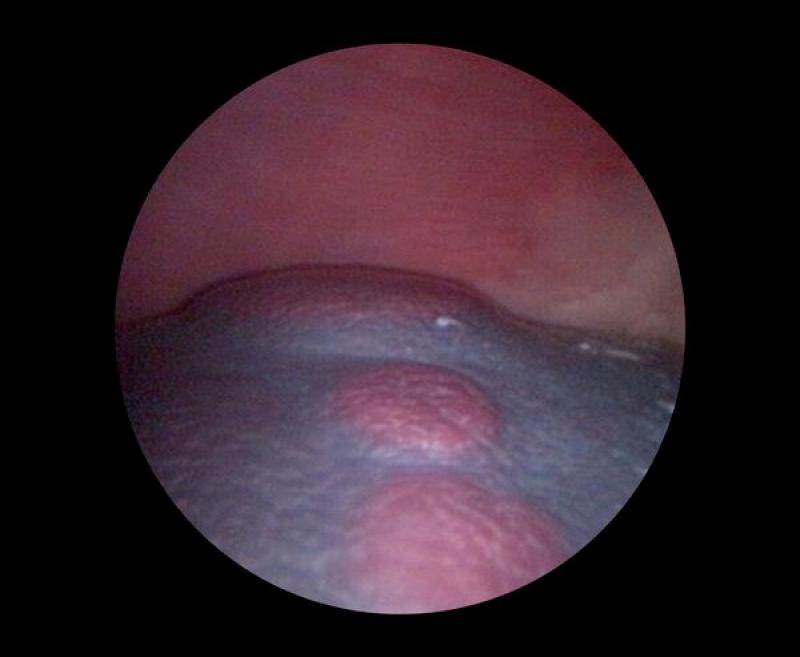
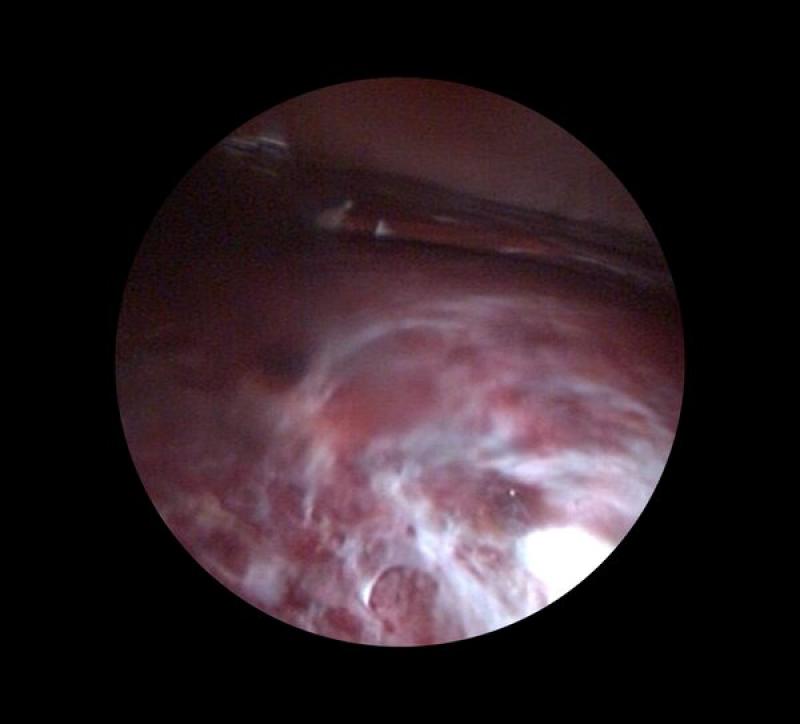
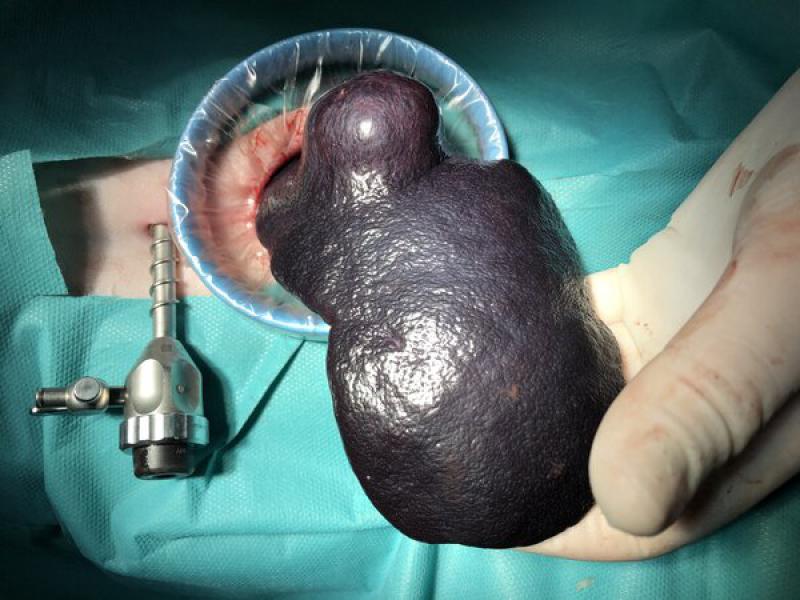
Además, en aquellos casos en los que exista evidencia de hemoperitoneo, aunque sea leve, será necesario tener disponibles unidades de sangre compatibles, ya que es probable que se pueda producir sangrado espontáneo de la masa durante el procedimiento, o incluso la laceración esplénica durante su manejo laparoscópico (Figura 2).
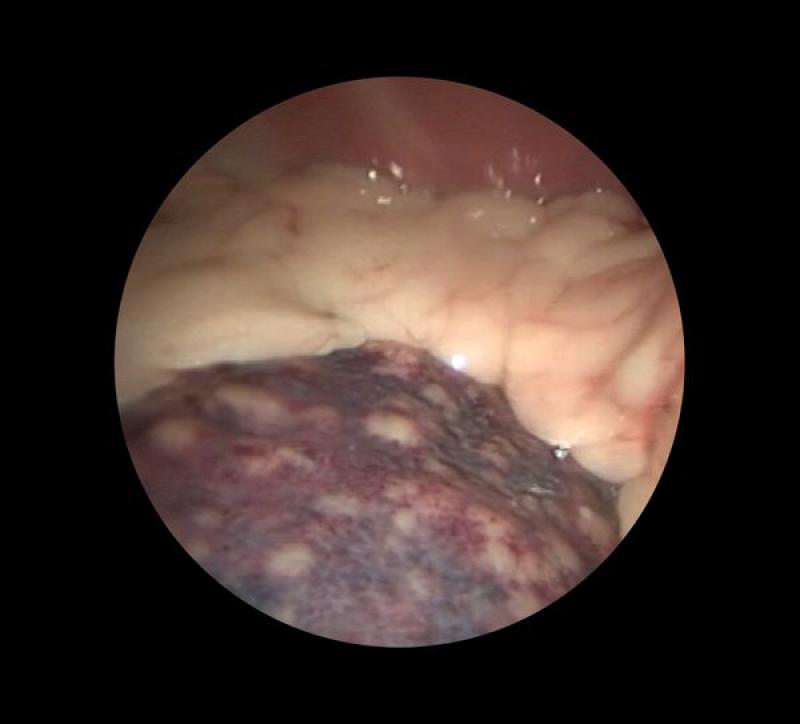
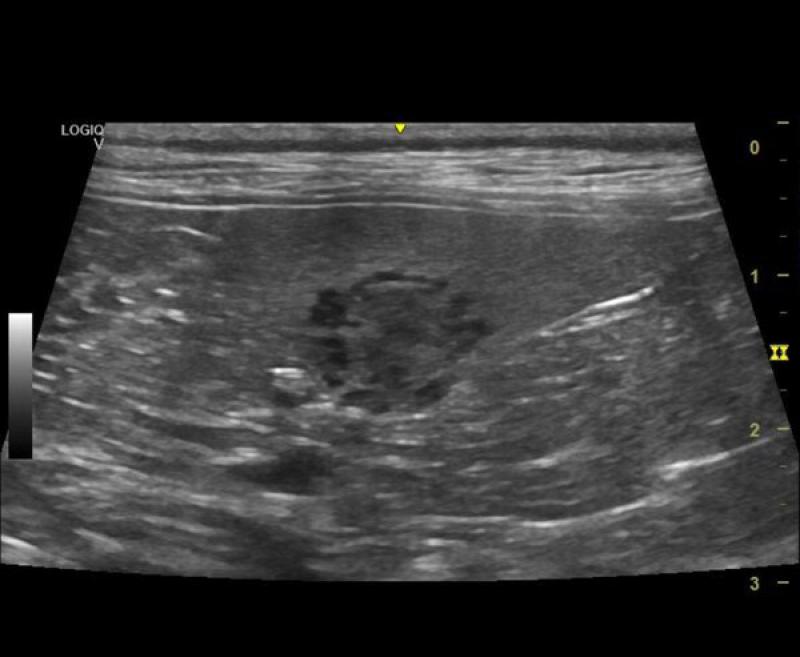
Los estudios de imagen, especialmente la ecografía abdominal, son fundamentales a la hora de prescribir la realización de una esplenectomía mediante cualquiera de las técnicas mínimamente invasiva (Figura 3).
Esto se debe a que han de ser consideradas distintas variables que pueden condicionar la realización de un acceso laparoscópico a la hora de llevar a cabo el procedimiento quirúrgico. Entre dichas variables a tener en cuenta destacan la existencia de líquido libre, el cual podría tratarse de hemoperitoneo, así como la forma y tamaño tanto del bazo, como de la masa en caso de que ésta sea el motivo de la cirugía.
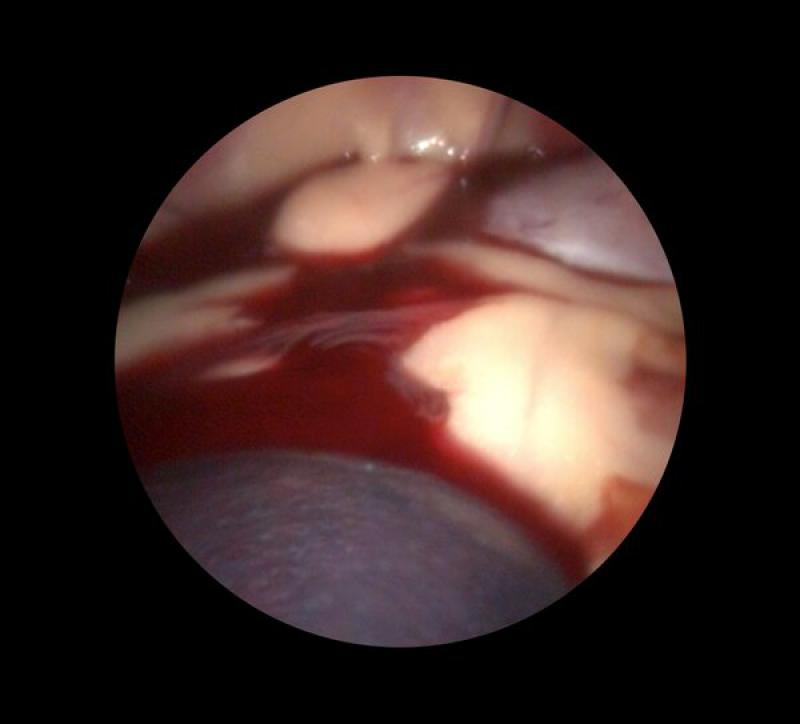
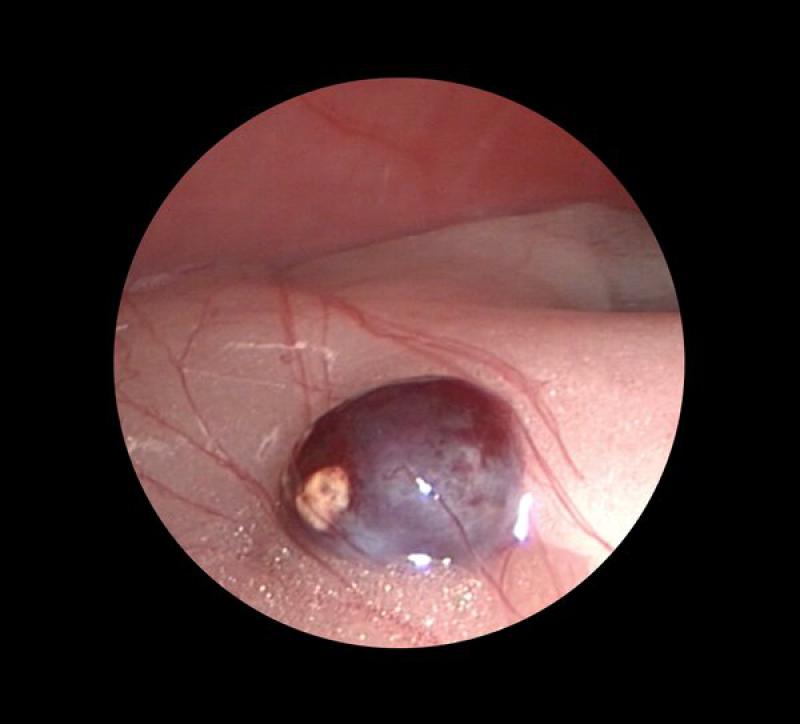
Se ha descrito que bazos muy grandes, mayores a 25 cm en su eje longitudinal, o masas de más de 5 cm podrían ser criterios relativos de exclusión a la hora de la realización de una esplenectomía laparoscópica. Lamentablemente, en ocasiones los hallazgos en las imágenes ecográficas difícilmente pueden diferenciarse de hematomas y otras afecciones no tumorales e incluso no patológicos, como la hiperplasia linfoide nodular (Figura 4).
Es por ello que, estimar si una masa esplénica corresponde o no a una neoplasia maligna es difícil debido a la heterogenicidad de tamaño y estructura que presentan los hematomas y otras masas benignas como la hiperplasia regenerativa hepática o la mencionada la hiperplasia linfoide nodular.
En el caso de sospechar de una neoplasia maligna, es fundamental realizar un trabajo diagnóstico previo, con el fin de establecer el estadio del cuadro oncológico, ya que la presencia de metástasis es un criterio de exclusión quirúrgico, siempre que no existan signos de sangrado activo a nivel abdominal asociados al bazo.
Para la búsqueda de potenciales lesiones metastásicas se recomiendan el empleo de técnicas de diagnóstico por imagen tradicionales como estudios radiográficos de tórax, ecocardiografía o la propia ecografía abdominal. Aunque evidentemente, la única forma de diagnosticar el origen y el grado patológico de un tumor maligno es el estudio histopatológico.
Debido a las limitaciones mencionadas del estudio ecográfico del abdomen, que aun así es una técnica imprescindible en el manejo diagnóstico de pacientes con enfermedades neoplásicas del bazo, en ocasiones puede ser recomendable la realización de un estudio TAC abdominal. Esto se debe a su mayor potencial diagnóstico a la hora de estimar el tamaño esplénico y el volumen de la/s masa/s, al igual que las relaciones de ésta/s con otros órganos.
Además, las imágenes contrastadas permiten valorar si la irrigación orgánica puede ser compatible con angiogénesis y aumentar el índice de sospecha de que la lesión sea o no de origen neoplásico.
En los casos en los que se valore la realización de una esplenectomía laparoscópica en casos de torsión esplénica espontánea, es importante tener en cuenta el llevar a cabo un seguimiento exahustivo del paciente, ya que se han descrito casos de trombosis de vasos esplénicos, émbolos sistémicos e incluso CID en el postquirúrgico.
La preparación quirúrgica para la esplenectomía, mediante cualquiera de las variantes laparoscópicas que se describirán a continuación, no guarda grandes diferencias respecto a la esplenectomía convencional mediante celiotomía. Sí se recomienda un estricto ayuno del paciente, ya que un incremento del volumen del paquete intestinal puede llegar a restar campo quirúrgico y dificultar la cirugía al tratar de movilizar el bazo. Como en toda cirugía laparoscópica, se procederá a realizar una completa tricotomía del abdomen, desde la apóxisis xifoides hasta el pubis, preparado asépticamente el campo quirúrgico.
Técnica quirúrgica
Desde un punto de vista mínimamente invasivo, la esplenectomía en pequeños animales se puede llevar a cabo mediante laparoscopia multipuerto, mediante laparoscopia por puerto único, así como por técnica laparoasistida, recomendándose el empleo de una óptica de 30º, cuyo diámetro (5 ó 10 mm) dependerá tanto de la talla del paciente, como de las preferencias del cirujano.
Evidentemente, es necesario contar con instrumentos laparoscópicos clásicos, como un sistema de aspiración y succión, pinza Maryland, porta agujas, así como un sellador vascular (p. ej., sistemas bipolares avanzados).
Este último equipo es fundamental a la hora de llevar a cabo una esplenectomía laparoscópica ya que, especialmente en procesos neoplásicos como el hemangiosarcoma esplénico, suele ser marcada la angiogénesis que se visualiza con la presencia de vasos tortuosos de gran calibre y que, normalmente, son la fuente de irrigación principal del tumor, lo que hace que el empleo de selladores vasculares sean la tecnología a tener en cuenta, ya que permite el sellado de vasos de calibre considerable (5-7 mm).
Independientemente de la técnica empleada, la configuración del quirófano requiere el disponer la mesa quirúrgica transversalmente a la torre de laparoscópica. Además se recomienda que tanto el equipo de anestesia como el anestesista se ubiquen cranealmente al paciente, mientras que la mesa de instrumental en el borde caudal del mismo, con el objetivo de que el el monitor de la torre quede enfrentando directamente a los cirujanos y lograr así respetar la ergonomía durante todo el procedimiento.
Esplenectomia laparoscópicamente asistida
Ofrece los beneficios de una técnica mínimamente invasiva como lo son una herida mas pequeña, magnificación durante la exploración y una mejor iluminación, además de haberse demostrado que no esta asociada a complicaciones posquirúrgicas mayores.
Para su realización, se debe de llevar a cabo una laparoscopia exploratoria situando los trócares craneal y caudalmente a la cicatriz umbilical, aunque es igualmente válido el empleo de puerto único o multipuertos.
Como en toda laparoscopia, inicialmente se debe de llevar a cabo una inspección minuciosa de todos los órganos abdominales en busca de anormalidades que puedan o no estar asociadas a la condición patológica del bazo (Figura 5).
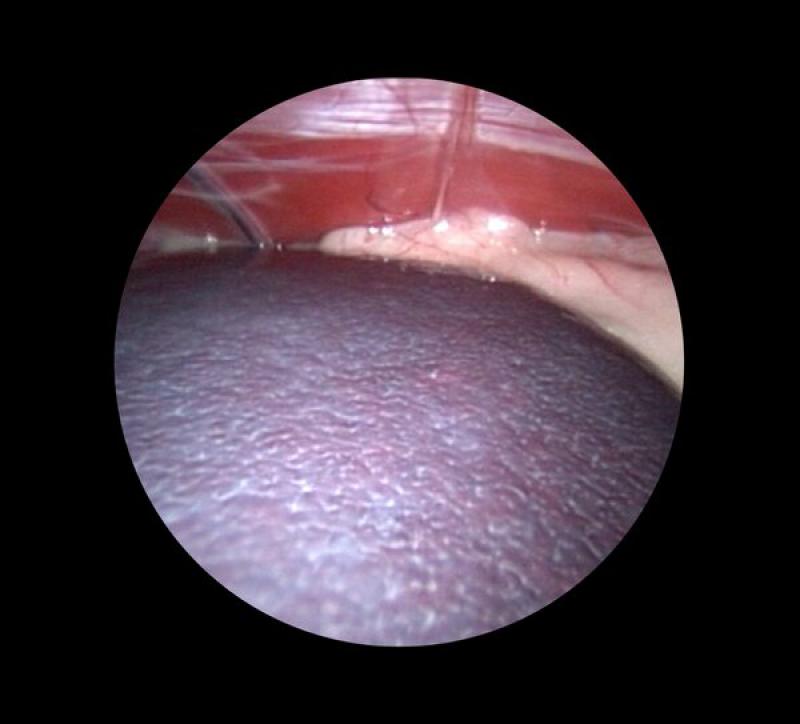
Es en este momento donde se puede optar por realizar una minilaparotomía de 5 a 7 cm, extrayendo el bazo a nivel caudal y cauterizando progresivamente los vasos esplénicos hasta su completa extirpación, o por el contrario realizar una esplenectomía laparoscópica pura sólo de forma parcial, en la que sólo se sellan y seccionan las arterias gástricas cortas, con el fin de que el bazo quede mucho más móvil y la extracción por minilaparotomía sea mucho más fácil.
Una vez exteriorizado el bazo, independientemente del procedimiento seleccionado por el cirujano, se completa la cirugía sellando las arterias y venas del hilio esplénico de manera extracorpórea usando un sellador vascular o simplemente empleando una técnica de ligadura hemostática convencional.
La única desventaja de la técnica laparoscópicamente asistida frente a las técnicas laparoscópicas puras, es que durante la extracción el bazo, éste sigue vascularizado y por lo tanto una lesión durante el proceso de exposición del mismo puede conllevar el desarrollo de una hemorragia.
Esplenectomia laparoscópicamente multipuerto
Es la técnica quirúrgica más comúnmente descrita. Para ello, se posiciona al paciente en decúbito dorsal para la creación del neumoperitoneo y, una vez instaurado este e implantado el resto de trócares.
El primer trócar, para la cámara, se puede introducir tras la creación del neumoperitoneo mediante cualquiera de las maniobras descritas de acceso laparoscópico. Este puerto se instala inmediatamente caudal a la cicatriz umbilical, siendo recomendable este sitio para evitar el ligamento falcifome, el cual puede dificultar la visualización al movilizar la cámara.
El resto de puertos de trabajo deben implantarse en la misma línea media, caudal y craneal al puerto de cámara, separados 5-10 cm, en función de la talla del paciente, para garantizar una correcta triangulación.
Una vez implantados todos los puertos de trabajo, se reposiciona al paciente en decúbito lateral derecho para obtener un buen acceso al extremo craneal del bazo donde se localizan las arterias gástricas cortas y en donde el órgano es menos móvil.
El bazo debe manipularse para exponer los vasos hiliares con separador romo o en abanico. Cuando se utiliza un separador romo, el bazo siempre debe manipularse con el cuerpo del instrumento en lugar de la punta, ya que ésta que puede penetrar fácilmente la cápsula esplénica delgada, generando una iatrogenia responsable de un grado variable de hemorragia. Aun así esta maniobra debe de llevarse a cabo ya que su objetivo es elevar el bazo para exponer su hilio y arterias y venas esplénicas.
Una vez que se identifican los vasos hiliares, se realiza el control y sección vascular con la fuente de energía de elección por el cirujano, generalmente comenzando desde la porción caudal móvil del bazo y trabajando sistemáticamente hacia la porción más craneal (Figura 6).
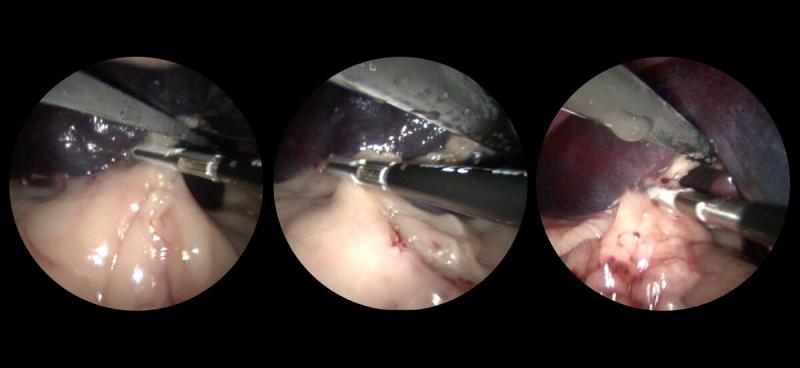
Esta estrategia puede ser modificada en el caso de que existencia un tumor con grandes vasos, ya que éste debe ser el primer objetivo a la hora de lograr el sellado vascular y control de la hemostasia. Una vez aislado el bazo, no es posible de extraer por la incisión de un puerto por lo que se deben extender una de éstas, uniéndose generalmente las incisiones media y caudal para extraer el órgano.
Es ideal el empleo de bolsas de extracción (p. ej., EndoBag® o un sistema similar) para extraer el bazo, especialmente si se sospecha de neoplasias y/o abscesos, ya que el riesgo de diseminación y siembra de celulas neoplasicas es alta al igual que una peritonitis séptica por ruptura del absceso.
El problema es que las bolsas de recuperación de un tamaño suficiente para recuperar el bazo completo son difíciles de conseguir. la extracción de la pieza puede resultar un desafío ya que, evidentemente, un bazo tumorado embolsado en una bolsa de extracción laparoscópica.
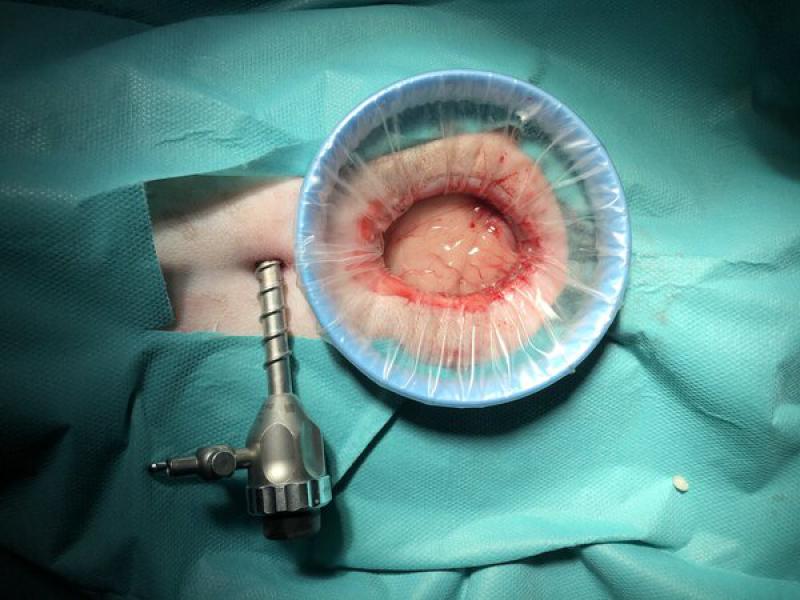
Ya que muchas veces no es posible contar con bolsas de las características necesarias para bazos de gran tamaño, puede optarse por la implantación de un retractor tisular que permita extraer la pieza con delicadeza, siempre haciendo coincidir su eje menor con el eje de la incisión (Figura 7).
Se ha descrito que el empleo de este tipo de retractores tisulares, además de aislar las distintas capas de la pared abdominal, también permite que el bazo pase más fácilmente a través de la pared abdominal, evitando la rotura de la cápsula esplénica durante la maniobra de extracción del órgano (Figura 8).
Esplenectomia laparoscópicamente por puerto único
Es una alternativa a la técnica anterior, con el objetivo de disminuir aún más la invasividad del procedimiento quirúrgico, por lo que está ganando cada vez más popularidad.La posición del paciente para esta técnica es igual que la anterior, aunque puede beneficiarse de aplicar una maniobra de trendelenburg no forzada.
El puerto único, es implantado en la zona de la cicatriz umbilical a través de una incisión de alrededor de 2,5 cm según el dispositivo empleado, teniendo en cuenta que existen varias versiones comerciales de puerto único. El procedimiento a nivel intrabdominal es prácticamente similar a la técnica multipuerto.
Debido a que las inserciones de los instrumentos son muy próximas, la triangulación en ocasiones es más complicada y habitualmente es normal cómo la imagen durante la laparoscopia se caracteriza en que el instrumental entra en paralelo en el campo quirúrgico, lo que probablemente predisponga al choque entre el instrumental de forma ocasional.
Esta situación puede subsanarse mediante el empleo de instrumental roticulado y/u ópticas anguladas. Una vez realizado el sellado y sección vascular de todo el pedículo esplénico, la extracción del bazo se llevará a cabo mediante cualquiera de las alternativas descritas en el procedicimiento anterior.
Control postquirúrgico
Se decribe el empleo de antibioterapia de cobertura durante los siguientes 6-8 días (p. ej., cefalosporinas), así como cobertura analgésica mediante el empleo de opiáceos agonistas μ cada 4 horas durante aproximadamente las primeras 12 horas postoperatorias. Posteriormente, y en el caso de que el estado del paciente lo permita, se puede proceder al alta ambulatoria del paciente, garantizando una cobertura anfiinflamatoria y analgésica mediante la administración de un AINE duante 7 días.
En aquellos casos en los que la analgesia pueda resultar escasa, se puede prescribir como analgésico de rescate la administracion de tramadol o bruprenorfina vía oral cada 12 horas durante 3-4 días.
Uno de los principales riesgos del procedimiento es la hemorragia por incompetencia hemostática, por lo que se recomienda realizar ecoFAST cada 4 horas durante el primer día del posquirúrgico, al igual que la medición de los niveles de hemoglobina a las 5 horas de haber finalizado el procedimiento. Si el paciente tiene signos de hipovolemia compatibles con hemorragia, se debe considerar la reintervención del paciente lo antes posible.
Además, cuando exista un diagnóstico histopatológico positivo de neoplasia, se debe realizar un seguimiento por imagen en búsqueda de metástasis por siembra quirúrgica o micrometástasis prequirúrgica que eventualmente se hayan podido desarrollar, especialmente en aquellos casos en los que haya existido sangrado de una masa esplénica antes o durante el procedimiento quirúrgico.
La estrategia más común es realizar estudios ecográficos abdominales y radiografías torácicas, aunque alternativamente se puede considerar la realización de estudios TAC especialmente en pacientes sospechosos o con neoplasias de alto grado patológico en la histopatología.
Las pruebas de imagen deben incluir una exploración minuciosa de los puntos de introducción de los trócares laparoscópicos, ya que es posible causar siembra iatrogénica en dichos puntos si no se ha empleado un retractor tisular o una bolsa de extracción durante la exteriorización del bazo.
Complicaciones
La hemorragia intraquirúrgica se ha descrito como la complicación más frecuente en la esplenectomía laparoscópica en pequeños animales, a diferencia de la esplenectomía abierta en donde se sabe que la complicación más común es la hemorragia postquirúrgica siendo además la razón más frecuente de muerte posquirúrgica inmediata en perros sometidos a esplenectomía por alteraciones no neoplásicas.
Probablemente la causa de ello es que en el abordaje abierto se suele utilizar hemostasia tradicional con ligaduras lo que aumenta la probabilidad de fallos por dehiscencia de la sutura, mientras que en el abordaje laparoscópico sólo se recomienda el empleo de sistemas de sellado vascular avanzado lo que podría explicar esta diferencia.
Dichas hemorragias durante la esplenectomía laparoscópica pueden suceder durante la creación del neumoperitoneo, ya sea por la implantación del primer trocar mediante técnica de Hasson modificada o por el empleo de la aguja de Veress, aunque también se ha descrito por manipulación excesiva del omento mayor así como por perforación del parénquima esplénico durante su suspensión por manejo poco delicado.
En el caso de que esta hemorragia sea masiva, es motivo suficiente para tener que reconvertir a cirugía abierta. Otras complicaciones postquirúrgicas descritas en la esplenectomía abierta son la isquemia del lóbulo izquierdo del páncreas por compromiso de las arterias derivadas de la arteria esplénica, especialmente frecuente en torsiones del pedículo esplénico, así como el desarrollo de arritmias cardiacas, parámetros hematológicos alterados y anomalías morfológicas, o el aumento del riesgo de infecciones bacterianas y hemoparasitarias, anemia no regenerativa y sepsis.
Aunque en la mayoría de los casos la ruptura capsular esplénica iatrogénica durante el procedimiento quirúrgico no suele tener consecuencias desde un punto de vista hemodinámico, puede hacer que la conversión a cirugía abierta sea más probable si la visualización se ve afectada y conlleva el riesgo de siembra neoplásica en casos en los que se trate de una neoplasia maligna (p. ej., hemangiosarcoma esplénico).
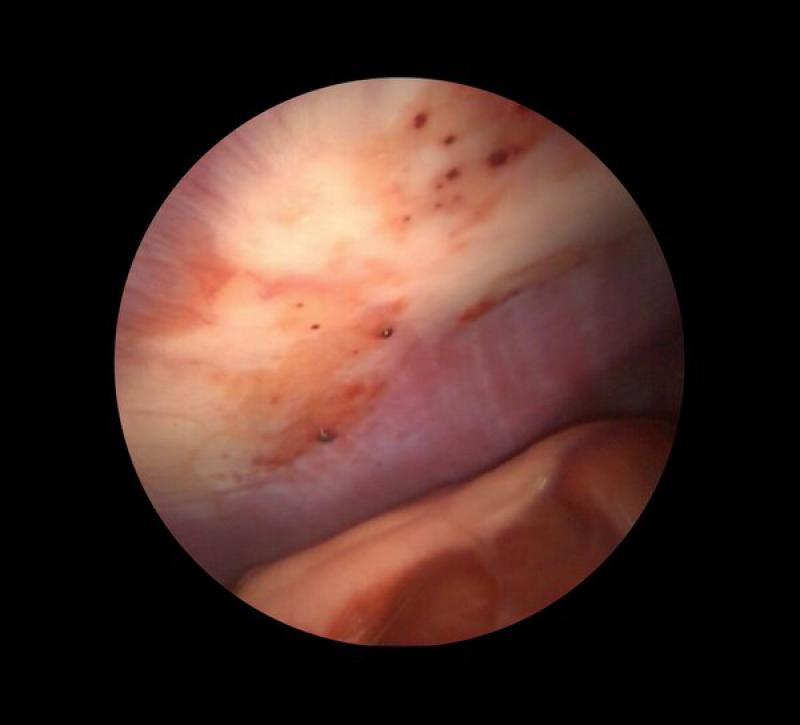
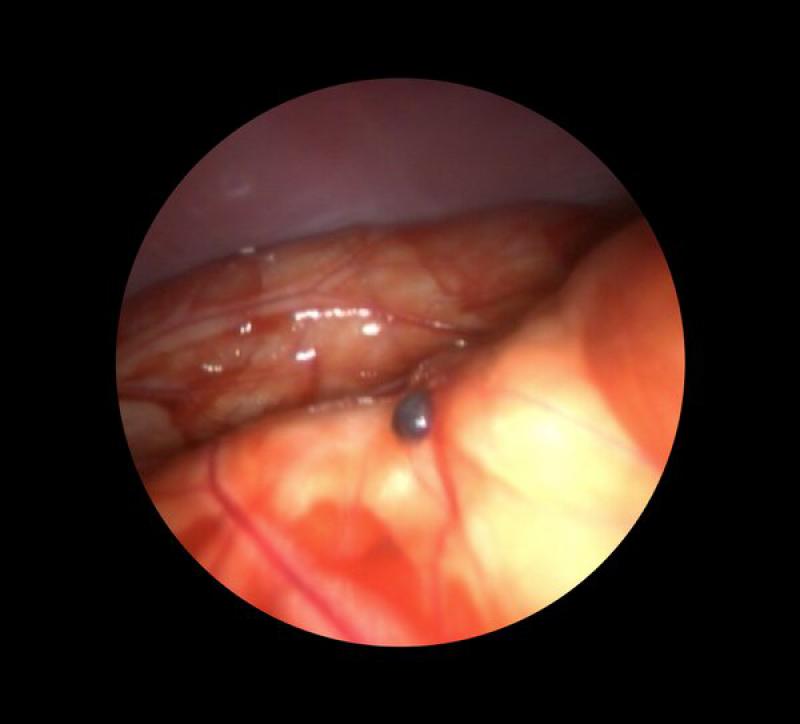
La esplenosis y la siembra neoplásica en la incisión a través de la cuál se extrae el órgano son sucesos bien definidos en humanos. La esplenosis se define como el autotrasplante heterotópico de tejido esplénico como resultado de una rotura del bazo por trauma o cirugía, teniendo un componente benigno y generalmente se trata de un hallazgo casual (Figura 9). Por su parte, la siembra neoplásica es considerada una metástasis por implante (Figura 10).
Conclusiones
La esplenectomía laparoscópica, es actualmente la técnica de elección para el tratamiento de los trastornos hematológicos del bazo en humanos, ya que tiene distintas ventajas en comparación con un acceso mediante celiotomía, incluyendo una recuperación más rápida, tasas de morbilidad más bajas, traumatismo quirúrgico reducido y dolor postoperatorio, hospitalización más corta y un retorno más rápido a la actividad diaria normal.
Aun así, y al igual que con todos los procedimientos laparoscópicos, es fundamental una correcta selección del caso para lograr un buen resultado quirúrgico. Así, un bazo o una masa de gran tamaño, así como la existencia de hemoabdomen se postulan como las principales contraindicaciones para la prescripción de un manejo laparoscópico para la realización de una esplenectomía laparoscópica, ya que potencialmente son susceptibles de requerir reconversión a cirugía abierta por un sangrado incontrolado o por un escaso campo quirúrgico.
Bibliografia
- Collard F, Nadeau ME, Carmel EN. Laparoscopic splenectomy for treatment of splenic hemangiosarcoma in a dog. Veterinary Surgery. 2010; 39, 870-872.
- Feldman LS, Demyttenaere SV, Polyhronopoulos GN. Rening the selection criteria for laparoscopic versus open splenectomy for splenomegaly. Journal of Laparoendoscopic and Advanced Surgical Techniques. 2008; 18:13‐19.
- Khalaj A, Bakhtiari J, Niasari-Naslaji A. Comparison between single and three portal laparoscopic splenectomy in dogs. BMC Veterinary Research. 2012; 8:161.
- Lillo-Araya F, Lobato-Cereceda C. Esplenectomía laparoscópica. En: Casas García DL, Santana González AJ (eds.) Técnicas de Mínima Invasión en Pequeños Animales. Multimédica Ediciones Veterinarias. (2018). 419-425.
- Mayhew PD, Sutton JS, Singh A, Runge JJ, Case JB, Griffin MA, Giuffrida MA. (2018). Complications and short‐term outcomes associated with single‐port laparoscopic splenectomy in dogs. Veterinary Surgery, 2018;47(S1):O67-O74
- O’Donnell E, Mayhew P, Culp W. Laparoscopic splenectomy: operative technique and outcome in three cats. Journal of Feline Medicine & Surgery. 2013; 15:48–52.
- Rivier P, Monnet E. Use of a vessel sealant device for splenectomy in dogs. Veterinary Surgery, 2011; 40:102-105.
- Shaver SL, Mayhew PD, Steffey MA. Short-term outcome of multiple port laparoscopic splenectomy in 10 dogs. Veterinary Surgery, 2015; 44(1):71–75.
- Shaver SL, Mayhew PD. Laparoscopic splenectomy. En: Fransson B, Mayhew PD (eds.) Small Animal Laparoscopy and Thoracoscopy. Wiley Blackwell. (2015) 134-140.
- Stedile R, Beck CA, Schiochet F. Laparoscopic versus open splenectomy in dogs. Pesquisa Veterinária Brasileira, 2009; 29:653–660.
- Tavakoli A, Khalaj A, Ghasempoor S. Minimally invasive total splenectomy in dogs: a clinical report. Iranian Journal of Veterinary Medicine, 2011; 5(1):9-12.
- Winslow ER, Brunt LM. Perioperative outcomes of laparoscopic versus open splenectomy: a meta-analysis with an emphasis on complications. Surgery. 2002; 134:647‐655.
- Wrigth T, Singh A, Mayhew PD, Runge JJ, Brisson BA, Oblak ML, Case JB. Laparoscopic-assisted splenectomy in dogs: 18 cases (2012–2014). Journal of the American Veterinary Medical Association, 2016; 248:916-922.
 by Multimédica
by Multimédica