Usos quirúrgicos de las endoprótesis
Resumen breve
Los stents o endoprótesis son dispositivos que se utilizan para el tratamiento de algunas patologías que conllevan estenosis, obstrucción, perforación, fístula, etc., de algún conducto del perro. Este conducto puede estar localizado en el aparato digestivo, urinario, circulatorio y respiratorio. Estos conductos, son estructuras huecas que deben de quedar distendidas, conservando su luz mediante el dispositivo y de esta manera permitir el paso de sustancias a través de dicho conducto.Índice de contenidos

Introducción
Los stents o endoprótesis son dispositivos que se utilizan para el tratamiento de algunas patologías que conllevan estenosis, obstrucción, perforación, fístula, etc., de algún conducto del perro. Este conducto puede estar localizado en el aparato digestivo, urinario, circulatorio y respiratorio. Estos conductos, son estructuras huecas que deben de quedar distendidas, conservando su luz mediante el dispositivo y de esta manera permitir el paso de sustancias a través de dicho conducto.
Los stents comenzaron a comercializarse en los años noventa. Eran instrumentos muy rudimentarios que fallaban en un 20 % de los casos. En la actualidad, los stents se fabrican con mejores materiales, con recubrimientos que son más compatibles y con liberación de fármacos que intentan reducir la inflamación secundaria al stent. El resultado de los nuevos stents es mejor con un índice de rechazos menor al 2 % gracias a la incorporación en la fabricación de polímeros biodegradables como vehículo de fármacos e incluso stents biodegradables.
Los stents están en continua evolución, aunque no existe un modelo ideal que no presente efectos indeseables.
Tipos de stent
SEM o Stents metálicos autoexpandible
Suelen ser de una aleación de titanio y níquel (nitinol) o de acero inoxidable. Han sido los stents más utilizados en veterinaria. En ocasiones estos stents se recubren de fármacos antiproliferativos. Algunas complicaciones que pueden sufrir estas endoprótesis son la migración y oclusión, estenosis, fístulas, granulomas, reflujo, sangrado, etc. Los stent de acero inoxidable se asocian a numerosas complicaciones derivadas de su colocación, formación de granulomas, acortamiento del stent, etc.
Stent de plástico autoexpandible
Inicialmente se fabricaban de plástico rígido de polivinilo, aunque en la actualidad se usa silicona de calidad médica. Estos stents tienen algunas limitaciones en cuanto a sus características y forma. Los stents de plástico pueden presentar menos complicaciones que los SEMs, aunque suelen ser más gruesos ya que tienen menos fuerza radial, disminuyendo la fricción con el conducto, aumentando la tasa de migración.
Stent biodegradable
Se usan poco en veterinaria. Estas endoprótesis se disuelven tras su instalación sin necesidad de ser extraídas en un segundo procedimiento. Su principal complicación es su mayor riesgo de migración.
Stent liberador de fármacos
También conocidos como DES, del inglés Drug-eluting stent. Son nuevos tipos de stent que liberan quimioterápicos buscando la reducción tumoral y de la granulación asociada al roce y contacto del stent, sobre todo en el caso de los SEMs.
USOS QUIRÚRGICOS DE LOS STENTS
Los stents tienen cuatro usos principales, patologías respiratorias, patologías urinarias, patologías digestivas y patologías cardiovasculares.
Este artículo se centrará en los stents utilizados en el aparato respiratorio.
El principal problema hallado en las vías respiratorias es la estenosis o colapso de una vía aérea.
USOS EN EL APARATO RESPIRATORIO
La laringe es un órgano cartilaginoso-muscular compuesto por los cartílagos cricoides, tiroides, aritenoides y epiglotis. Los nervios encargados de la abducción de estos cartílagos son el laríngeo recurrente y el vago, excepto para el músculo cricotiroideo que depende del nervio laríngeo caudal.
Funciones de la laringe
- Regular la entrada de aire
- Para vocalizar
- Para impedir la inhalación de alimento
- Aumentar la presión abdominal/torácica cuando se cierra
Las condiciones más frecuentes que afectan a la laringe son la parálisis, masas, inflamación, trauma, estenosis y colapso. Todas ellas pueden dar lugar a alteraciones en la entrada y salida del flujo de aire o en la vocalización. Los signos clínicos incluyen la presencia de ruidos respiratorios (estertor-estridor), disfagia, vómitos y tos, en casos agudos de laringitis.
Para localizar el problema en la laringe se deberá realizar una buena anamnesis y exploración física.
La laringoscopia es la técnica diagnóstica más adecuada ya que permitirá realizar una evaluación anatómica y funcional completas.
Los signos clínicos de las patologías que afectan a la laringe suelen ser de presentación progresiva, pero a veces generan distrés respiratorio.
La mayoría de las patologías que afectan a la laringe generarán una alteración del diámetro de la glotis con reducción del flujo de aire y silbidos respiratorios o cambios en el ladrido (Tabla 1).
| Signos clínicos habituales de las enfermedades que afectan a la laringe |
|---|
|
Tabla 1. Signos clínicos habituales de las enfermedades que afectan a la laringe.
El colapso laríngeo es una complicación grave como resultado de una obstrucción crónica de las vías respiratorias superiores. El colapso laríngeo puede ser clasificado atendiendo a su localización como supraglótico, glótico o subglótico.
El colapso laríngeo se trata del resultado de una presión negativa prolongada asociada al síndrome obstructivo respiratorio de los animales braquicéfalos (BAOS).
En estos pacientes que desarrollan el colapso laríngeo podría haber una predisposición a una malacia de los cartílagos. Es frecuente que el colapso laríngeo pase desapercibido al cirujano que realiza una corrección quirúrgica de un paciente con BAOS. En la bibliografía también se halla el colapso laríngeo en perros de raza miniatura con historial de alergias crónico.
Para realizar un diagnóstico de colapso laríngeo, la laringoscopia vuelve a ser de gran ayuda. Los
Puntos claves
• Insuficiente abducción de los cartílagos aritenoides de la laringe durante la inspiración, que conduce a obstrucción de las vías respiratorias altas
• Lo más habitual es que se trate de una enfermedad contraída causada por una neuropatía subyacente
• La neuropatía (cuando la hay) también puede causar otros signos clínicos, como debilidad de extremidades posteriores o disfagia
procesos cuneiformes de los cartílagos aritenoides tenderán a introducirse hacia la glotis con las estructuras del pliegue aritenoepiglótico. Incluso la epiglotis y los procesos corniculados podrán ser aspirados dentro de la glotis, apareciendo en la exploración débiles y edematosos.
La cirugía puede ayudar a mejorar la condición de un paciente con colapso laríngeo, pero requerirá tratamiento médico a largo plazo. Se estima que la fase de recuperación tras un evento quirúrgico puede estar entre 6-12 meses debido al deterioro del resto de estructuras no intervenidas.
Las traqueostomías temporales y las permanentes han sido usadas para tratar esta condición, pero suelen dar problemas de mantenimiento con formación de tapones de moco en animales de tráqueas pequeñas.
En el control conservativo del colapso laríngeo se recomienda:
- Control del peso del paciente. La mentalidad del dueño no suele ayudar dada la idea que suelen tener sobre el aspecto normal de un perro braquicéfalo, como el bulldog inglés. Este exceso de peso hace que el paciente sea reacio al ejercicio por lo que necesitará un cambio en su estilo de vida. Las capas de grasa del animal aíslan su temperatura por lo que los mecanismos de la termorregulación fallarán.
- El aire acondicionado puede ayudar a controlar el jadeo del animal. El propio jadeo incrementa el flujo de aire y finalmente inflama la mucosa nasal y laríngea.
- Se recomienda la preoxigenación del paciente durante 5 minutos previos a la inducción de la anestesia.
- El uso de esteroides puede estar indicado (como la prednisolona: 7-15 mg/kg) para minimizar la inflamación y edema postoperatorios.
- La furosemida puede ser de interés en la prevención o tratamiento del edema laríngeo.
- No utilizar máscaras de inducción ya que el paciente puede colapsarse.
- Extubación y recuperación lentas que eviten la excitación del paciente, ya que esto podría llevar a inflamación laríngea.
- Tener cuidado con las sedaciones ya que pueden inducir a la oclusión de las vías respiratorias.
- Se recomienda el diazepam para permitir la recuperación lenta durante varias horas. Esto conllevará un mejor control de las primeras horas críticas en las que puede aparecer un edema laríngeo.
- Monitorizar al paciente durante al menos 24 horas post cirugía.
El colapso laríngeo es tratable pero el propietario debe ser consciente de la naturaleza degenerativa de este proceso, del alto riesgo de los procedimientos y de las posibles largas estancias del paciente durante la recuperación.
Las técnicas para solucionar el colapso laríngeo serán las mismas que se realizarán en el caso de una parálisis laríngea (Tabla 2).
| Puntos claves del tratamiento del colapso laríngeo |
|---|
|
Tabla 2. Puntos claves del tratamiento del colapso laríngeo.
Las neoplasias faríngeas son infrecuentes tanto en el perro como en el gato. Los pacientes suelen ser viejos o de mediana edad, aunque también pueden ser diagnosticadas en pacientes jóvenes. Los rabdomiomas y los carcinomas son los tumores más frecuentes en perros, mientras que en gatos se tratan de tumoraciones mayormente malignas y suelen ser linfomas y carcinomas de células escamosas (Tabla 3).
| Signos clínicos producidos por las neoplasias laríngeas |
|---|
|
Tabla 3. Signos clínicos producidos por las neoplasias laríngeas.
Diagnóstico
Pueden tratarse de masas palpables o quizás se precise de una inspección directa de la laringe mediante un endoscopio.
La ecografía puede usarse en la inspección y toma de muestra de las posibles masas.
Las citologías por aspiración de aguja fina no son muy fiables pudiendo inducir diagnósticos erróneos de inflamación. En la mayoría de los casos será necesaria una biopsia para llegar a un diagnóstico definitivo. Los pacientes que sufran biopsias de la laringe deberían ser considerados de riesgo durante la recuperación de la anestesia.
En los gatos se recomienda aspiración de los ganglios submandibulares, radiografías torácicas, TAC, resonancia magnética, ecografía abdominal y test del virus de la leucemia felina.
Utilidad del stent de silicona en los colapsos laríngeos
Dentro de las emergencias vitales está la obstrucción mecánica o funcional de la laringe, cuyo tratamiento de emergencia clásico es la realización de una traqueostomía temporal, permitiendo que el aire ingrese en la tráquea mediante un acceso alternativo a la vía natural, mediante la colocación de un traqueotubo durante un corto periodo de tiempo. Sin embargo, requiere de cuidados intensivos postoperatorios para evitar la descolocación u obstrucción del tubo además de conllevar complicaciones como son la obstrucción aguda del tubo, infecciones o lesiones del nervio laríngeo recurrente.
Dentro de las emergencias vitales también está la opción de utilizar stents de silicona tubular que actuarán como dilatadores laríngeos, manteniendo la apertura fisiológica de la rima glottidis, mediante su fijación con puntos a los cartílagos laríngeos, para evitar su desplazamiento.
La traqueostomía temporal es un recurso adecuado ante una emergencia en pacientes disneicos por obstrucción de vías aéreas altas. Entre sus ventajas se incluye, la resolución inmediata de los signos clínicos al permitir el paso del aire a través de la laringe y facilitar que la zona afectada por la inflamación pueda resolverse con tratamiento médico en los días posteriores. Sin embargo, este procedimiento requiere de un manejo hospitalario intensivo y específico, ya que se puede obstruir con las secreciones traqueales o desarrollar infecciones de la tráquea en la zona del estoma.
Los stents laríngeos de silicona tienen forma tubular y mantienen la apertura fisiológica de la rima glottidis, pudiéndose fijar con puntos. El principal inconveniente que se observa en los pacientes es el coste del stent así como la sensibilidad de la mucosa laríngea a la presencia de una estructura extraña en este área. Por otro lado, se trata de una técnica sencilla, mínimamente invasiva y rápida con pocas complicaciones. Los pacientes suelen requerir hospitalización pero con un manejo sencillo. Por ello, la colocación de un stent de silicona podría ser una alternativa efectiva y menos agresiva que la traqueostomía temporal en el caso de un edema laríngeo de origen traumático (Figura 1).
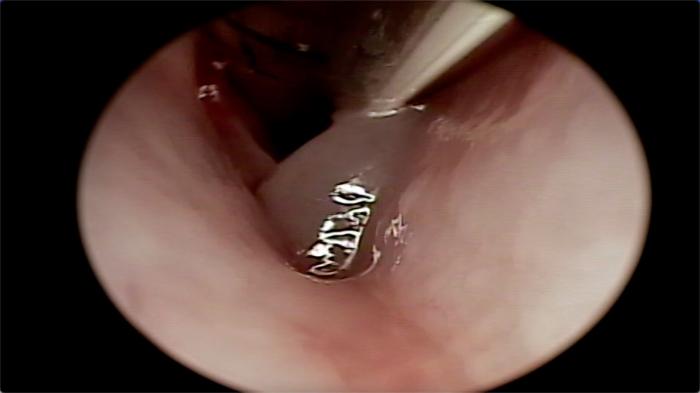
FIGURA 1. Edema de sáculo laríngeo en cachorro con edema agudo de glotis.
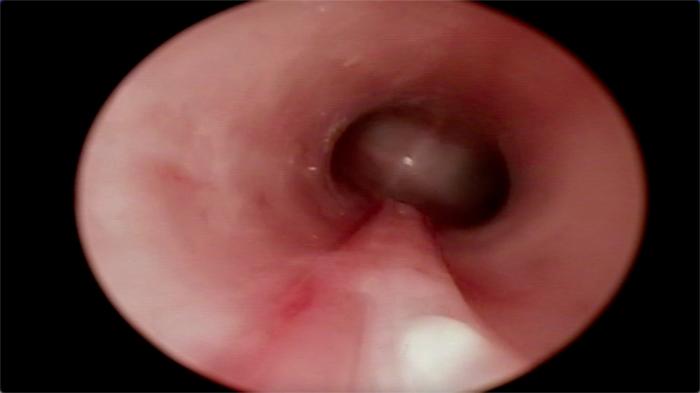
FIGURA 2. Mismo cachorro con mucosa de la tráquea intensamente inflamada.
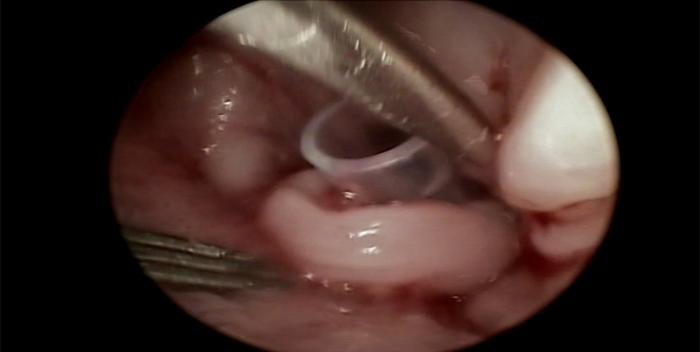
FIGURA 3A-B. Colocación de un stent de silicona en un cachorro con edema de glotis traumático.
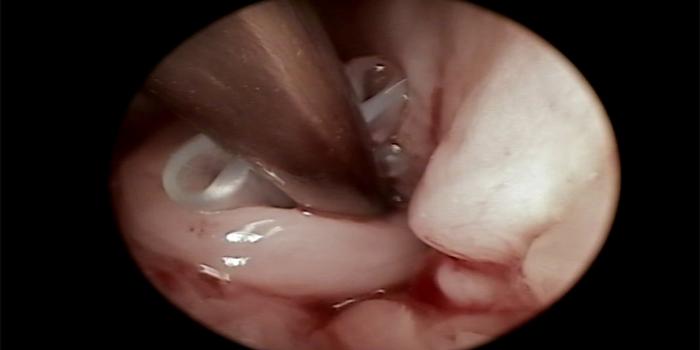
FIGURA 3A-B. Colocación de un stent de silicona en un cachorro con edema de glotis traumático.
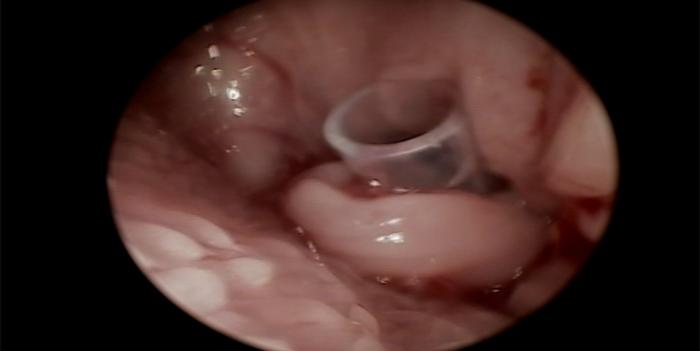
FIGURA 4. Stent laríngeo de silicona ya instalado en la glotis.
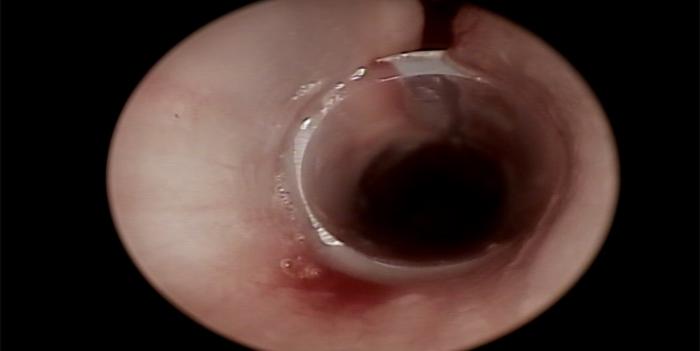
FIGURA 5. Vista frontal del stent de silicona ya colocado.
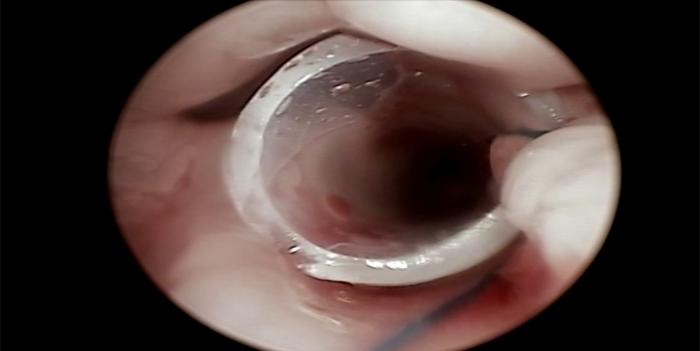
FIGURA 6. Stent de silicona fijado por un punto a la larínge.
Parálisi laríngea (PL)
Es una alteración de la inervación de los músculos intrínsecos de la laringe que evita la correcta abducción de los cartílagos ariteoniodes y de los pliegues vocales. En animales normales la contracción de ambos cricoaritenoides dorsales en la respiración forzada abduce los cartílagos y los pliegues vocales, ensanchando la glotis y minimizando la resistencia al flujo de aire.
Existen dos tipos:
Congénita
- Normalmente en animales de corta edad (<1 año)
- Bouvier des Flandres (rasgo autosómico dominante), Pastor Alemán blanco, Husky, Bull Terrier Inglés, Rottweiler
- Infrecuente
Adquirida
- Perros normalmente mayores de 10 años de razas medianas o gigantes
- Labrador, Collie, Golden Retriever, Setter Irlandés, Weimaraner
- Puede producirse en gatos, secundarias a neoplasias del nervio vago e intoxicación por plomo y se asocia con una enfermedad neuromuscular progresiva.
- La PL contraída en perros es la presentación más frecuente, como consecuencia de alteraciones en la inervación del músculo laríngeo recurrente debida a cuerpos extraños en esófago, incubaciones endotraqueales, neuropatías periféricas y centrales, traumatismos quirúrgicos y masas en cuello o mediastino craneal. La evolución suele ser una obstrucción lenta y progresiva de las vías respiratorias altas (probablemente a lo largo de varios años), avanzando desde una paresia a parálisis total.
- Puede producirse un recrudecimiento agudo, por ejemplo, durante el exceso de ejercicio en un día caluroso, presentando dichos animales cuadros de hipertermia asociados. Muchos animales con parálisis laríngea se presentan con un colapso dinámico que obstruye la glotis debido al incremento en el esfuerzo del diafragma y de los músculos intercostales para mantener una menor presión intrapleural y mantener el flujo de aire. Como consecuencia de este proceso se producirá una intolerancia al ejercicio muy manifiesta.
- Los hallazgos de la historia incluyen reducción de la tolerancia al ejercicio, respiración ruidosa (principalmente inspiratoria) y, en ocasiones, cambios en la voz. Algunos animales tienen una historia de náuseas y regurgitaciones como consecuencia de una presión intrapleural baja que conduzca a una hernia hiatal. Una tos persistente u ocasional puede darse en este tipo de pacientes debido a pequeñas aspiraciones, bien por una desensibilización de la laringe por la neuropatía subyacente o por un megaesófago (Tabla 4).
| ¿Cuándo hay que operar una parálisis laríngea? |
|---|
|
Tabla 4. ¿Cuándo hay que operar una parálisis laríngea?
Sintomatología
Los signos clínicos que alertan al propietario y que motivan la consulta son principalmente: ruidos respiratorios (estridor), intolerancia al esfuerzo, cambios más o menos importantes de la voz cuando el perro ladra pudiendo llegar a la afonía, tos que sobre todo se manifiesta en el momento de beber o comer y fatiga generalizada.
En los casos severos se puede presentar una cianosis importante como consecuencia de una marcada insuficiencia respiratoria, pudiendo llegar a producirse cuadros de síncope-colapso.
Estos síntomas observados por el propietario, suelen ser los más importantes en el momento de la consulta. Si los síntomas son discretos, un test de esfuerzo de unos minutos puede realizarse para acentuar los signos respiratorios. Un examen neurológico completo es indispensable para poder evaluar una miopatía o una neuropatía (normalmente mala propiocepción al realizar la prueba de percusión, saltos lentos, reducción del tiempo de respuesta en algún caso). La sospecha clínica es fundamental en el diagnóstico de esta afección (Tabla 5).
| Puntos clave en el diagnóstico de la paralisis laríngea |
|---|
|
Tabla 5. Puntos clave en el diagnóstico de la paralisis laríngea.
Diagnóstico
En animales jóvenes de razas braquicéfalas puede asociarse una parálisis laringe con la sintomatología típica de estas razas. En perros viejos las neoplasias y abscesos pueden provocar parálisis del nervio laríngeo recurrente que deben descartarse. Las neoplasias de faringe, tonsilas, laringe y tiroides pueden provocar signos clínicos compatibles con parálisis laríngea. Tampoco se debe confundir esta patología con el colapso traqueal, ya que esta es una enfermedad anatómica/estructural mientras que la PL es una enfermedad funcional.
El método estándar para el diagnóstico de la parálisis laríngea es la laringoscopia.
EL objetivo de la laringoscopia es descartar los siguientes diagnósticos diferenciales infrecuentes respecto a la obstrucción de las vías respiratorias altas:
- Neoplasia, por ejemplo, de amígdalas o laringe.
- Cuerpo extraño.
- Engrosamiento de la pared de la laringe, por ejemplo, por un mucocele salivar en la pared larínge o absceso para-auricular.
Tratamiento quirúrgico
El tratamiento quirúrgico es fundamental en la mayoría de los pacientes con BAOS debido a las dificultades respiratorias y al empeoramiento de su calidad de vida.
Numerosas técnicas quirúrgicas han sido descritas en medicina veterinaria para tratar la parálisis laríngea. Todas ellas tienen como objetivo agrandar la apertura glótica y así facilitar el paso del aire. Sin embargo, esta abertura debe ser suficiente pero no excesiva para limitar el riesgo de neumonía por aspiración. La lateralización unilateral del cartílago aritenoides (suturas a baja tensión), es actualmente la técnica de elección (Tabla 6).
| ¿Cuáles son los buenos candidatos a la cirugía? |
|---|
|
Tabla 6. ¿Cuáles son los buenos candidatos a la cirugía?
Ventrículo-cordectomía
Esta técnica consiste en retirar las cuerdas vocales del animal, ya sea por vía oral o a través de la laringe (abordaje externo ventral), y así agrandar la apertura glótica. Para evitar un efecto de cicatrización excesiva, se recomienda no retirar el primer cuarto ventral de las cuerdas vocales o sino realizar un abordaje por laringotomía ventral. La apertura glótica que se obtiene no suele ser suficiente y esta técnica tiene muchas e importantes complicaciones (edema laríngeo post-operatorio, fibrosis cicatricial, etc.). Además, en la mayoría de los casos requiere una traqueotomía temporal durante o después de la cirugía.
Laringectomía parcial
Es la asociación de una aritenoidectomía parcial y de una ventrículo-cordectomía. Esta técnica también presenta muchas complicaciones, en torno al 50 % de los casos (sangrado, edema, bronconeumonías por aspiración, necesidad de traqueotomía frecuente).
Fisura laríngea
Esta técnica, actualmente completamente abandonada y tiene como objetivo aumentar el diámetro del cartílago tiroides, realizando una plastia en escalera o “torre de castillo”, centralmente en él.
Lateralización del cartílago aritenoides o “Tie-back”
Se trata de la técnica de preferencia según los estudios realizados. El objetivo es, agrandar la apertura glótica retractando quirúrgicamente el cartílago aritenoides y restablecer su abducción permanente, y así crear una apertura glótica permanente, lo más fisiológica posible. Esta cirugía puede realizarse de uno o ambos lados. De manera general, suele realizarse unilateralmente (el izquierdo, mas fácil para el cirujano diestro), para limitar el riesgo de una apertura demasiado grande y un mayor riesgo de neumonía por aspiración. Después de haber disecado el cartílago aritenoides de sus ataduras, este mismo se retracta caudalmente con suturas o prótesis ancladas ya sea:
- A la porción caudo-dorsal del cartílago tiroides (laringoplastia o “Tie back” tiro-aritenoidea).
- A la parte dorso-caudal del cartílago cricoides (laringoplastia o “Tie back” crico-aritenoidea). Esta segunda es más fisiológica.
Una vez las suturas han sido cerradas, es imperativo que una tercera persona realice un control visual bucal de la apertura obtenida. Una apertura insuficiente necesita que las suturas sean cerradas de nuevo. Una apertura excesiva potencia el riesgo de una neumonía por aspiración, la sutura debe ser aflojada.
La técnica de elección según los diferentes estudios publicados y la experiencia personal del autor sigue siendo la lateralización unilateral crico-aritenoidea ya que está asociada al menor porcentaje de complicaciones y permite situar la sutura en el eje fisiológico del músculo crico-aritenoideo dorsal.
Traqueostomía permanente
Es una intervención de rescate que se aplica cuando todas las demás han fracasado. Es necesario asegurarse de que no hay ninguna otra causa para la insuficiencia observada, como la presencia de neumonía por aspiración.
Seguimiento y complicaciones
La laringe tiene una cierta propensión a producir granulomas. Los corticoesteroides reducirán el edema de la mucosa pero el tejido de granulación resulta difícil de prevenir, por ello se recomienda el cierre cuidadoso de cualquier cirugía practicada sin dejar zonas abiertas. Algunos agentes quimioterápicos como la mitomicina-C o el paclitaxel han demostrado ser útiles en la prevención de la formación de tejido cicatricial granular.
Especialmente en la cirugía de la parálisis laríngea, es muy importante tener en cuenta las complicaciones post-operatorias, ya que se dan en aproximadamente el 35 % de los casos, y cerca del 65 % de las mismas se darán en las primeras 2 semanas postoperatorias (Tabla 7).
| Las complicaciones habituales de las cirugías de la parálisis laríngea |
|---|
|
Tabla 7. Las complicaciones habituales de las cirugías de la parálisis laríngea.
Pronóstico
Aun teniendo un porcentaje elevado de complicaciones, el pronóstico a corto y medio plazo es favorable después del tratamiento quirúrgico. Según los estudios, cerca del 90 % de los propietarios nota una mejoría clínica y de la calidad de vida de su perro. Los factores determinados que predisponen a las complicaciones o a la muerte son: la edad avanzada del paciente, la realización de una traqueotomía y la presencia concomitante de una o varias de las anomalías siguientes: respiratoria, del esófago (megaesófago), neoplásica, una enfermedad del sistema nervioso subyacente (3 veces más probable que muera por una causa ligada a su parálisis laríngea). La parálisis laríngea es una entidad multifactorial. Por ello, el pronóstico dependerá de la cirugía seleccionada y de los factores de riesgo.
Los factores que predisponen a la muerte del animal incluirán la edad del animal, la realización de una traqueostomía temporal y del padecimiento de alteraciones espiratorias, esofágicas, tumorales o neurológicas.
La lateralización unilateral del aritenoides en perros se suele asociar a una mortalidad perioperatoria inferior al 15 %. Los signos clínicos suelen mejorar aunque puede haber persistencia de tos postoperatoria, especialmente al comer y beber. Se deberá informar al propietario ante la posible progresión de otros signos neurológicos por el cuerpo del animal produciendo debilidad y atrofia muscular.
El pronóstico en gatos dependerá de la naturaleza de la enfermedad laríngea y de la individual respuesta a la terapia. Las traqueostomías permanentes y las cirugías de lateralización suelen tener mal pronóstico.
Uso de stent de silicona en la parálisis laríngea
Los stents de silicona pueden utilizarse como una alternativa en el tratamiento de la parálisis laríngea del perro y del gato. Se trata de una técnica mínimamente invasiva, rápida, relativamente económica y fácil de colocar. Es una técnica que requiere poco tiempo anestésico lo cual la hace particularmente interesante como solución temporal a una parálisis laríngea.
La parálisis laríngea en perros suele observarse en animales de raza Retriever y otros de razas Spaniels, viejos de entorno a los 10-12 años. En muchas ocasiones se relaciona con hipotiroidismo pero que no mejora al suministrar hormona tiroidea.
La colocación de un stent traqueal es una técnica simple que no requiere un equipamiento muy especializado. Los stents pueden ser colocados y recolocados hasta que se consigue una localización adecuada. De la misma manera, pueden ser retirados si dan muchos problemas de tolerancia y, cuando ha estado un tiempo colocado puede aportar cierta consistencia al cartílago subyacente derivado de la fibrosis lesional. Muchos pacientes mejoran su estado tras retirar un stent que ha estado bastante tiempo posicionado. En nuestro caso, al menos 2 meses. Se pueden conseguir diferentes diámetros y longitudes para adaptar el stent que mejor encaje en la glotis del paciente afectado. Los stents no evitan el riesgo de neumonía por aspiración debido a la apertura permanente de la rima glottidis pero si muchos otros relacionados con la cirugía en sí.
La incidencia de complicaciones ha sido estudiada y es baja, con tolerancias de los implantes de más de 1 año y bien soportado en alrededor del 70 % de los pacientes. Los beneficios se observan de inmediato al desaparecer los signos clínicos de disnea y estridor.
Muchos perros suelen toser tras la implantación del stent pero no suele ser necesario administrar antitusivos. Una endoscopia de revisión de la posición del stent puede ser interesante para identificar un desplazamiento del stent.
Es frecuente que algunos pacientes desarrollen halitosis que suele ser debida a un acúmulo de secreciones entre la mucosa laríngea y el stent. Esta halitosis mejora tras la limpieza y desinfección de la prótesis. La clorhexidina suele dar buenos resultados para este fin.
En los stents de silicona no es frecuente observar granulomas como se han podido describir en otros tipos de stents como los metálicos.
Es importante encontrar el tamaño de la prótesis para evitar que una prótesis muy justa o grande produzca una compresión excesiva de la mucosa, lo que acentuaría los efectos indeseables como cuerpo extraño. Puede ocurrir lo contrario, que una prótesis pequeña haga una migración interna o una expulsión del stent. Los stents se suelen servir como kits de varios tamaños que permiten probar varias opciones durante la anestesia. Diversos tamaños de tubos endotraqueales pueden ser de ayuda para definir el tamaño más ajustado (Figura 2).
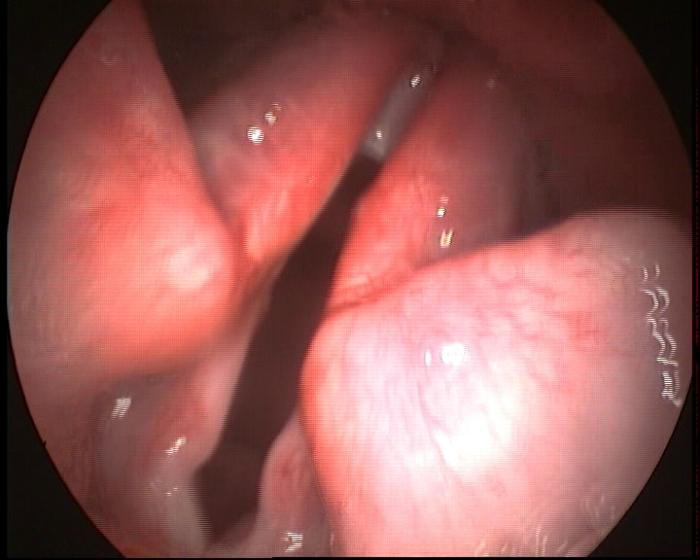
FIGURA 1. Glotis en espiración con salida forzada de aire por parálisis laríngea en un perro.
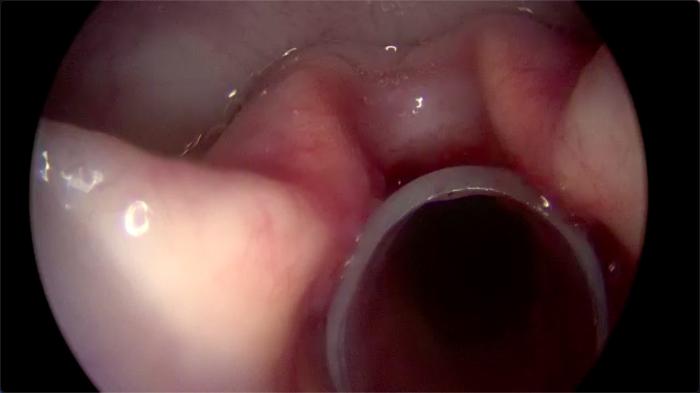
FIGURA 2. Stent de silicona translúcida colocado en glotis de perro con parálisis laríngea.
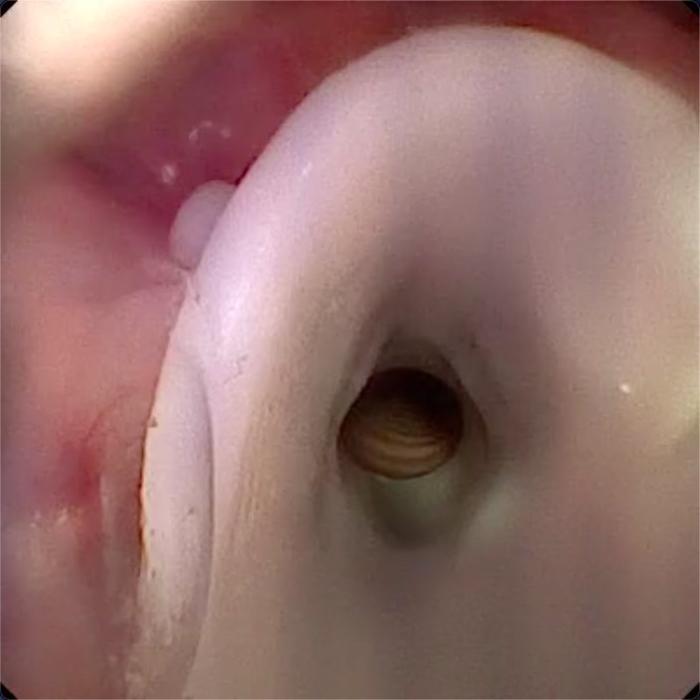
FIGURA 3. Stent de silicona radiopaca colocado en glotis de perro con parálisis laríngea.
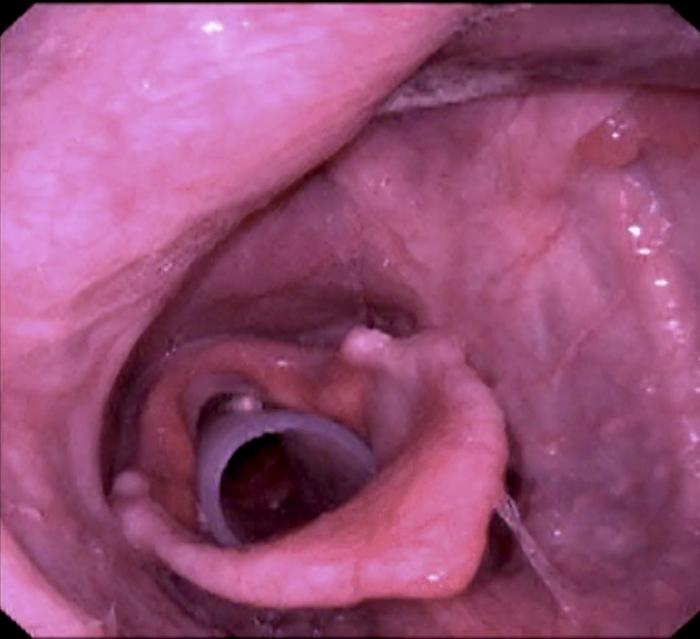
FIGURA 4. Stent de silicona translucida colocado en glotis de perro con parálisis laríngea.
Uso de stent de silicona en el colapso traqueal
El colapso traqueal es una patología frecuente en los perros e infrecuente en los gatos. La patogenia de esta enfermedad se basa en una degeneración progresiva del cartílago traqueal con un aplanamiento progresivo de la tráquea en dirección dorso-ventral. Se observará sobre todo en animales de raza pequeña y en el área cervical.
La tráquea es un conducto flexible que une las vías áereas altas (área nasal, oral, faríngea y laringe) y bajas (bronquios y bronquiolos). Está formada por anillos cartilaginosos en forma de “C” conectados por ligamentos anulares. La parte abierta de estos anillos está completada por el músculo o membrana
traqueal dorsal.
La situación de colapso es una reducción dinámica del diámetro de la luz traqueal cervical y/o torácica.
La reducción del diámetro traqueal suele ser dorso-ventral y conlleva un alargamiento de la membrana traqueal dorsal que será el causante del colapso traqueal dinámico.
Se desconoce, aunque se han descrito problemas en la función de los cóndrocitos que conducirá a defectos en el cartílago traqueal.
Hay una mayor incidencia de esta enfermedad en razas como el Yorkshire Terrier, Caniche, Pomerania, Bichón Maltés, Pug, Chihuahua y, en general, perros miniatura. Estos animales, con una nutrición deficiente o factores metabólicos pueden acabar con una alteración de la condrogénesis y del metabolismo del cartílago.
Se pensó en una inervación deficiente de la membrana traqueal pero no se ha demostrado.
En estudios realizados en la Universidad de Queensland durante dos años se encontró que de 2780 perros el 0.5 % presentaban esta patología. De 521 perros de raza miniatura el 2,7% (14 perros) tenían colapso traqueal. En diversos estudios se ratificó que suelen ser perros de edad media (6-7 años).
La tráquea es una estructura de cierta flexibilidad pero que apenas cambia con las variaciones de presión durante la respiración.
Inspiración. Cae la presión progresivamente de la glotis a los bronquiolos. Habrá un aumento del flujo de aire hacia los pulmones.
Espiración. Las estructuras cartilaginosas de las paredes de las vías respiratorias deberían evitar el colapso cuando aumente la presión intrapleural.
Algunos animales afectados tienen una carencia de condroitín sulfato y glucosaminoglicanos. Esto se traduce en una carencia de agua en la matriz del cartílago y, por lo tanto, debilitamiento. El debilitamiento del cartílago facilita el aplanamiento de la tráquea cervical en inspiración y al aplanamiento de las
vías respiratorias intratorácicas durante la espiración o durante la tos.
La obstrucción crónica da lugar a disnea y tos que induce a su vez laringo-traqueo-bronquitis crónica. Estos trastornos unidos a otros concurrentes (obstrucción de vías respiratorias altas, bronquitis crónica o insuficiencia cardíaca crónica) pueden producir grave sintomatología. La obesidad agrava más el proceso al alterarse la distensibilidad torácica y del diafragma, con lo que se asistirá a una disminución en la expansión del pulmón en la inspiración y a una tendencia evidente al colapso de las vías respiratorias.
Está descrita la intubación endotraqueal y las infecciones respiratorias como desencadenantes del cuadro.
El colapso cervical suele producir tos u obstrucción inspiratoria. El colapso intratorácico suele producirse durante la espiración y los signos suelen sermás fuertes. Pueden coincidir ambos colapsos o no e incluso se puedenobservar colapsos bronquiales sin que ocurran los traqueales.
Son frecuentes los ataques paroxísticos descritos como “graznido de ganso”. Los signos pueden ser provocados por agitación, presión sobre la tráquea, condiciones ambientales (elevada temperatura o humedad) o al comer o beber.
La tos puede acabar en vómito debido al intento de eliminar secreciones acumuladas en las vías respiratorias.
El método diagnóstico de elección del colapso traqueal se suele realizar mediante:
- La exploración del paciente.
- Radiografías torácicas en inspiración y espiración que ayudarán a ver los posibles cambios dinámicos del colapso.
- Traqueobroncoscopia. Mediante este procedimiento se puede visualizar el grado, la extensión y la gravedad del colapso. Es recomendable realizar en el mismo procedimiento y lavado traqueobronquial que ayuden a realizar un análisis citológico y un cultivo de las muestras recogidas.
La endoscopia de las vías respiratorias bajas es la técnica exploratoria indicada y más útil para el estudio y diagnóstico de trastornos patológicos de dichas vías, al proporcionar una visión directa y permitir al mismo tiempo obtener muestras de tejidos, estructuras específicas o muestras de lavado. Esta prueba
es fundamental cuando se quiere valorar anormalidades estructurales (colapso traqueal), presencia de masas, comprobar el estado de las paredes de la tráquea y bronquios, observar la posible inflamación de las vías respiratorias, presencia de exudados, torsiones lobares o la hemorragia pulmonar. También
es útil para recoger muestras para su análisis posterior.
En el tratamiento farmacológico que se suele administrar a un paciente al que se le va a colocar un stent debido a un colapso traqueal están:
- Corticoesteroides. Para reducir la inflamación pero tienen el inconveniente que aumentan el jadeo y el peso del animal.
- Broncodilatadores. Pueden ir bien al disminuir la probabilidad del colapso respiratorio. Teofilina 20 mg/kg/2 veces al día.
- Antibióticos. Si es posible por cultivo del lavado traqueobronquial.
- Antitusivos. Deben ser agentes potentes como el butorfanol 0.5-1.0 mg/kg/2-4 veces al día.
- Tratar la insuficiencia cardíaca.
- Tratar la obesidad.
- Cambio de correa a arnés
- Evitar el calor, la humedad, la agitación y el estrés.
La colocación de un stent puede ser un sistema rápido, eficaz y relativamente sencillo frente a las técnicas quirúrgicas descritas para este fin.
Hay múltiples opciones protésicas que van desde los implantes extraluminales con materiales plásticos, siliconas y fibra de vidrio, hasta los endoluminales con muy diferentes tipos de stents. Todas las opciones pueden presentar problemas secundarios a la colocación y pueden dar variados resultados.
El uso de un stent autoexpandible que abarque la porción colapsada para aumentar la permeabilidad de la vía aérea supone una alternativa prometedora de efecto inmediato y prolongado en el tiempo, así como de carácter no invasivo. Esta solución puede ser ideal en caso de urgencia para obtener una vía aérea de forma rápida y puede ser combinado con un tratamiento conservador. Las endoprótesis pueden ser una opción que puede ser adoptada de una forma mínimamente invasiva con una baja incidencia de complicaciones.
Indicaciones de las endoprótesis
Compromiso de la calidad de vida por los signos clínicos respiratorios.
- Fallo o falta de respuesta al tratamiento médico.
- Haber sufrido una obstrucción aguda de las vías aéreas con hospitalización.
La endoprótesis, en estos casos, intenta dar sostén estructural a los cartílagos y al músculo traqueal de forma extra-luminal o intra-luminal colocada mediante un procedimiento mínimamente invasivo o una técnica quirúrgica convencional y tratando de evitar la alteración del funcionamiento muco-ciliar.
El primer paso en la decisión de qué endoprótesis colocar es estudiar el colapso traqueal y definir la localización, grado, longitud y diámetro del mismo. Según algunos estudios, una endoprótesis puede mostrar mejoría clínica en más del 90 % de los casos.
El stent debe de ser fácil de colocar y debe aportar suficiente fuerza radial para mantener la permeabilidad traqueal, evitar su migración, tener alta elasticidad y buena flexibilidad longitudinal para evitar la fatiga del material, una aceptable bio-compatibilidad para evitar la formación de tejido de granulación o infección y mantener el aclaramiento muco-ciliar.
Es importante tener en cuenta que el stent, al ser desplegado, sufre un acortamiento del 20 al 40 % de su longitud.
Dentro de las complicaciones frecuentes asociadas a la colocación de stent en las vías aéreas se pueden citar:
- Mal posicionamiento.
- Imposibilidad técnica para la colocación.
- Perforación traqueo-bronquial.
- Enfisema.
- Neumotórax.
- Sangrado.
Complicaciones agudas tras la colocación de un stent traqueal (en los tres primeros días):
- Sangrado.
- Disfonía.
- Tos.
- Migración.
- Retención de secreciones.
- Obstrucción.
Complicaciones tardías tras la colocación de un stent:
- Infección.
- Shock séptico.
- Formación de tejido de granulación.
- Fatiga o fractura del metal.
- Dolor.
- Tos.
Como colocar un stent en la tráquea
Se deberá definir el diámetro y longitud del stent y esto es complicado y crucial para su función. Para saber el diámetro traqueal la forma más recomendable sería mediante tomografía computarizada, seguida de la radiografía y la fluoroscopia. Algunos autores recomiendan tomar stents con un diámetro 2-3 mm superior al diámetro medido en la tráquea para que éste se adapte adecuadamente. La longitud es a veces proporcionada por los fabricantes que utilizan tablas de acortamiento en expansión. La longitud máxima de un stent en la tráquea deberá dejar, al menos, 10 mm libres hacia el cartílago cricoides y otros 10 mm hacia la carina.
La aplicación del stent se realiza sin el tubo endotraqueal, mediante endoscopia o fluoroscopia en la zona afectada por el colapso. Una vez implantado el stent, se recomienda hacer radiografías laterales de ambos lados y ventro-dorsal para confirmar la posición final. Es conveniente hospitalizar al paciente durante 24 horas con medicación antitusiva como butorfanol o hidrocodona y se prescribirán antibióticos de amplio espectro junto a antiinflimatorios durante 1 o 2 semanas. En pacientes ansiosos se recomienda el uso de trazadona. Se recomienda hacer nuevos controles radiográficos cada 2 o 3 meses dependiendo de la evolución del animal. Es frecuente observar tos seca durante 1 mes postimplantación.
El propietario es fundamental en la recuperación del paciente y deberá controlar el nivel de disnea y tos así como cualquier cambio significativo en su evolución.
Se deberá vigilar un posible acortamiento del stent debido a la fuerza radial que ejerce sobre la tráquea durante el primer mes. Este acortamiento suele ocurrir más en la tráquea torácica que en la cervical, produciendo una retirada progresiva del stent sobre la zona afectada, volviendo a presentarse los signos clínicos de colapso traqueal.
Otras complicaciones que se pueden observar son la rotura del stent, la formación de tejido de granulación con o sin infección asociada, etc. Estas complicaciones pueden ser graves y requerir una nueva implantación de stent.
Los stents más utilizados para el colapso traqueal son los stents metálicos autoexpandibles, que suelen estar fabricados con acero inoxidable o nitinol. Los de acero inoxidable suelen asociarse a muchas complicaciones como el acortamiento y la formación de granulomas. Los stents de nitinol autoexpandibles suelen ser más sencillos de colocar y tienen menos problemas de migración y fractura.
En cuanto a los stents de silicona, éstos deben de tener mucho grosor de pared para ser capaces de dilatar la tráquea. La silicona produce un proceso inflamatorio agudo al mes de su implantación así como una metaplasia escamosa secundaria a la irritación prolongada de forma crónica. La metaplasia escamosa tiende a acumular secreciones al no presentar una superficie ciliada como el epitelio traqueal normal.
Algunos stents van recubiertos de fármacos antiproliferativos, como el paclitaxel, que se libera de forma lenta y local, pudiendo reducir de forma significativa la formación de tejido de granulación. En algunos estudios se prefieren los stents de nitinol a los de liberación de fármacos ya que parece que generan menos complicaciones secundarias.
También existen stents bioabsorbibles de materiales biodegradables con propiedades de expansión aceptables, que podrían evitar una segunda intervención para retirar el stent.
La colocación de un stent traqueal de silicona es una técnica simple que no requiere un equipamiento muy especializado. Los stents pueden ser colocados y recolocados hasta que se consigue una localización adecuada. En la tráquea, tras un cierto tiempo de al menos 2 meses, se ha observado que puede existir un cierto endurecimiento de la pared traqueal secundario a la inflamación crónica y que puede dar soporte estructural anatómica durante un tiempo. Se pueden conseguir diferentes diámetros y longitudes para adaptar el stent que mejor encaje en la tráquea del paciente afectado. Generalmente, la colocación puede ser más compleja que en la glotis debido a que el stent debe entrar doblado hasta su localización definitiva o mediante ópticas especiales de tipo telescópico. Otro problema asociado a los stents de silicona puede ser la obtención de endoprótesis de la longitud adecuada. Los autores, han podido solucionar este problema uniendo dos prótesis y fijándolas a la pared traqueal mediante un punto, aunque no es lo ideal (Figura 3).
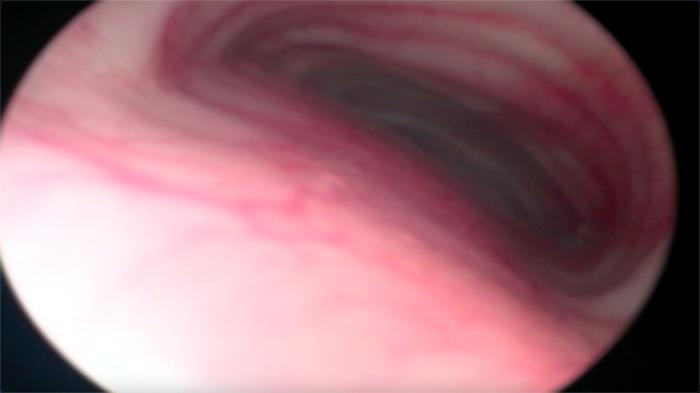
FIGURA 1. Grado II de colapso traqueal en un perro.
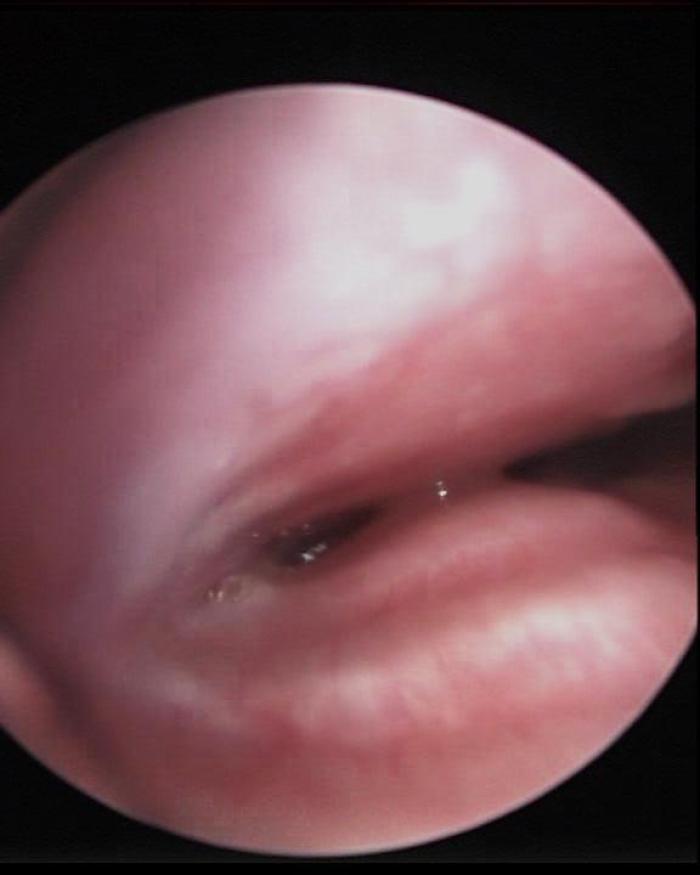
FIGURA 2. Grado IV de colapso traqueal en un perro.
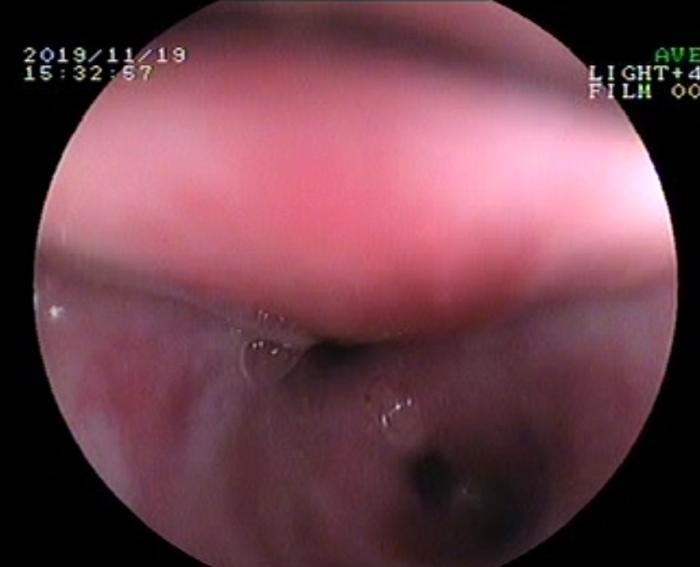
FIGURA 3. Colapso de bronquio principal en un perro.
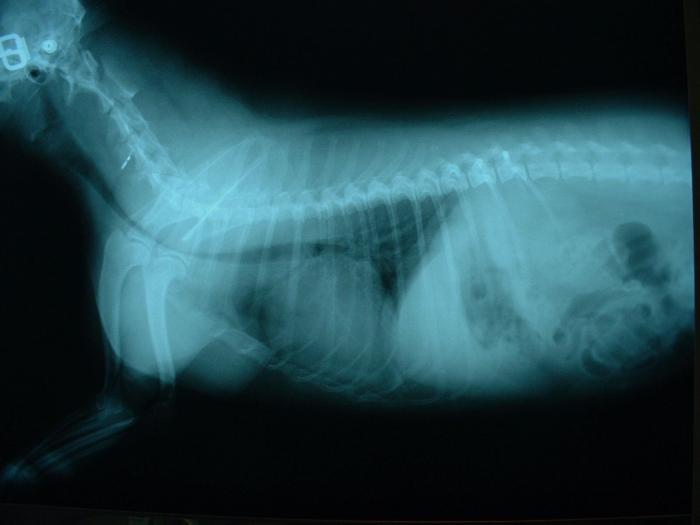
FIGURA 4. Radiografía laterolateral con colapso traqueal cervico-torácico en uN perro.
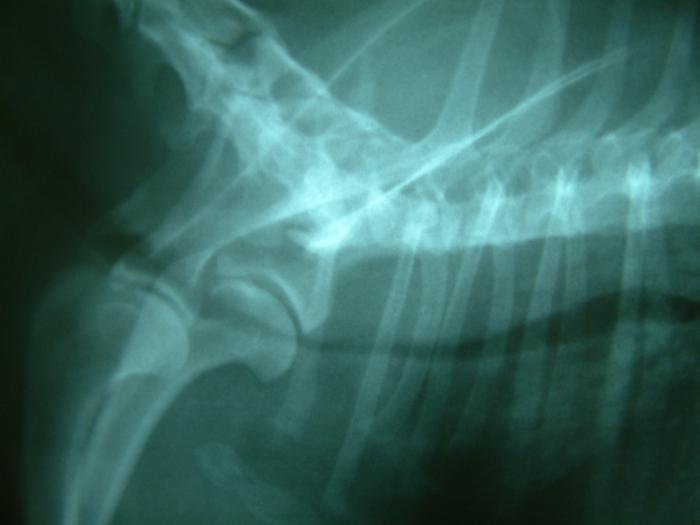
FIGURA 5. Radiografía laterolateral de perro con colapso traqueal torácico.
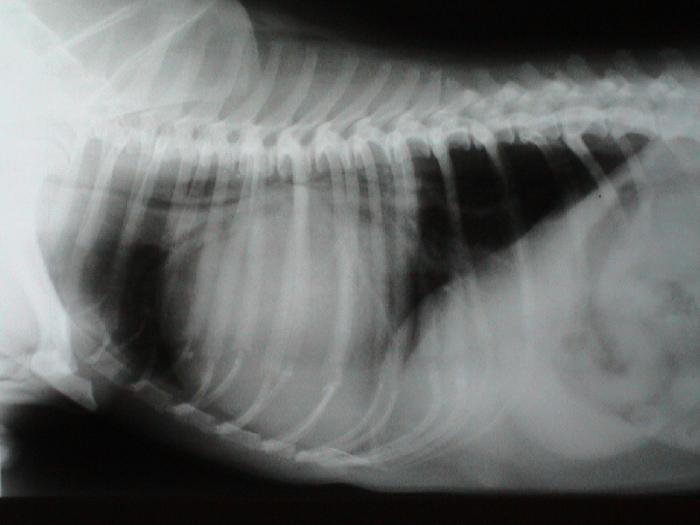
FIGURA 6. Radiografía laterolateral de perro con colapso traqueal grave torácico.
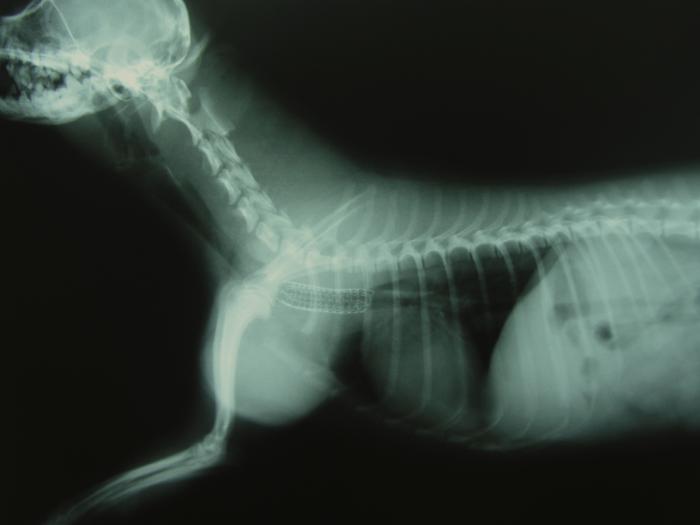
FIGURA 7. Radiografía laterolateral del perro de la radiografía 4 tras colocarle un stent metálico con recubrimiento traquea.
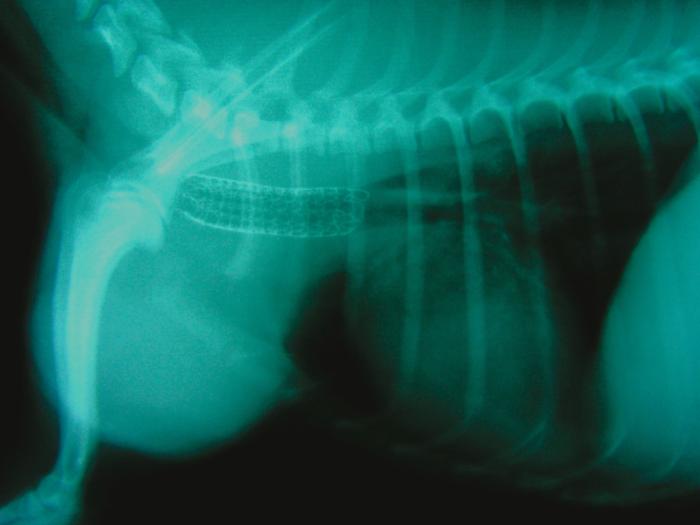
FIGURA 8. Radiografía ampliada con posición laterolateral del perro de la radiografía 4 tras colocarle un stent metálico con recubrimiento en tráquea.
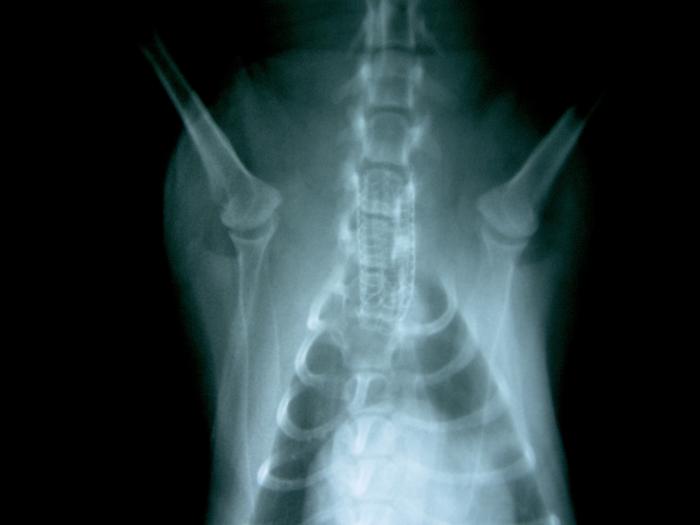
FIGURA 9. Radiografía ampliada con posición ventrodorsal del perro de la radiografía 4 tras un stent metálico con recubrimiento en tráquea.
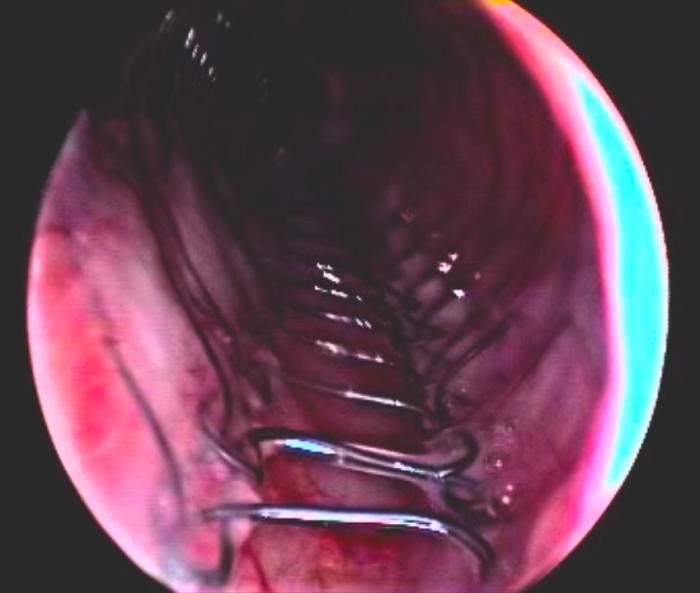
FIGURA 10. Vista endoscópica del stent metálico con recubrimiento para tratar un colapso traqueal.
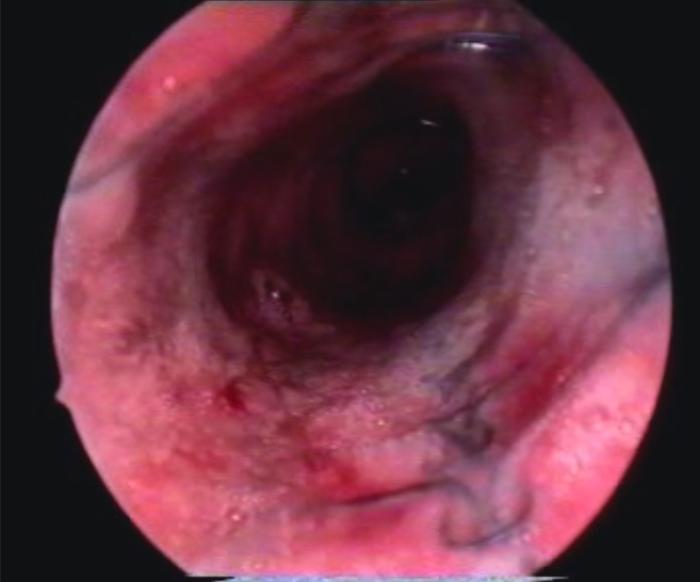
FIGURA 11. Mismo stent de la figura 10 un año después de su implantación. Obsérvese como ha sido recubierto por la mucosa.
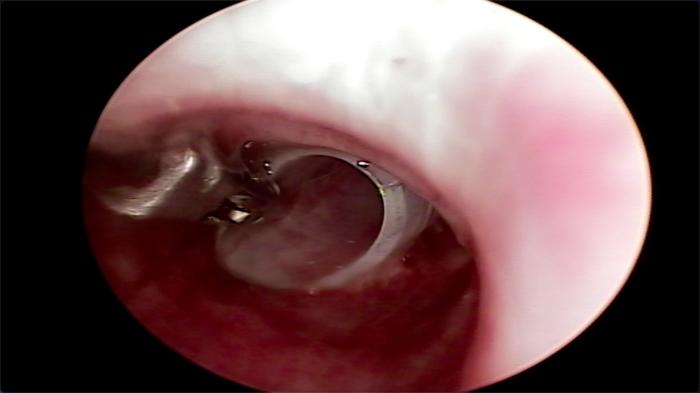
FIGURA 12. Visualización endoscópica de la colocación de un stent de silicona para el tratamiento de un colapso traqueal.
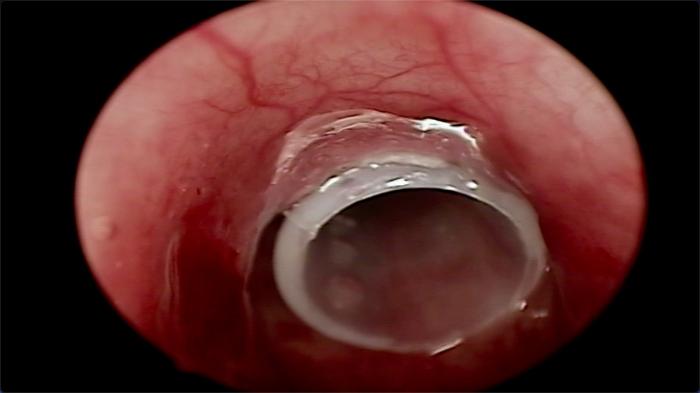
FIGURA 13. Mismo stent de la figura 12 una vez colocado en la posición deseada para tratar el colapso traqueal.
 by Multimédica
by Multimédica