Hipertiroidismo felino: actualización y revisión
Resumen breve
El hipertiroidismo felino es una patología causada por la excesiva secreción de T3 (triyodotironina) y T4 (tiroxina) por la glándula tiroides debido a factores que alteran la fisiología glandular generando desde una hiperplasia a una neoplasia (Figura 1). Esta enfermedad descubierta en el año 1979 por el Dr. Mark Peterson1 es de gran casuística en los Estados Unidos.Índice de contenidos

Introducción y situación actual
El hipertiroidismo felino es una patología causada por la excesiva secreción de T3 (triyodotironina) y T4 (tiroxina) por la glándula tiroides debido a factores que alteran la fisiología glandular generando desde una hiperplasia a una neoplasia (Figura 1). Esta enfermedad descubierta en el año 1979 por el Dr. Mark Peterson1 es de gran casuística en los Estados Unidos.
Hoy en día está tomando también gran importancia en varios países, de aquí la importancia de realizar una actualización y revisión.
El 98.3 % de los pacientes con hipertiroidismo tiene adenomas tiroideos benigno y el 1.7 % restante presentará carcinomas tiroideo2; sabiendo que los adenomas pueden sufrir una transformación a carcinomas3 teniendo la misma naturaleza en su desarrollo. La extensión de la enfermedad se categorizó según los cinco patrones de captación de 99mTcO4- 2.
- Enfermedad Unilateral
- Enfermedad bilateral simétrica
- Enfermedad bilateral asimétrica
- Enfermedad multifocal (más de 3 áreas de captación de 99mTcO4-
- Enfermedad no clasificable (tejido ectópico en conjunto con enfermedad unilateral, tejido ectópico aislado, carcinomas con uno o dos áreas de captación de 99mTcO4- ).
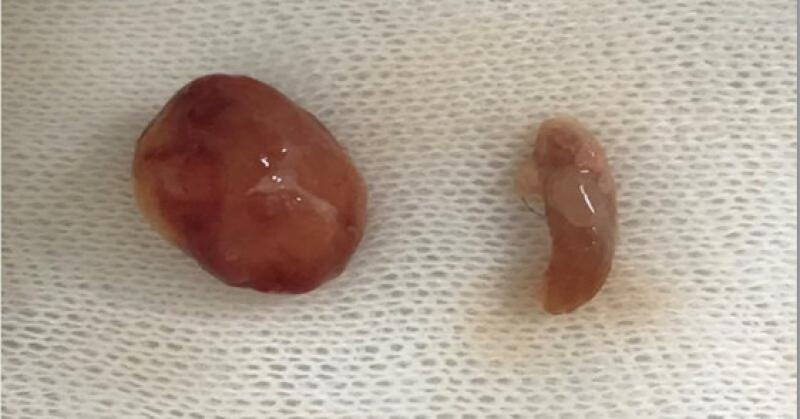
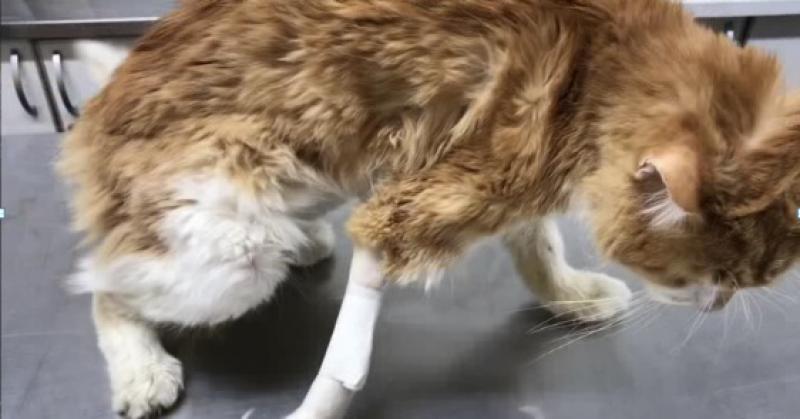
Un estudio publicado por El Dr. Mark Peterson en el año 20124 muestra que hoy en día han sido identificados los factores y la fisiopatología que cursaría con el desarrollo de la neoplasia tiroidea. Se nombrarán alguno de los más destacados; para más información referirse a la bibliografía citada.
Deficiencias o excesos nutricionales
- Las dietas enlatadas han sido categorizadas como potenciales factores, en especial las harinas de pescado, de hígado y de menudos. Los excesos o déficit de iodo y sobre todo las isoflavonas de soja también están siendo investigadas.
Disruptores del eje tiroideo
- Bisfenol A. Este producto es un elemento esencial que se usa en las latas de comidas enlatadas para evitar su corrosión.
- Metimazol. Este fármaco paradójicamente ha sido involucrado en la génesis de carcinomas tiroideos en pacientes tratados a largo plazo, aumentando la probabilidad a un 20 % en pacientes tratados durante 4 años3,4,5.
Se conoce también de la relación entre el hipertiroidismo y la enfermedad renal crónica (Figura 2). Tanto el exceso como el déficit de hormonas tiroideas alteran la funcionalidad renal6. Por lo tanto se deben contar con nuevas herramientas para categorizar mejor a los pacientes para tomar decisiones terapéuticas (ver sección de Hipertiroidismo y enfermedad renal crónica).Luego de estos avances de los últimos tiempos surgen varios interrogantes:
- Si se conocen los factores que tenderían a generar la neoplasia tiroidea; ¿Se podría ayudar a prevenir la enfermedad?
- Conociendo la existencia de los 5 patrones posibles de la enfermedad tiroidea, el uso de centellografía se hace obligatorio para el diagnóstico y terapéutica.
- Las neoplasias benignas pueden sufrir transformación a neoplasias malignas. Las drogas antitiroideas están siendo involucradas en el desarrollo de esta transformación y se debe recalcar siempre que las terapias médicas no son curativas en este caso. La terapia con iodo radioactivo (I-131) debería ser la terapia de elección en la gran mayoría de los pacientes y en caso de no estar disponible, evaluar la terapia quirúrgica; siempre y cuando el paciente amerite.
- Se debe comenzar a reevaluar a los pacientes con hipertiroidismo y enfermedad renal crónica concomitante de manera exhaustiva comenzando a utilizar herramientas como el uso de la dimetilarginina simétrica (SDMA) o la interpretación de la tirotropina canina (TSH) para poder tomar las decisiones que generen mejor calidad de vida.
Son muchos los interrogantes, he aquí esta revisión y actualización de esta patología.
Etiología
Neoplasia benigna
Como se mencionó el 98.3 % de los pacientes con hipertiroidismo tiene adenomas tiroideos. Histopatológicamente consiste en simples o múltiples nódulos entre 1-3 mm de diámetro7. Puede haber áreas quísticas involucradas teniendo en cuenta que el desarrollo de quistes suele ser consecuencia de pacientes con hipertiroidismo, pero puede asociarse también a paciente eutiroideos con neoplasias tanto benignas como malignas8.
Neoplasia maligna
El 1.7 % de los pacientes con hipertiroidismo tiene neoplasias de origen maligno. El método de elección siempre será la histopatología pero como alternativa se desarrolló el acrónimo SHIM-RAD de sus siglas en inglés (Severe-Huge-intrathoracic-multifocal-refractory)3.
- Hipertiroidismo severo: T4t mayor a 23 ug/dl
- Tamaño grande: nódulo mayor a 8 cm tanto a la palpación como en la centellografía
- Nódulos intratorácico: el compromiso intratorácico podría indicar tanto tejido ectópico como metástasis.
- Enfermedad multifocal: categorizado como más de 3 áreas de captación de 99mTcO4- en el centellograma.
- Refractario a drogas antitiroideas: categorizado como dosis mayores a 15-20 mg/por día.
A esta clasificación se puede agregar estos determinantes9
- Historia de larga data de hipertiroidismo > a 2 años.
- Recurrencia o falta de respuesta ante la tiroidectomía o terapia con iodo radioactivo.
- Patrón heterogéneo con márgenes irregulares en el centellograma.
- Patrón linear multifocal en el centellograma.
La mayoría de los carcinomas tiroideos felinos son funcionales, aunque existen los no funcionales pero abarcando 1/3 de los carcinomas tiroideos9.
Los criterios histopatológicos para clasificar los carcinomas tiroideos son:
- Invasión extracapsular.
- Invasión vascular.
- Pleomorfismo celular.
- Alto índice mitótico.
Teniendo en cuenta que también hay reportes que indican tejido mixto tanto benigno como maligno aportando a la teoría de la malignizacion de neoplasias benignas10.
Más allá de su naturaleza maligna, el potencial metastásico es bajo y el índice biológico es lento.
Signología Clínica
Las hormonas tiroideas tienen varios órganos blancos, y el aumento en la secreción de estas se verá reflejado en un aumento de la acción.
Signos metabólicos
- Pérdida de peso crónica a expensas de una polifagia marcada.
- Intolerancia al calor reflejada muchas veces en acicalamiento excesivo.
Fisiopatología
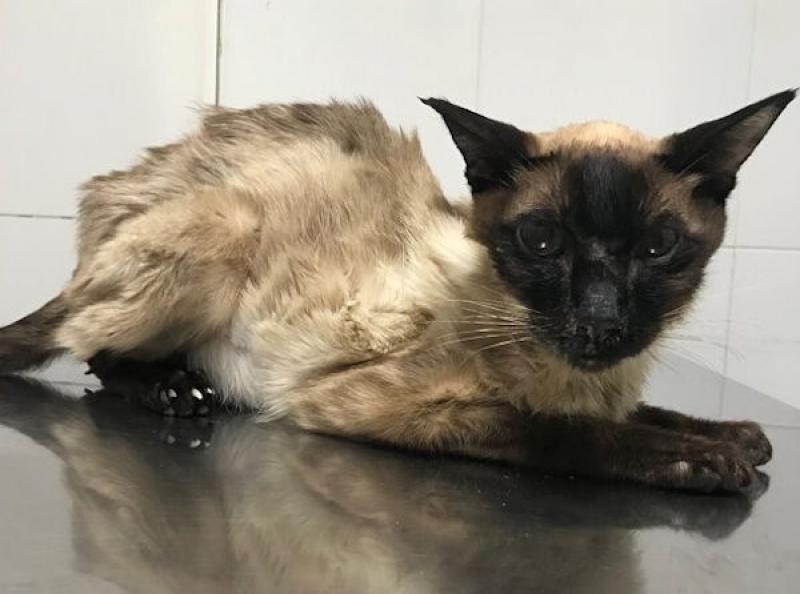
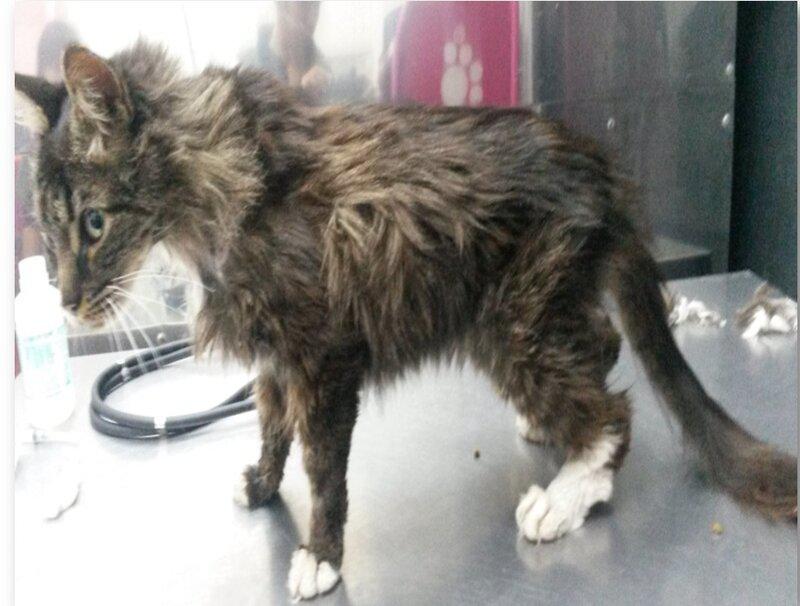
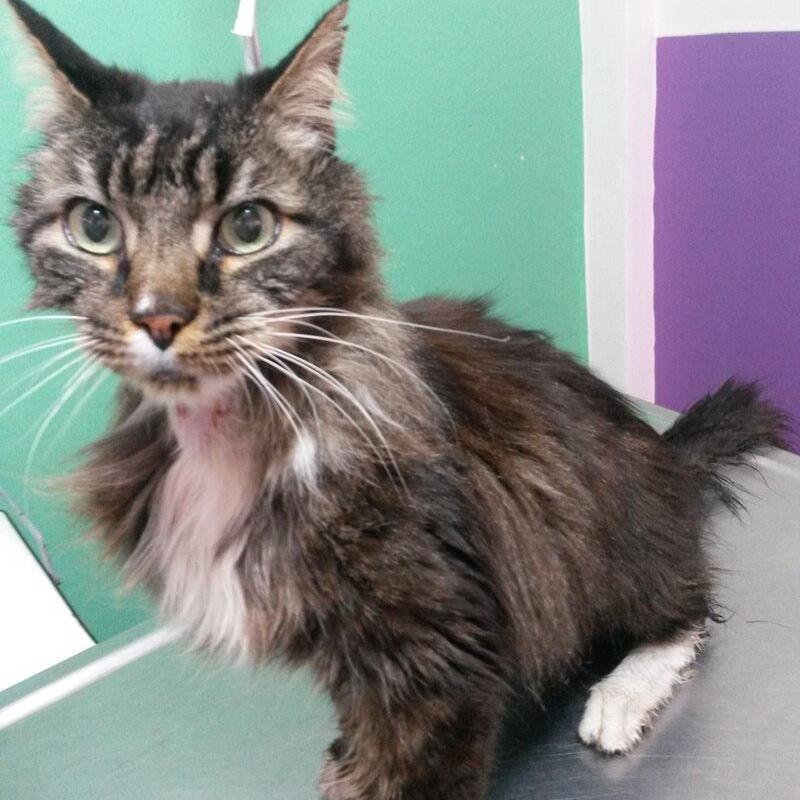
Aumento del metabolismo basal y de la generación del calor por parte de las mitocondrias. Se genera un catabolismo marcado llevando a una pérdida de peso crónica (Figura 3). La pérdida de peso crónica en un animal que aparenta estar sano es el signo cardinal del paciente con hipertiroidismo.
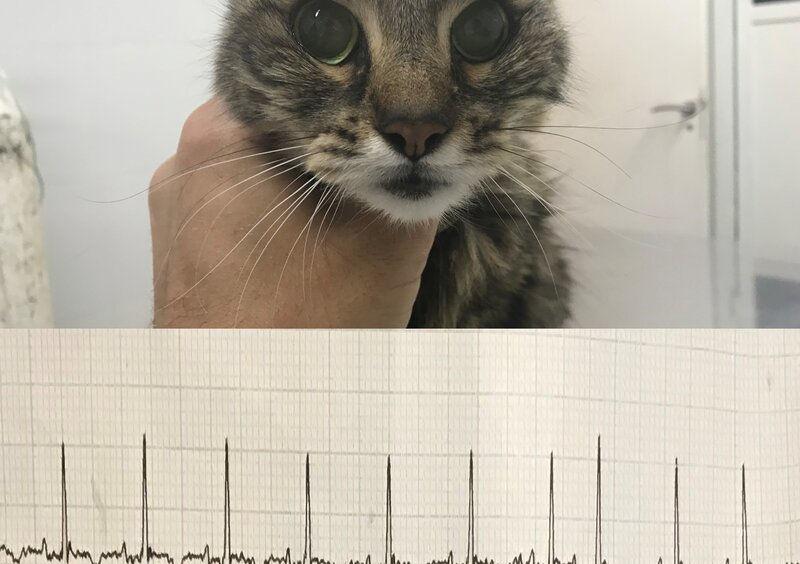
Es muy diferente a la pérdida de peso crónica que podrían manifestar otras patologías como la enfermedad renal crónica, la enfermedad inflamatoria intestinal o la presencia de enfermedades virales, ya que los pacientes hipertiroideos se mantienen con un estado mental alerta con polifagia y polidipsia hasta un estadio terminal en el cual se manifiesta una sarcopenia severa y se genera debilidad; pero hasta este momento aparentan estar sanos a la vista del propietario. La atrofia muscular marcada en la cara refleja la fascie característica de estos pacientes (Figura 4).
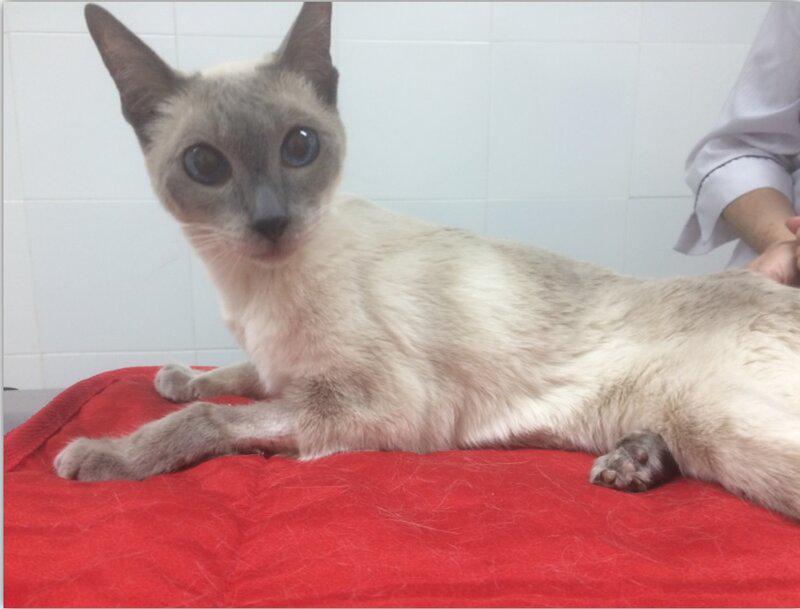

Signos gastrointestinales
- Vómitos
- Diarreas
Fisiopatología
- Acción directa en la zona quimiorreceptora.
- Polifagia.
- Aumento del tránsito gastrointestinal.
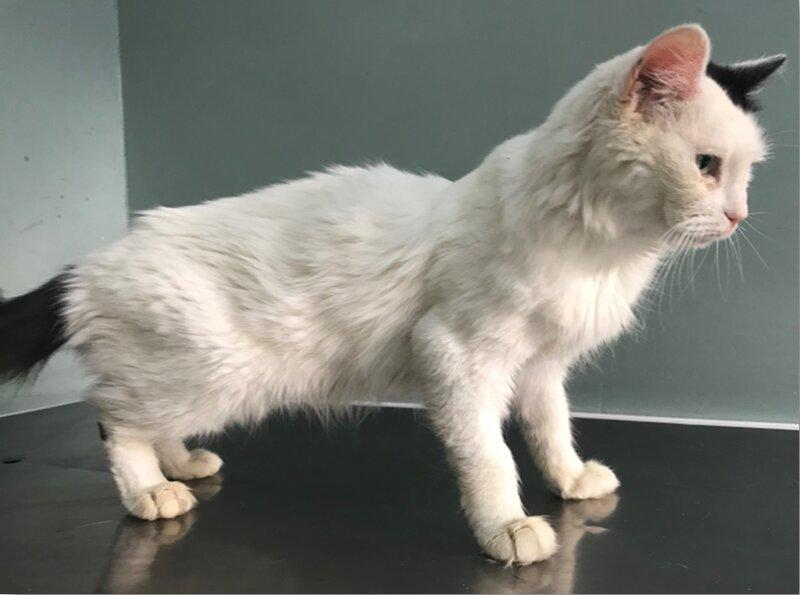
Estos 3 mecanismos subyacentes llevan a que el paciente padezca de vómitos y diarreas crónicas. El gran diferencial en estos casos es la enfermedad inflamatoria intestinal (Figura 5). Hoy en día el autor también presta atención dentro los diferenciales a la insuficiencia pancreática exocrina felina (Figura 6).
Signos neuromusculares
- Intolerancia al estrés.
- Tendencia a no dormir y estar en movimiento constante.
- Dificultad respiratoria asociada a intolerancia.
- Temblores.
- Convulsiones.
Fisiopatología
- Estimulación del sistema adrenérgico.
- Acción directa de las hormonas tiroideas.
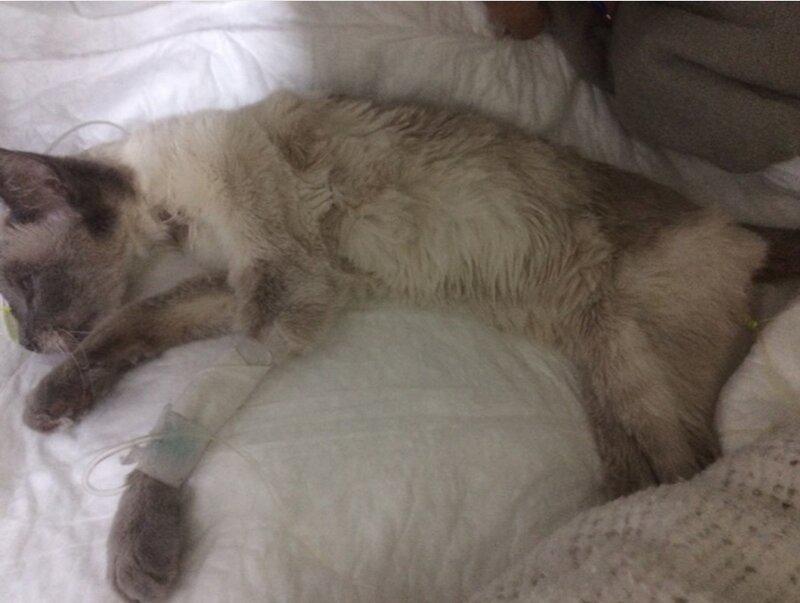
Estos pacientes no siempre se encuentran en un estado de hiperactividad constante, pero si es muy común que manifiesten intolerancia a ser manipulados incluso muchas veces presentando taquipnea y dificultad respiratoria evidente (Figura 7).
Muchas veces el dato anamnésico refiere a que el paciente duerme menos que antes. Los temblores y convulsiones son una consecuencia extremadamente rara del hipertiroidismo12.
Aunque fisiopatológicamente podrían disminuir el umbral a las convulsiones mediante la alteración de neurotransmisores o generar un ambiente de hipoglucemia e hipoxia a nivel cerebral debido al aumento del consumo, la asociación no sigue siendo clara. Algunos pacientes han manifestado convulsiones, pero aún queda en duda si adjudicarlos al hipertiroidismo en tales casos (Figura 8).
Signos Cardiovasculares
- Taquicardia sinusal.
- Soplo.
- Hipertrofia interventricular o ventricular izquierda.
- Hipertensión.
- Presencia de arritmias.
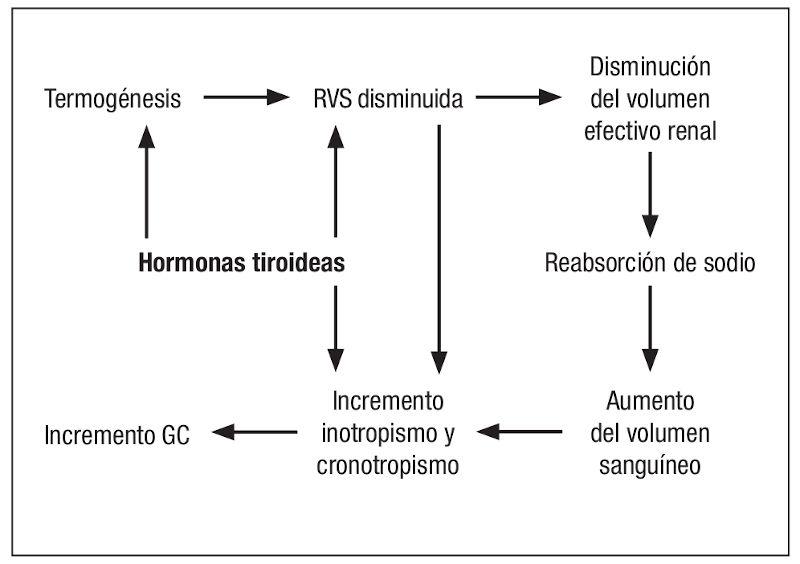
Fisiopatología (Figura 9)
Las hormonas tiroideas tienen acción directa tanto a nivel cardiaco como a nivel vascular. La taquicardia es un hallazgo muy común, pudiendo encontrar a veces extrasístoles auriculoventriculares y ventriculares como las arritmias más comúnmente diagnosticadas13 (Figura 10).
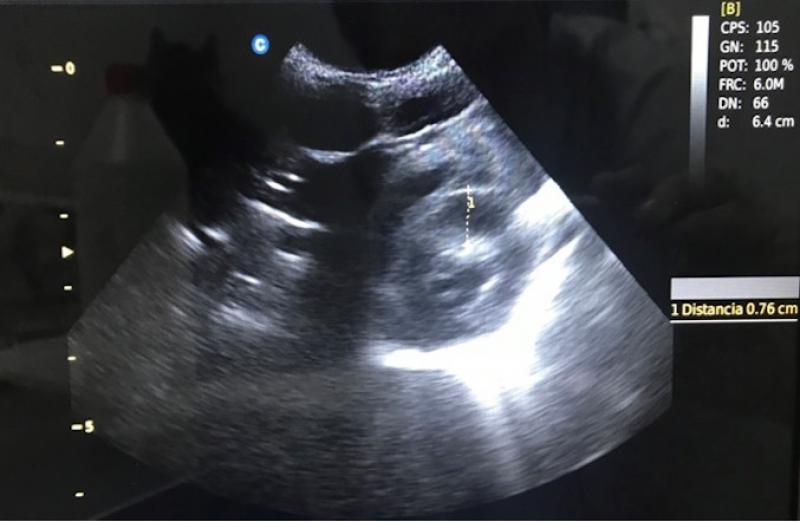
La hipertrofia ventricular o interventricular es el hallazgo ecocardiográfico más común 14 (Figura 11). Muchas veces las alteraciones camerales revierten luego del tratamiento y en caso de no revertir pensar en daño permanente o enfermedad cardiaca primaria subyacente.
Estos hallazgos en conjunto con la taquicardia pueden dar origen al ruido de galope debido al rápido llenado ventricular y a soplos cardiacos originados por la obstrucción del flujo de salida y no en relación a insuficiencia mitral o tricuspidea como se suponía anteriormente.
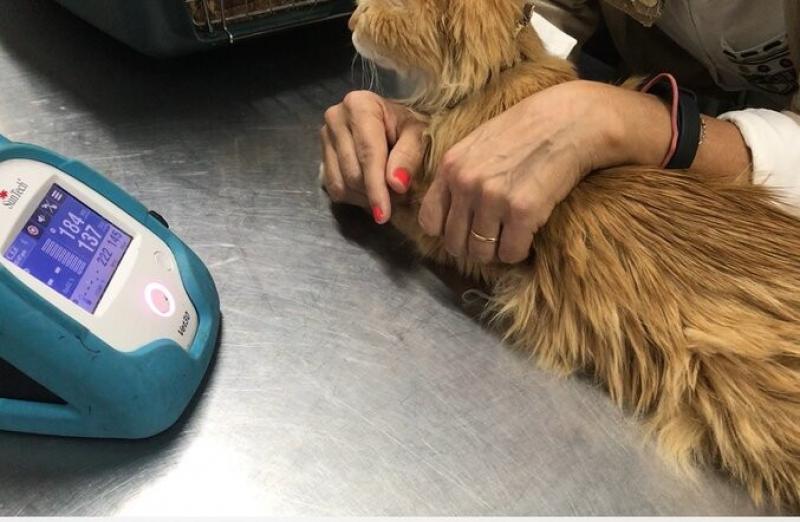
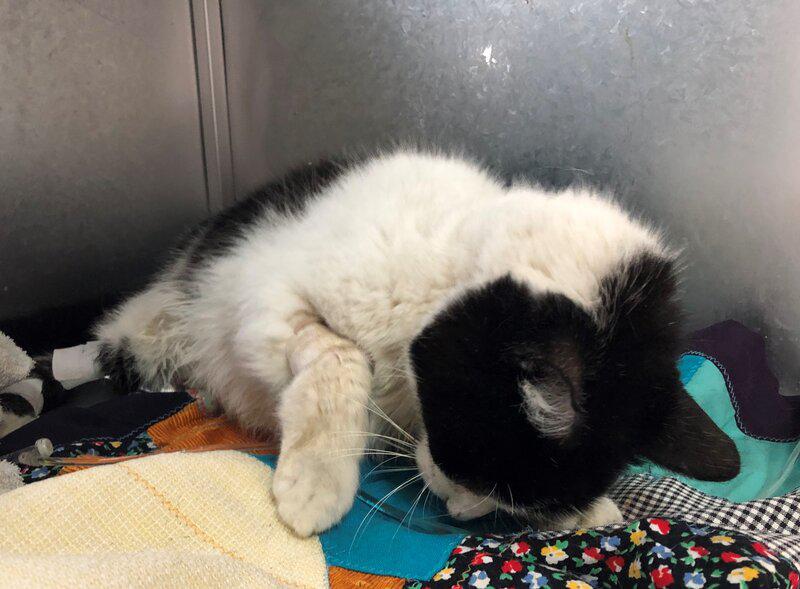
La hipertensión no es un hallazgo tan común como se creía15, ya que la disminución de las resistencias generan un alteración de la presión diastólica y como mecanismo compensatorio aumenta el flujo generando hipertensión en algunos pacientes15 (Figura 12) . Antes de adjudicarla al hipertiroidismo descartar siempre presencia de enfermedad renal crónica y de hiperaldosteronismo felino (Figura 13).
Signos urinarios
- Poliuria-Polidipsia
Fisiopatología
- Hiperfiltracion glomerular por aumento del gasto cardiaco.
- Alteraciones electrolíticas.
- Polidipsia primaria.
Esta hiperfiltración glomerular tiene su fisiología basada en el sistema renal y el sistema cardiovascular que tienden a dar un aumento del volumen de filtrado glomerular como resultado del aumento del gasto cardiaco (ver sección signos cardiovasculares).
La estimulación a nivel cerebral genera un cuadro de polidipsia primaria15. Contribuye también la hipopotasemia que se genera por lavado medular. Tener en cuenta que la manera de evaluar de forma objetiva la polidipsia-poliuria es la medición de la densidad urinaria (Figura 14).
Agrandamiento de glándula tiroides
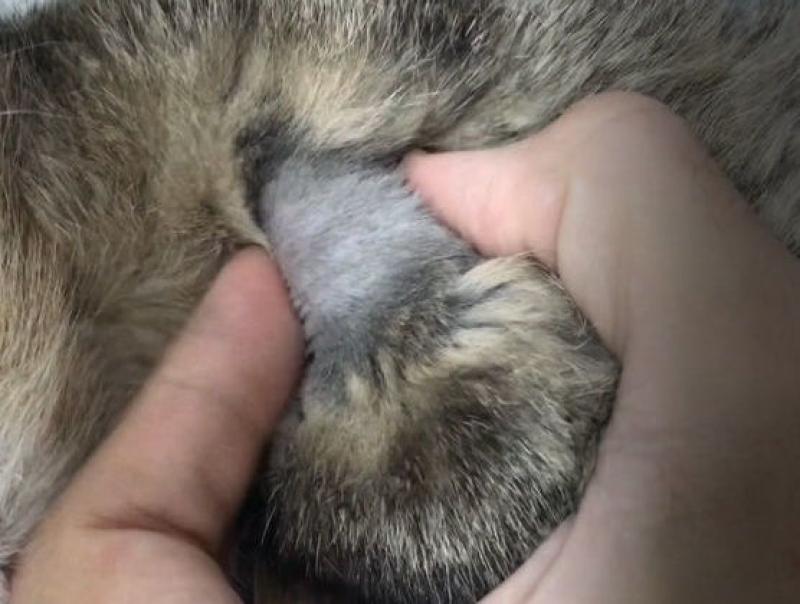
Todos los gatos hipertiroideos presentan un aumento de tamaño de uno o ambos lóbulos tiroideos y en la gran mayoría se detecta por palpación. La técnica consiste en extender la cabeza del paciente suavemente y con el dedo índice situarse en el canal yugular e ir descendiendo bien despacio desde la laringe hasta la entrada del tórax.
Evaluando primero un lado y luego el otro lado. Se debe tomar el tiempo necesario, ya que esta maniobra es de vital importancia en el diagnóstico. Tener en cuenta:
- Muchas veces el área debe ser rasurada y humedecida con alcohol.
- Si se extiende mucho el cuello, el nódulo tiroideo se “esconderá” debajo de los músculos y no podrá palparse.
- Los nódulos tiroideos no se encuentran muy adheridos al tejido circundante por lo cual se palpará como un nódulo que se desliza debajo del dedo de quien realice la maniobra (Figura 15).
- Si los nódulos tiroideos no son palpables, puede ser que por su peso y movilidad hayan descendido a la entrada del tórax.
Hallazgos a nivel sanguíneo
Hematología
Son poco comunes y de muy escaso valor diagnóstico.
Eritrocitosis
Fisiopatología
- Aumento de eritropoyetina por aumento del consumo de oxígeno.
- Efecto directo en la médula ósea.
Leucograma de estrés
Puede haber linfopenia, eosinopenia, pero son cambios inespecíficos.
Bioquímica
Elevación de las enzimas hepáticas
Fisiopatología
- Hipoxia y efectos tóxicos directo del catabolismo.
Es un hallazgo extremadamente común13 (Figura 16). Una gran diferencia con los humanos es que la GGT no se incrementa en pacientes hipertiroideos felinos16, y la fosfatasa alcalina suele estar elevada en un gran porcentaje por la isoenzima ósea17.
| BIOQUÍMICA |
| Termogénesis | Valor | Valor relativo |
| GPT | 208 | <80 UI |
| GOT | 100 | <80 UI |
| FAS | 251 | <100 UI |
Ecográficamente los cambios a nivel hepático son inespecíficos16. La funcionalidad hepática se encuentra conservada y los cambios histopatológicos son mínimos y refieren a infiltración grasa centrolobulillar13. Los valores vuelven a la normalidad luego de la terapéutica concluyendo cambios totalmente atribuidos al hipertiroidismo16.
Hiperfosfatemia a expensas de ERC
Fisiopatología
Es bastante compleja ya que interfieren varios factores. El exceso de hormona tiroidea estimula el recambio óseo aumentando en poca cantidad el fósforo y en gran cantidad el calcio que induce una disminución de la paratohormona para mantener niveles normales de calcemia.
Esta disminución de la paratahormona junto con el exceso de hormona tiroidea estimulan la reabsorción renal de fósforo llevando a una hiperfosfatemia y a elevación de la paratohormona consecuente.
El calcio iónico, a pesar de haber recambio óseo y aumento de la paratohormona finalmente, se encuentra disminuido creyéndose que es quelado por fósforo. En conclusión los pacientes hipertiroideos manifiestan aumento de fósforo, disminución del calcio iónico y aumento de paratohormona.
Urea y Creatinina
Ver sección de Hipertiroidismo y Enfermedad Renal Cronica.
Glucemia
La insulinoresistencia generada por hormonas tiroideas es muy leve, muchas veces generando solamente intolerancia a la glucosa sin llevar a una diabetes mellitus clínica18,19. La asociación entre la diabetes y el hipertiroidismo debe ser tenida en cuenta, pero la incidencia es realmente baja en comparación con el hiperadrencoroticismo o el hipersomatotropismo20.
Perfil hormonal
La interpretación del perfil hormonal es esencial en el diagnóstico (Figura 17). En los datos que se muestran en esta sección, obtenidos del trabajo citado por el Dr. Peterson 21 se puede concluir que las diferencias entre medir T4t o T4l son muy poco significativas, que la T3 tiene demasiada baja sensibilidad para ser tenida en cuenta, y que la medición de TSH canina tiene que comenzar a tenerse en cuenta para poder discernir aquellos pacientes que la interpretación de la clínica o de las fracciones de hormonas tiroideas sea difícil de interpretar.
| PERFIL TIROIDEO |
| Análisis | Valor | Valor relativo |
| T4T | 8.6 | 1-3 ug/dl |
| T4T | 2.76 | 0.6-1.6 ng/dl |
| TSH | 0.03 | 0.03-0.5 mg/dl |
Medición de T3
Sensibilidad: 65.3 %
- N = 917 gatos hipertiroideos.
- N = 599 niveles de T3 elevados.
- N = 318 niveles de T3 normales.
Especificidad: 98.2 %
- N = 163 gatos sanos.
- N = 3 con valores de T3 levemente elevados.
- N = 160 con valores de T3 normales.
Muy baja sensibilidad debido a:
- La gran mayoría deriva de la T4 (60 %).
- Con el tiempo se deprime la conversión de T4 a T3.
- Muy afectada por síndrome de enfermo eutiroideo.
Medición de T4t
Sensibilidad: 95.2 %
- N = 917 gatos hipertiroideos.
- N = 873 niveles de T4 elevados.
- N = 44 niveles de T4 normal.
Especificidad: 96.3 %
- N = 163 gatos sanos.
- N = 6 con valores de T4 elevados.
- N = 157 con valores de T4 normales
Medición de T4I
Sensibilidad: 96.8 %
- N = 917 gatos hipertiroideos.
- N = 888 niveles de T4l elevados.
- N = 29 niveles de T4l normal.
Especificidad: 95.1 %
- N = 163 gatos sanos.
- N = 8 con valores de T4l elevados.
- N = 155 con valores de T4l normales.
Los % restantes de pacientes con respecto a la sensibilidad tienen su origen en pacientes con hipertiroidismo oculto con fluctuaciones de los niveles.
Los % restantes de pacientes con respecto a la especificidad tienen su origen en que pacientes con enfermedades subyacentes por un mecanismo no del todo dilucidado producirían elevación de sus hormonas tiroideas.
Medición de TSH Canina
Sensibilidad: 98 %
- N = 917 gatos con hipertiroidismo.
- N = 899 valores < 0.03 ng/ml.
- N = 18 valores > 0.03 ng/ml.
Especificidad: 69 %
- N = 163 gatos sanos.
- N = 114 valores > 0.03 ng/ml.
- N = 49 valores < 0.03 ng/ml.
La medición de TSH canina detecta un 35 % de la fracción felina. El 98 % de los pacientes con hipertiroidismo mostrarán niveles de TSH < 0.03 ng/ml, por lo cual es un método extremadamente sensible y de screening. Pero su baja especificidad radica en que no se puede distinguir los niveles no detectados de los niveles suprimidos.
Centellografía
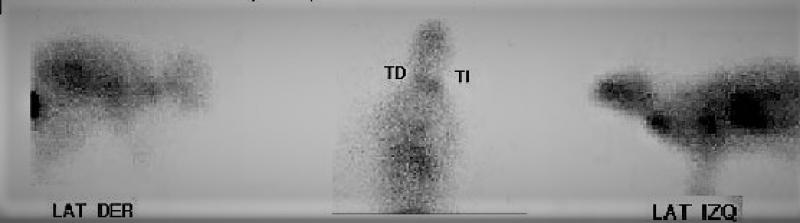
La centellografía es una herramienta obligatoria en todo paciente (Figuras 18 y 19) con hipertiroidismo ya que ayuda a:
- Diagnóstico de hipertiroidismo en fase oculta.
- Determinación de la extensión y compromiso.
- Determinación de metástasis.
- Determinación de tejido ectópico.
- Diferenciación de síndrome de enfermo eutiroideo.
- Determinación de masas cervicales.
- Calcular dosaje del I 131.
Cabe recordar que en este método se aplica un radioisótopo como el 99mTcO4- y luego mediante la evaluación del ratio tiroides/glándula salival se estima la capacidad funcional del tejido con una sensibilidad del 98.7 %2. La glándula tiroides, la glándula salival, la vejiga y la mucosa gástrica son órganos que captan iodo y por lo tanto tecnecio.
En el trabajo presentado por el Dr. Mark Peterson se describen los 5 patrones posibles de centellografía observados en 2096 gatos2 concluyendo que:
- 665 pacientes con enfermedad unilateral.
- 257 pacientes con enfermedad bilateral simétrica.
- 1060 pacientes con enfermedad bilateral asimétrica.
- 81 pacientes con enfermedad multifocal (más de 3 áreas de captación de 99mTcO4- ).
- 33 pacientes con enfermedad no clasificable (tejido ectópico en conjunto con enfermedad unilateral, tejido ectópico aislado, carcinomas con uno o dos áreas de captación de 99mTcO4- ).
Este trabajo destaca la importancia y que la centellografía es obligatoria en todo paciente con hipertiroidismo. La gran mayoría de los pacientes presenta enfermedad bilateral asimétrica, la cual no es perceptible macroscópicamente, ni ecográficamente, por lo cual instaurar una terapia quirúrgica en estos casos podría llevar al fracaso terapéutico.
La tiroides deriva embriológicamente del endodermo faríngeo que prolifera y migra desde la base de la lengua hasta la localización pre-traqueal dando origen a los lóbulos tiroideos. Una falla en el primordio tiroideo para descender puede dar origen a tejido tiroideo lingual o sublingual. A su vez la migración de la tiroides depende de su asociación con el saco aórtico.
Una falla en la separación del primordio tiroideo del saco aórtico puede originar una tiroides ectópica de localización en el mediastino o en la base del corazón. El tejido tiroideo ectópico está expuesto también a tumorogénesis. En este trabajo de 79 pacientes con tejido ectópico la gran mayoría fue de origen intratorácico, seguido por el tejido sublingual y por el tejido ectópico cervical lateral. En el caso de los carcinomas la gran mayoría cumplió con las características descriptas del acrónimo SHIM-RAD (ver sección carcinoma).
Terapéutica
Existen 4 métodos para poder manejar el hipertiroidismo, teniendo en cuenta ventajas y desventajas de cada método.
Terapia médica con drogas antiroideas
El principal representante de las drogas antitiroideas es el metimazol.
Presentación
- Oral.
- Transdérmica.
Acción
- Inhibición de la tiroperoxidasa.
Dosificación
- 1.25-2.5 mg totales cada 12 horas.
- Se puede llegar a evaluar pasar a una frecuencia de 24 horas a las 4 semanas
El monitoreo consta en evaluar los niveles de hormonas tiroideas (principalmente T4t) a los 15 días buscando valores cercanos al límite inferior. No interfiere el horario de chequeo con respecto a la medicación22.
Los efectos adversos del metimazol ocurren entre 10-25 % de los pacientes, siendo los más comunes el vómito, anorexia, letargia. Las discrasias sanguíneas, las alteraciones dérmicas y hepáticas ocurrieron en un % muy chico de pacientes23.
Estos efectos suceden generalmente entre el primer y segundo mes de tratamiento. En caso de no lograr los niveles buscados se aumenta 2.5 mg totales por día y se rechequea a los 15 días nuevamente. El autor realiza chequeo de control de hormonas tiroideas a los 15 días evaluando T4t y TSH y luego realiza chequeos de control de efectos adversos 1 vez por mes durante 3 meses.
Terapia con iodo radioactivo34
Objetivo
Restaurar el eutoriodismo sin causar hipotiroidismo y con la menor dosis posible
Acción y fundamento
- Las células tiroideas no diferencian el iodo (I.127) del iodo radioactivo (I.131).
- El 20-60 % del I.131 se acumula en la tiroides generando partículas β que dañan el tejido funcional.
- Se excreta en orina la mayor cantidad y el porcentaje restante en heces. Su vida media es de 8 días.
Protección del tejido sano
- El tejido sano se encuentra atrofiado y no captante; por retroalimentación negativa. Por esto se recomienda actualmente suspender drogas antitiroideas y dietas restringidas en iodo 5-7 días previos.
- Las partículas β, que causan el 80 % del daño tisular, viajan un máximo de 2 mm en tejido y tienen una trayectoria media (longitud de 400 μm). Por lo cual si las dosis calculadas son correctas la posibilidad de causar hipotiroidismo es baja.
Efectos adversos
- Disfagia –Fiebre asociada a la tiroiditis causada por la radiación.
- Carcinogénesis no reportada.
Posibles escenarios luego de la terapia con I.131
Eutiroidismo
- El paciente presentará niveles estables de hormonas tiroideas a los 3 meses.
Hipertiroidismo persistente
- En el caso de que las hormonas tiroideas persistan altas luego de los 3 meses, este paciente posiblemente necesitará otra dosis.
Hipotiroidismo transitorio/permanente
- Pueden estar bajas hasta los 3 meses y raramente hasta los 6 meses.
- Pasado los 6 meses evaluar resultados y terapéutica con levotiroxina.
Reincidencia
- Cuando reaparece generalmente se trata de nuevos nódulos. Se sugiere evaluar por lo menos 1 vez al año y realizar prevención.
La medición de la TSH canina lleva un papel muy importante en la detección del hipotiroidismo iatrogénico; una elevación por encima de 0.5 ng/ml indicaría hipotirodismo, ya que solamente se detecta un 35 % de la fracción felina, por lo tanto el valor incluso debería ser mayor. La medición debe ser rutinaria en los controles.
Cirugía
La tiroidectomía es efectiva y es un método curativo, pero la disponibilidad de centros de realización de terapia con iodo radioactivo está haciendo que a futuro tienda a ser menos común. En caso que no esté disponible la terapia con iodo radioactivo, sería la terapia indicada; siempre y cuando se realice centellografía previamente ya que macroscópicamente no se pueden identificar los casos de compromiso bilateral asimétrico (siendo los de mayor frecuencia), ni tampoco el tejido ectópico; y en tal caso que se realice extracción del tejido ectópico la recurrencia es común.
En el caso de compromiso bilateral, la tiroidectomía bilateral se realizará dependiendo del contexto, la edad del paciente y sobre todo teniendo en cuenta la posibilidad de hipotiroidismo e hipoparatiroidismo.
En conclusión la tiroidectomía debe indicarse si no hay disponibilidad de realizar terapia con iodo radioactivo y en los casos en que se pueda realizar centellografía ya que esto justifica el éxito de la terapia. Para descripción de la técnica quirúrgica referirse a bibliografía ya que no es la intención de esta revisión.
Manejo nutricional
Los requerimientos de iodo son de 0.46 mg/kg y en los alimentos implicados son de 0.32 mg/kg25. Las dietas restringidas en iodo son capaces de disminuir los niveles de T4t entre 2-4 meses26.
Los pacientes con niveles más altos son los que llevará más tiempo disminuirlos ya que la hormona tiroidea está almacenada junto con tiroglobulina para poder suplir al cuerpo durante 2-3 meses.
Estos pacientes deben comer la dieta de por vida, sin interrupción, ni con otros tipos de alimento. Incluso la restricción del iodo ha sido implicada en el desarrollo del hipertiroidismo por ende no debería ser de acceso a felinos eutiroideos4.
No ha sido estudiada la probabilidad de malignización de la neoplasia pero el mecanismo fisiopatológico es el mismo que se desarrollaría en la terapia con metimazol.
Todavía faltan estudios para poder evaluar la viabilidad a largo plazo de esta terapia; pero hoy en día se sabe que estos pacientes mantienen su frecuencia cardiaca alta y no ganan peso, por lo cual fisiológicamente persisten siendo hipertiroideos26.
Conclusiones generales de la terapia
Se sabe que hay terapias curativas como la cirugía y el iodo radioactivo y terapias paliativas no curativas como el manejo nutricional y las drogas antitiroideas, en la cual la sintomatología disminuye pero el nódulo tiroideo sigue en crecimiento. La probabilidad de malignización está estudiada y confirmada en el caso de las drogas antitiroideas y fisiopatológicamente debería ser similar en el caso de la terapia nutricional.
Han sido detalladas las complicaciones de la terapia nutricional en cuanto manejo del paciente, aunque aún falten estudios que avalen los efectos adversos a largo plazo. Debido a que son terapias no curativas, a la probalidad de malignización y a las complicaciones que respecta, dichos tratamientos no deberían ser indicados en primera instancia; teniendo en cuenta siempre el contexto que rodea al paciente y la disponibilidad de terapias curativas en el país.
Hoy en día los pacientes son diagnosticados de manera temprana, por lo tanto si la funcionalidad renal lo permite y para cumplir con el objetivo de establecer un estado eutiroideo total la terapia de elección es y debería ser a futuro sin dudarlo el iodo radioactivo, ya que en relación con la cirugía tiene muchas más ventajas.
Hipertiroidismo y enfermedad renal crónica
Tanto el exceso como el déficit de hormonas tiroideas están implicados en la funcionalidad renal aumentando o disminuyendo la filtración glomerular. En el caso del hipertiroidismo hay factores que enmascaran la funcionalidad renal disminuyendo la azotemia a corto plazo pero generando daño renal a largo plazo y progreso de la enfermedad renal crónica. La terapia instaurada sea cual fuese, no genera daño renal, si no que al disminuir la filtración glomerular desenmascara los signos enmascarados. Por lo cual la premisa que los gatos con enfermedad renal crónica no deberían tratarse queda anulada totalmente y el gran desafío es:
¿Como y cuándo debería tratarlos?
Factores del hipertiroidismo que enmascaran la ERC
- Aumento de la tasa de filtración glomerular.
- Poca masa muscular.
Factores del hipertiroidismo que contribuye a la ERC
- Hiperfiltración-hipertensión glomerular-proteinuria.
El desarrollo de la escala IRIS y el ensayo con metimazol toman lugar en este momento6.
Pacientes azotemicos IRIS 3-4 previos a tratamiento
Realizar ensayos con metimazol
- Comenzar a dar 1.25-2.5 mg cada 24 horas monitoreando cada 2 semanas y aumentando gradualmente hasta llevar a un estado eutiroideo.
- Evaluar parámetros renales definitivos y signología clínica relacionada con la azotemia 4 semanas post eutiroidismo.
De acuerdo a resultados
- Si al generar un estado eutiroideo se genera azotemia marcada y se altera la calidad de vida (hiporexia, vómitos, etc.) del paciente, será necesario tratar definitivamente con metimazol graduando dosis hasta lograr un equilibrio; a pesar de que el hipertiroidismo deteriore la función renal.
- Si al generar un estado eutiroideo no se genera azotemia marcada y no está alterada la calidad de vida del paciente, tratar con terapias definitivas el hipertiroidismo a pesar de la enfermedad renal crónica.
Evaluar siempre situaciones extremas para evaluar que tiene mejor pronóstico si la generación de síndrome urémico o la persistencia del hipertiroidismo.
Pacientes no azotemicos IRIS 1-2 previos a tratamiento
Ensayos con metimazol
- No es necesario, ya que el pronóstico es mejor tratando el hipertiroidismo, sin importar que empeore la tasa de filtración glomerular. Por lo tanto realizar terapias definitivas.
¿Hay forma de predecir que pacientes desarrollarán azotemia?
En el trabajo citado27 se llega a la conclusión que:
- Una densidad urinaria < 1035 tiene una sensibilidad de 92 % y una especificidad de 71 % para predecir azotemia.
- Un valor de SDMA > 14 ug/dl tiene una sensibilidad del 33 % pero una especificidad de 97.7 % para predecir azotemia.
Conclusiones finales
En este artículo se realizó una revisión actual del hipertiroidismo felino basado en la evidencia científica tanto descripta como de la experiencia del autor. Esta patología es cada día de mayor incidencia, los pacientes viven más y son diagnosticados a tiempo por lo cual la interpretación de los signos clínicos, de las pruebas diagnósticas, de las complicaciones y sobre todo la indicación terapéutica que más se adecue al paciente es de vital importancia para aumentar tanto la sobrevida como la calidad de vida de los pacientes.
Bibliografia
- Mark E. Peterson J.G. Johnson L.K. Andrews. Spontaneous hyperthyroidism in the cat. Conference: Proceedings of the American College of Veterinary Internal Medicine At: Seattle, Washington June 1979
- Peterson ME, Broome MR. Thyroid scintigraphy findings in 2096 cats with hyperthyroidism.Vet Radiol Ultrasound. 2015 Jan-Feb;56(1):84-95
- Peterson ME, Broome MR, Rishniw M. Prevalence and degree of thyroid pathology in hyperthyroid cats increases with disease duration: a cross-sectional analysis of 2096 cats referred for radioiodine therapy. J Feline Med Surg. 2016 Feb;18(2):92-10
- Peterson M. Hyperthyroidism in cats: what's causing this epidemic of thyroid disease and can we prevent it? J Feline Med Surg. 2012 Nov;14(11):804-18.
- Peterson M.E. and Broome M.R. Hyperthyroid Cats on Long-Term Medical Treatment Show a Progressive Increase in the Prevalence of Large Thyroid Tumors, Intrathoracic Thyroid Masses and Suspected Thyroid Carcinoma Conference Proceedings, (2012). ECVIM, Maastricht, Netherlands:
- Mark E. Peterson Treatment of hyperthyroidism and concurrent renal disease: is the "Tapazole trial" necessary? Conference: 29th Annual Veterinary Medical Forum (American College of Veterinary Internal Medicine) Volume: pp. 101-103.
- Gerber H, Peter H, Ferguson DC, Peterson ME. Etiopathology of feline toxic nodular goiter. Vet Clin North Am Small Anim Pract. 1994 May;24(3):541-65.
- M.L. Miller, M.E. Peterson, J.F. Randolph, M.R. Broome, G.D. Norsworthy, and M. Rishniw thyroid Cysts in Cats: A Retrospective Study of 40 Cases J Vet Intern Med. 2017 May-Jun; 31(3): 723–729.Published online 2017 Apr 6.
- Peterson M.E. Treatment of Severe, Unresponsive, or Recurrent Hyperthroidism in CatsConference Proceedings, (2011). American College of Veterinary Internal Medicine: p.104-106
- Hibbert A, Gruffydd-Jones T, Barrett EL, Day MJ and Harvey AM. Feline thyroid carcinoma: diagnosis and response to high-dose radioactive iodine treatment. J Feline Med Surg 2009; 11: 116–124.)
- Xenoulis PG, Zoran DL, Fosgate GT, Suchodolski JS, Steiner JM. Feline Exocrine Pancreatic Insufficiency: A Retrospective Study of 150 Cases. J Vet Intern Med. 2016 Nov;30(6):1790-1797
- R.J. Joseph, Peterson ME, Review and comparison of neuromuscular and central nervous system manifestations of hyperthyroidism in cats and humans. Progress in Veterinary Neurology Vol 3 No.4 1993
- Peterson ME, Kintzer PP, Cavanagh PG, Fox PR, Ferguson DC, Johnson GF, Becker DV. Feline hyperthyroidism: pretreatment clinical and laboratory evaluation of 131 cases. J Am Vet Med Assoc. 1983 Jul 1;183(1):103-10.
- Bond BR, Fox PR, Peterson ME, Skavaril RV. Echocardiographic findings in 103 cats with hyperthyroidism. J Am Vet Med Assoc. 1988 Jun 1;192(11):1546-9.
- Mark E. Peterson. Feline Hyperthyroidism. BSAVA Manual of canine and feline Endocrinology 4th edition 2012 Carmel T. Mooney and Mark E. Peterson.
- Berent AC, Drobatz KJ, Ziemer L, Johnson VS, Ward CR. Liver function in cats with hyperthyroidism before and after 131I therapy. J Vet Intern Med. 2007 Nov-Dec;21(6):1217-23
- Foster DJ, Thoday KL. Tissue sources of serum alkaline phosphatase in 34 hyperthyroid cats: a qualitative and quantitative study Res Vet Sci. 2000 Feb;68(1):89-94.
- Hoenig M, Ferguson DC. Impairment of glucose tolerance in hyperthyroid cats. Journal of Endocrinology 1989;121:249-251.
- Hoenig M, Peterson ME, Ferguson DC. Glucose tolerance and insulin secretion in spontaneously hyperthyroid cats. Research in Veterinary Science 1992;53:338-341.
- Scott-Moncrieff JC. Insulin resistance in cats. Vet Clin North Am Small Anim Pract. 2010 Mar;40(2):241-57
- Peterson ME, Guterl JN, Nichols R, Rishniw M. Evaluation of Serum Thyroid-Stimulating Hormone Concentration as a Diagnostic Test for Hyperthyroidism in Cats. J Vet Intern Med. 2015 Sep-Oct;29(5):1327-34.
- Rutland BE, Nachreiner RF, Kruger JM. Optimal testing for thyroid hormone concentration after treatment with methimazole in healthy and hyperthyroid cats. J Vet Intern Med. 2009 Sep-Oct;23(5):1025-30
- Peterson ME, Kintzer PP, Hurvitz AI. Methimazole treatment of 262 cats with hyperthyroidism. J Vet Intern Med. 1988 Jul-Sep;2(3):150-7.
- Peterson ME. Radioiodine treatment of hyperthyroidism. SClin Tech Small Anim Pract. 2006 Feb;21(1):34
- Mark E. Peterson. Nutritional Management of Feline Hyperthyroidism: What's the Best Diet to Feed these Cats? Animal Endocrine Clinic upload.2011
- Scott-Moncrieff JC, Heng HG, Weng HY, Dimeo D, Jones MD. Effect of a Limited Iodine Diet on Iodine Uptake by Thyroid Glands in Hyperthyroid Cats. J Vet Intern Med. 2015 Sep-Oct;29(5):1322-6
- Peterson ME, Varela FV, Rishniw M, Polzin DJ. Evaluation of Serum Symmetric Dimethylarginine Concentration as a Marker for Masked Chronic Kidney Disease in Cats With Hyperthyroidism. J Vet Intern Med. 2018 Jan;32(1):295-304
 by Multimédica
by Multimédica