Convulsiones secundarias a micosis sistémica en un perro con hiperadrenocorticismo en el Reino Unido
Resumen breve
Se describe el caso de una perra mestiza, hembra entera de 12 años, remitida por un inicio agudo de convulsiones en clúster. El examen neurológico localizó la lesión en prosencéfalo. Las pruebas laboratoriales evidenciaron leucocitosis neutrofílica leve, azotemia leve y marcada elevación de enzimas hepáticas. La ecografía abdominal mostró hígado difusamente hiperecoico, mucocele biliar y adrenomegalia unilateral, además de un nódulo esplénico cuya citología reveló inflamación mixta…Índice de contenidos
Resumen
Se describe el caso de una perra mestiza, hembra entera de 12 años, remitida por un inicio agudo de convulsiones en clúster. El examen neurológico localizó la lesión en prosencéfalo. Las pruebas laboratoriales evidenciaron leucocitosis neutrofílica leve, azotemia leve y marcada elevación de enzimas hepáticas. La ecografía abdominal mostró hígado difusamente hiperecoico, mucocele biliar y adrenomegalia unilateral, además de un nódulo esplénico cuya citología reveló inflamación mixta con hifas fúngicas pigmentadas. El test de supresión con dexametasona a dosis bajas fue compatible con hiperadrenocorticismo.
La resonancia magnética cerebral evidenció lesiones multifocales compatibles con encefalitis, y el análisis de líquido cefalorraquídeo mostró disociación albuminocitológica. Se instauró tratamiento con levetiracetam, dexametasona, fluconazol y terapia de soporte. Sin embargo, el paciente presentó deterioro neurológico progresivo y se realizó eutanasia humanitaria.
El estudio post mortem confirmó hepatitis y encefalitis granulomatosa necrotizante con abundantes hifas pigmentadas, compatibles con feohifomicosis sistémica, así como hiperplasia cortical adrenal bilateral.
Este caso destaca la importancia de considerar micosis sistémicas como diagnóstico diferencial en pacientes con signos neurológicos y alteraciones hepáticas, especialmente en presencia de posibles factores predisponentes como el hiperadrenocorticismo.
Introducción
Las micosis sistémicas son infrecuentes en medicina de pequeños animales. Se presenta el caso de una feohifomicosis sistémica en un perro en el Reino Unido, describiendo su presentación clínica, abordaje diagnóstico y evolución. El paciente se presentó con un clúster convulsivo y elevación de enzimas hepáticas, diagnosticándose finalmente encefalitis y hepatitis fúngicas.
Caso clínico
Se remitió una perra mestiza, hembra entera de 12 años, por un inicio agudo de convulsiones de 24 horas de evolución. Se determinó que el animal presentaba un clúster convulsivo. No existían antecedentes previos de crisis epilépticas según los tutores. Se describió una posible poliuria-polidipsia de aproximadamente seis meses de duración, aunque el consumo de agua no había sido cuantificado. El protocolo vacunal y de desparasitación estaba actualizado y no recibía medicación en el momento de la presentación. Ocho años antes había viajado a Alemania.
El examen físico general únicamente evidenció estado mental deprimido y deshidratación leve estimada en un 5%. El examen neurológico reveló déficits propioceptivos en las cuatro extremidades. La neurolocalización fue compatible con afectación del prosencéfalo.
Pruebas diagnósticas iniciales (Tabla 1)
- Hemograma: leucocitosis neutrofílica leve.
- Bioquímica sérica: azotemia leve, marcada elevación de ALT y FA, e hipercolesterolemia moderada.
Tabla 1. Alteraciones de la hematología y la bioquímica y resultados de los tiempos de coagulación y el ammonio.
| Prueba | Valor | Unidades | Rango de referencia |
|---|---|---|---|
| Neutrófilos | 18.77 | ×10^9/L | 6.0–15.0 ×10^9/L |
| Urea | 17.7 | mmol/L | 2.7–7.4 mmol/L |
| Creatinina | 154 | µmol/L | 40–145 µmol/L |
| Alanina aminotransferasa (ALT) | 905 | U/L | 13–88 U/L |
| Fosfatasa alcalina (ALP) | 2836 | U/L | 14–105 U/L |
| Gamma-glutamiltransferasa (GGT) | 240 | U/L | 0–10 U/L |
| Ácidos biliares pre | 113 | µmol/L | 0–10 µmol/L |
| Colesterol | 10.1 | mmol/L | 3.8–7 mmol/L |
| Triglicéridos | 1.2 | mmol/L | 0.56–1.14 mmol/L |
| Bilirrubina total | 5 | µmol/L | 0–16 µmol/L |
| Tiempo de protrombina (PT) | 8.5 | s | 7–12 s |
| Amonio | 54 | s | 15–25 s |
Pruebas adicionales (ver Tabla 1)
- Amonio: dentro del rango de referencia.
- Tiempos de coagulación (TP y TTPa): dentro de los valores normales.
Ecografía abdominal
Se realizó ecografía abdominal ante la elevación de enzimas hepáticas y la sospecha de posible origen extracraneal de las convulsiones. El estudio, realizado por un especialista europeo en diagnóstico por imagen, evidenció:
- Hígado difusamente hiperecoico.
- Mucocele biliar no obstructivo.
- Nódulo esplénico hiperecoico, bien delimitado, de 1.4 × 1.1 cm (Figura 1).
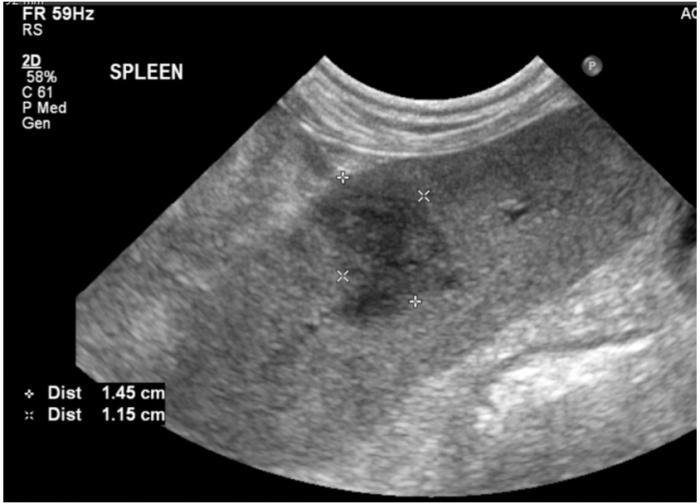
- Glándula adrenal izquierda aumentada de tamaño (0,96 cm) con nódulo hipoecoico craneal de 1.2 cm
Durante el procedimiento se realizó:
- Cistocentesis: densidad urinaria 1,018; sedimento inactivo; tira de orina con todos los valores negativos.
- Citología hepática (PAAF): inflamación mixta con colestasis.
- Citología esplénica (PAAF): inflamación mixta con abundantes hifas fúngicas, tanto extracelulares como intracelulares (macrófagos) (Figura 2).
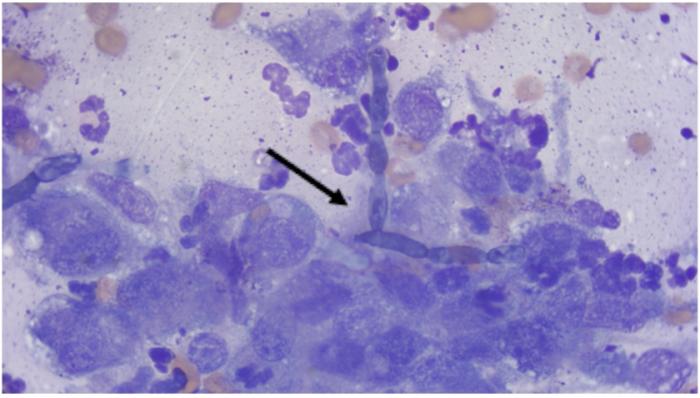
- Cultivo esplénico: negativo.
Primer diagnóstico
Se concluyó la presencia de infección fúngica sistémica responsable de la alteración hepática. No obstante, la relación causal directa con las convulsiones no pudo establecerse en ese momento.
Diagnósticos diferenciales de las convulsiones
- Encefalitis fúngica (como parte de micosis sistémica).
- Encefalopatía hepática secundaria a hepatitis fúngica.
- Enfermedad neurológica concomitante no relacionada.
Evaluación endocrina
Dado que las micosis sistémicas suelen afectar a animales inmunocomprometidos, junto con la presencia de poliuria-polidipsia y adrenomegalia, se realizó un test de supresión con dexametasona a dosis bajas, compatible con hiperadrenocorticismo (Tabla 2). No se pudo diferenciar entre tipos de hiperadrenocorticismo (pituitario o adrenal).
Tabla 2. Resultados del test de supresión con dexametasona a dosis bajas.
| Prueba | Valor | Unidades | Rango de referencia |
|---|---|---|---|
| Cortisol basal | 475 | nmol/L | 27.5–125 |
| Cortisol post 4 h | 444 | nmol/L | Igual/menos de 40 |
| Cortisol post 8 h | 502 | nmol/L | Igual/menos de 40 |
Resonancia magnética (RM) cerebral
Se realizó resonancia magnética (Hitachi Lucent Aperto, 0.4T), observándose:
- Hiperintensidad en T2 e hipointensidad en T1 en sustancia blanca de giros del cíngulo y cápsulas internas (más marcada en el lado derecho).
- Áreas hiperintensas parcheadas en T2 en tronco encefálico.
- Realce multifocal tras contraste en sustancia blanca subcortical, lóbulos occipital y frontal izquierdos.
- Leve efecto masa con desplazamiento del falx cerebri hacia la izquierda y compresión dorsal leve del ventrículo lateral derecho.
Los hallazgos fueron compatibles con encefalitis fúngica.
Análisis líquido cefalorraquídeo
El análisis (cisterna magna) mostró disociación albuminocitológica.
Tratamiento
Durante la hospitalización se instauró:
- Levetiracetam (20 mg/kg IV TID).
- Fluidoterapia intravenosa.
- Dexametasona (0.2 mg/kg IV SID).
- Manitol (0.25 mg/kg IV) el día del ingreso.
- Fluconazol (3.5 mg/kg PO BID).
- Lactulosa vía rectal como soporte ante posible encefalopatía hepática.
No se observó mejoría clínica en los siete días siguientes. El paciente presentó deterioro neurológico progresivo hasta estado estuporoso. Dado el pronóstico desfavorable, se optó por eutanasia humanitaria.
Estudio post mortem
- Hepatitis granulomatosa con abundantes hifas fúngicas pigmentadas (Figura 3).
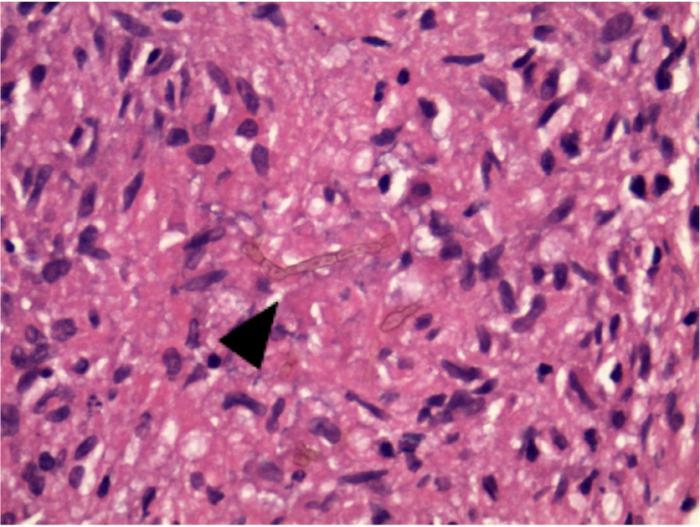
- Encefalitis granulomatosa necrotizante multifocal con hifas intralesionales (Figura 4).
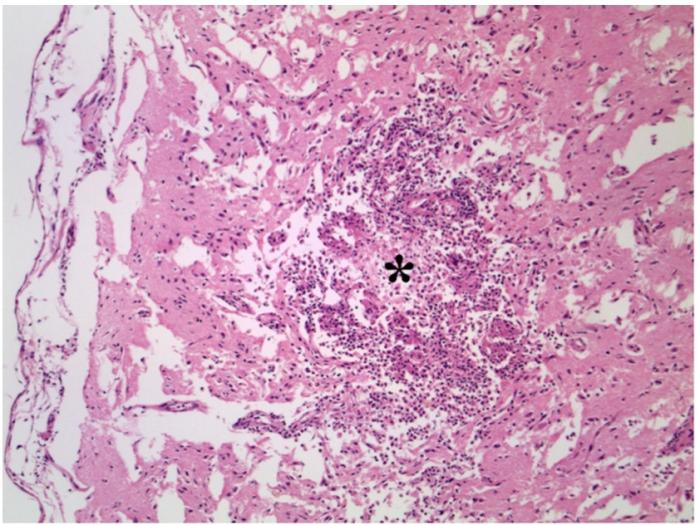
- Hiperplasia cortical adrenal bilateral.
- Mucocele biliar.
Los cultivos fúngicos fueron negativos, pero la morfología histológica fue altamente compatible con feohifomicosis.
Discusión
La hipótesis final fue que el hiperadrenocorticismo subyacente generó inmunosupresión, predisponiendo al desarrollo de feohifomicosis sistémica con afectación hepática y encefálica.
El estudio post mortem confirmo que el encéfalo estaba afectado por la infección fúngica y la presencia de inflamación asociada (encefalitis granulomatosa). Esta encefalitis granulomatosa fue considerada la principal causa de las convulsiones. Desde un punto de vista histológico, las infecciones micóticas del sistema nervioso central suelen causar este tipo de inflamación1.
Aunque no puede descartarse completamente un componente de encefalopatía hepática, la concentración normal de amonio hizo este diagnóstico menos probable. Sin embargo, no se puede descartar definitivamente que los signos neurológicos no fueran, parcialmente, debidos a un componente de encefalopatía hepática. Un amonio dentro del rango de referencia no descarta completamente esta alteración metabólica, pero la hace menos probable. Hay muchas otras substancias que participan en la patofisiología de la encefalopatía hepática como las benzodiazepinas y glutamato. No obstante, el hecho de que el amonio fuera normal es el motivo por el cual se procedió con resonancia magnética del cerebro.
La feohifomicosis comprende las infecciones causadas por hongos dematiáceos pigmentados. El término phaeo deriva del griego antiguo y significa “oscuro”, en referencia a la coloración característica producida por la melanina presente en la pared celular de las hifas o levaduras. Entre los géneros implicados se incluyen Alternaria, Aureobasidium, Bipolaris y Curvularia, entre otros1.
La infección suele producirse por inoculación cutánea a partir del ambiente y puede manifestarse como enfermedad cutánea, subcutánea, cerebral o diseminada. La afectación del sistema nervioso central puede ocurrir por extensión local (por ejemplo, desde la cavidad nasal) o por diseminación hematógena. Tradicionalmente, esta micosis se ha descrito con mayor frecuencia en regiones con climas cálidos y húmedos, como Oriente Medio y el sudeste asiático; sin embargo, actualmente se reconoce su distribución global1.
En animales inmunocompetentes, las manifestaciones clínicas más habituales son lesiones cutáneas localizadas, especialmente en orejas, dígitos y plano nasal. Estas lesiones suelen presentarse como nódulos o masas pigmentadas, por lo que el melanoma constituye un diagnóstico diferencial relevante. Las lesiones pueden ser localmente invasivas y afectar linfonodos regionales. En pacientes inmunosuprimidos, aunque las lesiones cutáneas también son frecuentes, la afectación sistémica es más común1. Los signos neurológicos pueden deberse tanto al efecto masa de granulomas fúngicos como a la respuesta inflamatoria asociada a la invasión tisular2.
Ante el diagnóstico de una micosis sistémica, es fundamental investigar posibles factores predisponentes, como tratamientos inmunosupresores o enfermedades concomitantes. No obstante, estas infecciones también se han descrito en animales aparentemente inmunocompetentes1.
El uso de ciclosporina se ha señalado en la literatura como uno de los factores predisponentes más frecuentes. Se han publicado casos de infecciones fúngicas sistémicas en perros tratados con este fármaco para dermatitis atópica, incluyendo infecciones por Byssochlamys spp. YExophiala dermatitidis3,4.
Entre las enfermedades predisponentes se incluye el hiperadrenocorticismo, sospechado en el presente caso. Aunque el test de supresión con dexametasona a dosis bajas puede arrojar resultados falsamente positivos5, el contexto clínico hacía esta hipótesis plausible. El hiperadrenocorticismo se asocia con un mayor riesgo de infecciones, habiéndose descrito prevalencias de infecciones urinarias del 30–50 % en estos pacientes6. Los mecanismos implicados incluyen alteraciones inmunológicas inducidas por el exceso de glucocorticoides y factores mecánicos como la combinación de poliuria y disminución del tono vesical, favoreciendo la retención urinaria. Las piodermas son igualmente frecuentes, y aproximadamente un 10 % de los casos de demodicosis en adultos se han relacionado con esta endocrinopatía5,6. Asimismo, el hiperadrenocorticismo podría explicar la poliuria y polidipsia descritas por los tutores.
Las alteraciones hematológicas y bioquímicas en la feohifomicosis suelen ser inespecíficas y pueden reflejar inflamación sistémica o enfermedades concomitantes. El tipo y la magnitud de las alteraciones dependen de los órganos afectados. El urianálisis puede ser normal1,2.
En el presente caso, la ecografía abdominal evidenció un mucocele biliar. El hiperadrenocorticismo se ha asociado con el desarrollo de mucoceles debido a la influencia de los glucocorticoides sobre la composición biliar. Aunque no puede determinarse con certeza el papel del mucocele en la elevación de enzimas hepáticas, se consideró un hallazgo incidental, atribuyéndose principalmente las alteraciones hepáticas a la hepatitis fúngica.
Las pruebas de imagen avanzadas, como la resonancia magnética o la tomografía computarizada, pueden revelar lesiones focales o multifocales con realce tras contraste cuando existe afectación del sistema nervioso central. El análisis del líquido cefalorraquídeo suele mostrar pleocitosis mixta y/o disociación albuminocitológica2.
Desde el punto de vista citológico e histológico, se observan hifas septadas, de morfología irregular y diámetro variable, con paredes celulares pigmentadas como característica distintiva. En ocasiones puede emplearse la tinción de Fontana-Masson para confirmar la presencia de melanina. El diagnóstico definitivo requiere aislamiento mediante cultivo y/o técnicas moleculares como PCR, aunque pueden obtenerse resultados negativos incluso en casos confirmados histológicamente1.
El tratamiento de las infecciones por hongos dematiáceos es complejo y el pronóstico reservado1. La melanina actúa como factor de virulencia y puede contribuir a la resistencia terapéutica. En lesiones cutáneas localizadas, se recomienda la escisión quirúrgica con márgenes amplios seguida de tratamiento antifúngico prolongado (3–6 meses). En casos seleccionados, puede considerarse la resección quirúrgica de granulomas intracraneales2. En el presente caso, la afectación multifocal descartó la opción quirúrgica.
El tratamiento médico aislado suele tener eficacia limitada en infecciones diseminadas, ya que la mayoría de antifúngicos son fungistáticos1. Fluconazol y flucitosina presentan buena penetración en el sistema nervioso central2, motivo por el cual se instauró fluconazol. No obstante, la información disponible sobre meningoencefalitis por hongos dematiáceos es escasa, y el pronóstico suele considerarse grave a fatal para feohifomicosis y Aspergillus2. En este paciente se produjo un rápido deterioro neurológico, y considerando el pronóstico desfavorable, se optó por eutanasia humanitaria.
No se ha demostrado transmisión entre mamíferos. La infección en humanos suele deberse a inoculación ambiental. Se recomiendan medidas básicas de bioseguridad, incluyendo el uso de guantes y precaución en la manipulación de agujas1.
Conclusión
Este caso amplía la literatura sobre feohifomicosis sistémica en perros y destaca la importancia de considerar micosis sistémicas en pacientes con signos neurológicos y alteraciones hepáticas, especialmente cuando existen factores predisponentes como hiperadrenocorticismo. Asimismo, subraya la necesidad de un abordaje diagnóstico integral y la consideración de enfermedades endocrinas como posibles factores facilitadores de infecciones oportunistas.
Bibliografía
- Grooters AM. Miscellaneous Fungal Diseases. Greene’s Infectious Diseases of the Dog and the Cat. 2023.
- Dewey CW. Encephalopathies: disorders of the brain. A practical guide to canine & feline neurology. Iowa, 2016.
- Atencia, S., Papakonstantinou, S., Leggett, B.et al.Systemic fungal infection in a dog: a unique case in Ireland.Ir Vet J., 2014.
- Giri D.K, Sims W.P, Sura R, et al. Cerebral and renal phaeohyphomycosis in a dog infected with Bipolaris species . Vet Pathol., 2011.
- Behrend, E. Canine Hyperadrenocorticism. Canine & Feline Endocrinology. StLouis, 2015.
- Hoffman JM,Lourenço BN,Promislow DEL, et al.Canine hyperadrenocorticism associations with signalment, selected comorbidities and mortality within North American veterinary teaching hospitals.J Small Anim Pract2018.
 by Multimédica
by Multimédica