Ovariohisterectomía por piómetra
Resumen breve
La piómetra es una patología quirúrgica frecuente, que se puede presentar con muy diversos cuadros clínicos, desde leves a muy complejos, pudiendo acabar incluso en septicemia. El riesgo de perforación uterina empeora considerablemente el cuadro, siendo mucho más frecuente con cuadros de piómetra cerrada, presentándose con cuadros clínicos muy deteriorados y siendo una urgencia quirúrgica real.Índice de contenidos
Introducción
La piómetra es una patología quirúrgica frecuente, que se puede presentar con muy diversos cuadros clínicos, desde leves a muy complejos, pudiendo acabar incluso en septicemia. El riesgo de perforación uterina empeora considerablemente el cuadro, siendo mucho más frecuente con cuadros de piómetra cerrada, presentándose con cuadros clínicos muy deteriorados y siendo una urgencia quirúrgica real.
Una evaluación prequirúrgica detallada y una optimización a objetivos son las mejores estrategias para afrontar este tipo de pacientes, ya que en ocasiones se puede conseguir una mejora clínica que mejore los resultados quirúrgicos. A este respecto, hay que recordar que idealmente durante la anestesia no se debe estabilizar a los pacientes, siendo más eficaz la optimización previa.
Descripción del caso clínico
Lola se fue remitida al servicio de cirugía con diagnóstico previo de piómetra.
Los hallazgos más reseñables de la evaluación preanestésica se reseñan en la Tabla 1. Según los análisis, anamnesis y exploración se determina una valoración de riesgo anestésico ASA 4.
En ecografía no se valora peritonitis en el momento del ingreso, por lo que se decide optimizar el paciente unas horas antes de la anestesia, administrándose fluidoterapia a base de cristaloides (Ringer lactato), con un bolo inicial de 10 ml/kg en 20 min, seguido de 5 ml/kg/h hasta el momento de la cirugía, la cual se programa para 6 h después. En este tiempo también se administró cefalexina 25 mg/kg IV, paracetamol 15 mg/kg IV administrado en 15 minutos y se inició una infusión de lidocaína (2 mg/kg/h) con una dosis previa de carga administrada en 10 min una vez acabada la resucitación inicial de la volemia (Figura 1).
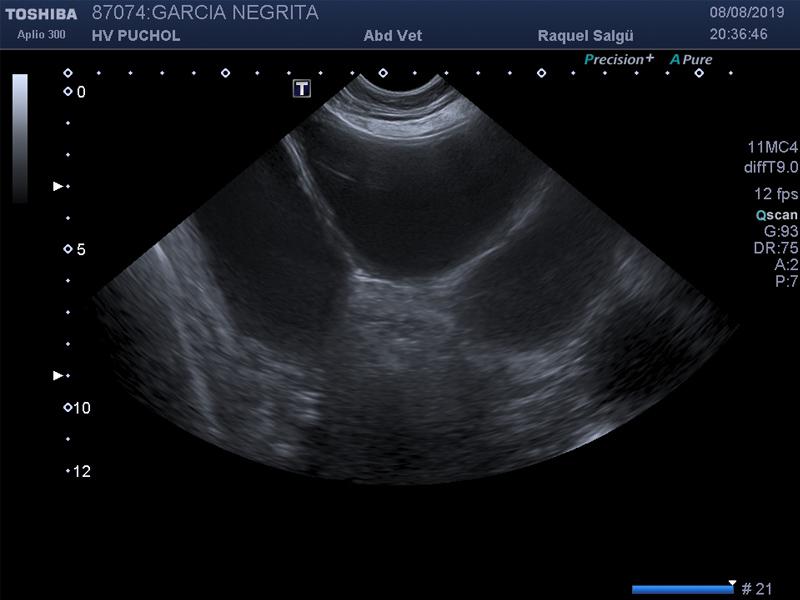
Durante el periodo de optimización se monitorizaron parámetros hemodinámicos, con una mejora en cuanto a la presión arterial y frecuencia cardiaca, mejorando también el estado anímico.
Plan anestésico y monitorización
En la evaluación anestésica previa a la premedicación, Lola presenta mejores parámetros que a su llegada: 96 lpm, PAS 118 y 25 rpm con buen color de mucosas y buena auscultación cardiopulmonar.
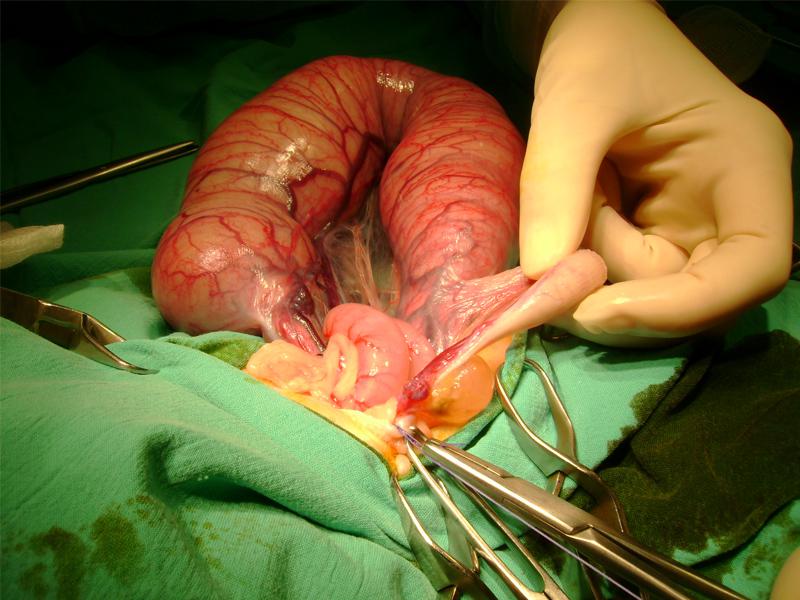
Se mantiene la infusión de lidocaína y se procede a la premedicación con metadona 0.2 mg/kg IV lento (3 minutos). A los 10 minutos de esta, Lola presenta un leve estado de sedación y se procede a la preoxigenación mediante mascarilla y alto flujo de gas fresco (O2 al 100 % y 3 l de flujo) durante unos minutos y monitorización mediante ECG, tras los cuales se administra como inducción una combinación de alfaxalona (1 mg/kg) combinado con fentanilo (5 mcg/kg) hasta conseguir una intubación cómoda para el paciente, conectándose acto seguido a la máquina de anestesia mediante un circuito circular con reinhalación manteniendo un flujo de gas fresco de 2 l, iniciando la vaporización de isofluorano. Tras la intubación se preparó la zona quirúrgica con el paciente en decúbito lateral el mayor tiempo posible, situándolo lentamente en decúbito dorsal y vigilando ya las presiones por si hubiera algún episodio de hipotensión posicional (Figura 2).
La monitorización intraoperatoria se realizó mediante ECG, pulsioxímetro y pletismograma, CO2, presión arterial (invasiva y oscilométrica) y temperatura. Como protocolo analgésico se preparó una dosis de fentanilo (2 mcg/kg) y ketamina (0.25 mg/kg) para administrar previo a la tracción del pedículo ovárico.
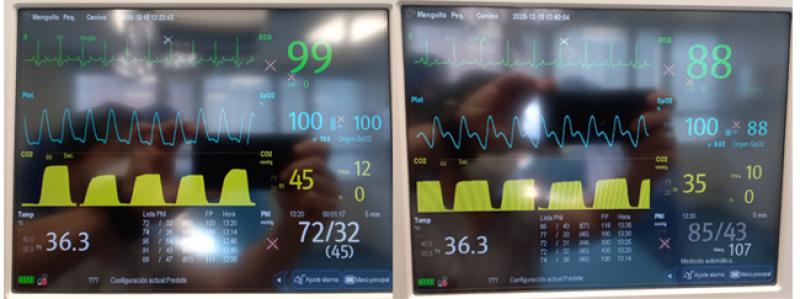
Al inicio del procedimiento se detectó una presión arterial baja, con PAM de 52 mmHg. Tras valorar el plano de hipnosis y el resto de la monitorización, se valoró también una ligera variabilidad y morfología de vasodilatación en la curva de pletismografía por lo que se administró un bolo de Ringer Lactato a 5 ml/kg en 10 minutos, obteniendo una leve mejoría (PAM 55 mmHg) por lo que se optó acto seguido a la administración de noradrenalina con una dosis inicial de 0.5 mcg/kg/min, con mejoría significativa, consiguiendo una PAM 70 mmHg.
En prevención de la respuesta simpática se administró la dosis de fentanilo y ketamina que estaba preparada, con un descenso del 10 % de la dosis de isofluorano.
El resto del procedimiento se continuó sin más complicaciones.
Recuperación y plan analgésico posoperatorio
Durante el posoperatorio se mantuvo la analgesia con lidocaína a 2 mg/kg/h durante las primeras 24 h y posteriormente se redujo a 1.5 mg/kg/h. También se continuó con la administración de paracetamol cada 8 h, vía intravenosa y en administración lenta (15 minutos). Se estableció como analgesia de rescate metadona 0.15 mg/kg en el caso de detectar dolor, y para monitorizarlo, se pautó un seguimiento posoperatorio mediante la escala abreviada de Glasgow cada 2-3 h. Esta analgesia de rescate no fue necesaria durante la estancia en el hospital.
La analítica en el momento del alta había mejorado considerablemente, quedando únicamente un aumento de la creatinina, por lo que se decidió no prescribir AINEs y dar el alta con paracetamol y tramadol como analgesia ambulatoria, con revisión en las primeras 24 h tras el alta para poder evaluar el estado general y la calidad de la analgesia prescrita, indicando al tutor comportamientos indicativos de dolor por si esta no era suficiente.
En la primera revisión tras el alta no fue necesario añadir más analgesia y se mantuvo durante 7 días, con una recuperación satisfactoria.
Discusión
En diferentes estudios, el riesgo de mortalidad anestésica se asocia al estado del paciente. Mientras que para una ovariohisterectomía rutinaria el riesgo de muerte es de un 0.009 %, cuando la valoración de riesgo anestésico aumenta, la probabilidad de muerte en las siguientes 48 h también aumenta1. Con estos datos parece lógico que la optimización previa pueda ayudar a disminuir el riesgo de muerte perioperatoria.
En el caso de la piómetra, la valoración preanestésica es fundamental ya que se puede presentar con muy diferentes cuadros clínicos, desde los más leves, donde la polidipsia y poliuria pueden ser los únicos síntomas, hasta pacientes en shock séptico de rápida evolución, asociado muchas veces a las endotoxinas de Escherichia coli, principal causante de la sintomatología y asociado a la pérdida de acción de la hormona antidiurética (ADH) en el paciente, provocando la sintomatología inicial, con imposibilidad de concentración urinaria e incremento de la diuresis y la consiguiente hipovolemia, siendo este cuadro el responsable del daño renal asociado, que se puede cronificar si se produce un daño tubular permanente2. Esta valoración pasará por una analítica lo más completa posible:
- Hematología (serie blanca y serie roja, ya que es frecuente que aparezcan cuadros de anemia asociado a la piómetra)
- Valores renales (mínimo creatinina)
- Albumina (puede estar disminuida)
- Glucosa (puede estar disminuida en pacientes sépticos o aumentada en casos de diabetes asociada a progesterona)
- Iones (alterados por anorexia, cuadro renal y vómitos si existen)
- Gasometría sanguínea (aquí los cuadros pueden ser variados, con frecuencia se presentan mixtos, con acidosis asociada al aumento de lactato por la hipovolemia y alcalosis hipoclorémica en el caso de anorexia mantenida y/o vómitos).
En función de esta valoración preanestésica, la determinación de la urgencia quirúrgica suele estar referida a la presencia de peritonitis, que pueda determinar una rotura uterina o zona perforada muy próxima a la rotura. La optimización con fluidoterapia a objetivos con reposición de iones es ideal. En el caso de pacientes anémicos, este sería el momento ideal para realizar la transfusión. Igualmente, en pacientes hiperglicémicos, el control con insulina es también importante para disminuir el riesgo de cetoacidosis, teniendo en cuenta que en muchos casos el problema remite tras la ovariohisterectomía, por lo que es necesario un control estricto de la glucosa posoperatoria para evitar hipoglucemias yatrogénicas.
Aunque los estudios en veterinaria son aún escasos, la administración temprana de antibióticos de amplio espectro parece que puede disminuir la mortalidad3, por eso se incluyó en el protocolo de optimización previa.
En el triage inicial se valoró también un dolor moderado en la palpación abdominal, por lo que se incluyeron el paracetamol y la lidocaína, iniciando el protocolo analgésico de forma temprana y con un enfoque multimodal. Existen diferentes estudios del uso de paracetamol como analgésico posoperatorio, dando unos resultados en algunos de ellos incluso comparables a los AINES, además de presentar efecto antipirético4.
La lidocaína ha demostrado efectos analgésicos por administración intravenosa, principalmente en cuadros de dolor neuropático, visceral y también en protocolos de analgesia multimodal, en combinación con opiáceos, ketamina e incluso α2 agonistas5.
El mecanismo de acción propuesto en este caso va más allá del bloqueo de los canales de sodio como se pensaba tradicionalmente y se cree que además hay interacción con diferentes tipos de neuronas en el asta dorsal de la médula (muscarínicas/dopaminérgicas/K/nicotínicas). Además del efecto analgésico, se han referenciado otros efectos beneficiosos tras la administración por esta vía.
| Tabla 1. Otros efectos beneficiosos de la lidocaína IV (modificado de Baussier 2018)6. |
|
Durante el procedimiento se presentó un episodio de hipotensión. Valorando el resto de las variables hemodinámicas se observó una curva de pletismograma y de presión arterial invasiva compatible con vasodilatación sin detectarse signos compatibles con hipovolemia, por lo que tras valorar el estado de hipnosis y no pudiendo disminuir la concentración de isofluorano y siendo un paciente séptico se decidió el uso de vasopresores, siendo la noradrenalina la opción elegida. No está claro cuál es el escenario ideal para la elección de uno u otro vasopresor7, pero sí está demostrado que el manejo de la hipotensión debe de ser razonado y ordenado, estableciendo el tratamiento o tratamientos ideales en función de las causas y prioridades, ya sea fluidos, vasopresores o inótropos o la suma de algunos de ellos. En el caso del shock séptico según las guías de medicina humana, la noradrenalina será la elección de primera línea3. En relación a la hipotensión, el manejo posicional del paciente es importante ya que cambios bruscos de posición y sobre todo la colocación en decúbito dorsal de pacientes con piómetras cerradas de gran volumen (u otras situaciones en las que haya grandes volúmenes abdominales, como hembras gestantes o masas abdominales) ya que el propio peso puede disminuir el gasto cardiaco por diminución del volumen de precarga causado por la compresión de los grandes vasos abdominales (cava principalmente) (Figuras 3 y 4).
Como apoyo analgésico en este caso se optó por la administración de una dosis baja y muy lenta de fentanilo y ketamina previa a la tracción y exteriorización del útero. Este es otro momento delicado por la posibilidad de aparición de un reflejo vaso-vagal, con bradicardia asociada cuyo tratamiento será la administración de atropina (0.02-0.04 mg/kg IV).Otras opciones analgésicas para la realización de OVH han sido discutidas en el caso de Peppa. En esta situación concreta, y con la situación de sepsis del paciente, la realización de la epidural sería preferible evitarla, tanto por la sepsis como por la posibilidad de hipotensión asociada a la propia técnica. Respecto a otras posibles técnicas de anestesia/analgesia locorregional, hay que tener en cuenta el riesgo de sobredosificación que puede aparecer por el uso de la lidocaína intravenosa. Hasta estudios específicos en veterinaria, parece razonable seguir las recomendaciones de humana en las que se aconsejan que entre el uso de una infusión continua de lidocaína y la realización de un bloqueo y viceversa, deberían de pasar por lo menos 3-4 h para evitar efectos tóxicos sumatorios en el caso de usar bupivacaína en la realización del bloqueo8.Como analgesia posoperatoria se mantuvo la lidocaína en infusión continua y paracetamol, pautando valoraciones de dolor dentro de la monitorización posoperatoria. Como rescate analgésico se pautó metadona, aunque otra opción también interesante en estas situaciones puede ser la combinación de ketamina y lidocaína en infusión continua, ya que se completan respecto a la actividad analgésica y en el caso de la ketamina, la acción sobre los receptores NMDA ha demostrado una actividad antihiperalgésica con menor consumo de opioides en el posoperatorio, aunque los estudios en veterinaria son aún escasos, pero prometedores9. La no inclusión de AINES dentro del protocolo tiene como objetivo disminuir el daño renal que puede aparecer en pacientes con alteración renal previa y que, aunque no la tengan, por su estado, puedan desarrollarla durante el perioperatorio.
Bibliografía
- Shoop-Worrall SJ, O'Neill DG, Viscasillas J, Brodbelt DC. Mortality related to general anaesthesia and sedation in dogs under UK primary veterinary care. Vet Anaesth Analg. 2022 Jun 30: S1467-2987(22)00101-5. doi: 10.1016/j.vaa.2022.03.006.
- Hagman R. Pyometra in Small Animals. Vet Clin North Am Small Anim Pract. 2018 Jul; 48(4):639-661. doi: 10.1016/j.cvsm.2018.03.001.
- Evans L, Rhodes A, Alhazzani W, Antonelli M, Coopersmith CM, French C, Machado FR, Mcintyre L, Ostermann M, Prescott HC, Schorr C, Simpson S, Wiersinga WJ, Alshamsi F, Angus DC, Arabi Y, Azevedo L, Beale R, Beilman G, Belley-Cote E, Burry L, Cecconi M, Centofanti J, Coz Yataco A, De Waele J, Dellinger RP, Doi K, Du B, Estenssoro E, Ferrer R, Gomersall C, Hodgson C, Møller MH, Iwashyna T, Jacob S, Kleinpell R, Klompas M, Koh Y, Kumar A, Kwizera A, Lobo S, Masur H, McGloughlin S, Mehta S, Mehta Y, Mer M, Nunnally M, Oczkowski S, Osborn T, Papathanassoglou E, Perner A, Puskarich M, Roberts J, Schweickert W, Seckel M, Sevransky J, Sprung CL, Welte T, Zimmerman J, Levy M. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021. Intensive Care Med. 2021 Nov;47(11):1181-1247. doi: 10.1007/s00134-021-06506-y.
- Hernández-Avalos I, Valverde A, Ibancovichi-Camarillo JA, Sánchez-Aparicio P, Recillas-Morales S, Osorio-Avalos J, Rodríguez-Velázquez D, Miranda-Cortés AE. Clinical evaluation of postoperative analgesia, cardiorespiratory parameters and changes in liver and renal function tests of paracetamol compared to meloxicam and carprofen in dogs undergoing ovariohysterectomy. PLoS One. 2020 Feb 14;15(2):e0223697. doi: 10.1371/journal.pone.0223697.
- Vullo C, Tambella AM, Falcone A, Marino G, Catone G. Constant Rate Infusion of Lidocaine, Tumescent Anesthesia and Their Combination in Dogs Undergoing Unilateral Mastectomy. Animals (Basel). 2021 Apr 29;11(5):1280. doi: 10.3390/ani11051280.
- Beaussier M, Delbos A, Maurice-Szamburski A, Ecoffey C, Mercadal L. Perioperative Use of Intravenous Lidocaine. Drugs. 2018 Aug;78(12):1229-1246. doi: 10.1007/s40265-018-0955-x.
- Silverstein, D. C. & Beer, K. A. S. Controversies regarding choice of vasopressor therapy for management of septic shock in animals. J Vet Emerg Crit Car 25, 48–54 (2015).
- Foo I, Macfarlane AJR, Srivastava D, Bhaskar A, Barker H, Knaggs R, Eipe N, Smith AF. The use of intravenous lidocaine for postoperative pain and recovery: international consensus statement on efficacy and safety. Anaesthesia. 2021 Feb;76(2):238-250. doi: 10.1111/anae.15270.
- Kaka U, Saifullah B, Abubakar AA, Goh YM, Fakurazi S, Kaka A, Behan AA, Ebrahimi M, Chen HC. Serum concentration of ketamine and antinociceptive effects of ketamine and ketamine-lidocaine infusions in conscious dogs. BMC Vet Res. 2016 Sep
- 12(1):198. doi: 10.1186/s12917-016-0815-4.
 by Multimédica
by Multimédica