Manejo anestésico y cuidados del perro y gato con aumento de presión intracraneal
Resumen breve
Los pacientes con aumento de presión intracraneal (PIC) pueden requerir sedación o incluso anestesia general, bien para la realización de pruebas de diagnóstico por imagen, bien para la resolución quirúrgica del problema. La anestesia de estos pacientes es compleja y requiere un adecuado conocimiento de la fisiopatología y consecuencias clínicas de dicho aumento de PIC. El objetivo de este trabajo es realizar una visión global del manejo anestésico de pacientes con aumento de PIC, lo que…Índice de contenidos
Resumen
Los pacientes con aumento de presión intracraneal (PIC) pueden requerir sedación o incluso anestesia general, bien para la realización de pruebas de diagnóstico por imagen, bien para la resolución quirúrgica del problema. La anestesia de estos pacientes es compleja y requiere un adecuado conocimiento de la fisiopatología y consecuencias clínicas de dicho aumento de PIC. El objetivo de este trabajo es realizar una visión global del manejo anestésico de pacientes con aumento de PIC, lo que incluye conocer: los efectos que los diferentes fármacos anestésicos pueden tener sobre el flujo sanguíneo cerebral (FSC), el metabolismo cerebral y la PIC, las diferentes maniobras para evitar aumentos bruscos de la PIC, las principales complicaciones que pueden darse durante la anestesia y cirugía y como anticiparnos a ellas, así como los cuidados posoperatorios.
Introducción
El aumento de la presión intracraneal (PIC) constituye una de las complicaciones más críticas en pacientes veterinarios con patologías neurológicas. Ya sea secundario a tumores, hematomas, hidrocefalia o procesos inflamatorios, un incremento sostenido de la PIC compromete la perfusión cerebral y puede conducir a isquemia, deterioro neurológico progresivo y potencialmente herniación cerebral, un evento que conlleva un riesgo vital sustancial1, 2. Este escenario cobra especial relevancia en el contexto anestésico, dado que muchos fármacos y maniobras pueden modificar el flujo sanguíneo cerebral (FSC) y con ello la PIC, y porque las decisiones intra- y perioperatorias afectan directamente la evolución neurológica1, 3.
Diferentes estudios han demostrado que la hipertensión intracraneal no sólo refleja la gravedad del proceso subyacente, sino que influye de forma determinante en el pronóstico. Por ejemplo, en perros sometidos a cirugía de tumores cerebrales, la presencia de PIC elevada durante la recuperación anestésica se ha asociado con mayor riesgo de mortalidad y complicaciones1, 2. Además, las complicaciones postquirúrgicas (convulsiones, deterioro neurológico agudo, neumonía por aspiración y alteraciones sistémicas) son determinantes en la supervivencia y el tiempo de hospitalización3-5.
El objetivo de este trabajo es presentar una revisión aplicada del manejo anestésico en pequeños animales con aumento de la PIC, integrando fisiología, farmacología y evidencia clínica contemporánea.
Fisiología del flujo sanguíneo cerebral (FSC) y la presión intracraneal (PIC)
El FSC depende de la presión de perfusión cerebral (PPC), definida como la diferencia entre la presión arterial media (PAM) y la PIC.
PPC= PAM-PIC
Según la doctrina de Monroe-Kelly, la rigidez del cráneo y el volumen intracraneal fijo implican que cualquier incremento en tejidos, sangre o LCR puede traducirse en elevación de la PIC1, 2 Los mecanismos compensatorios (redistribución de LCR, salida venosa, etc.) amortiguan cambios pequeños, pero al superarse estos mecanismos, la PIC aumentará de forma exponencial con mínima variación de volumen (Figura 1).
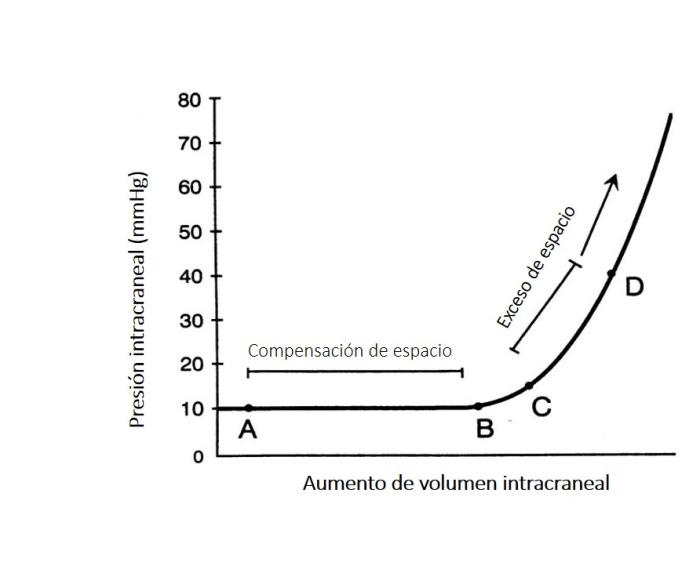
En pacientes con tumores intracraneales la relación entre volumen tumoral, edema peritumoral y PIC es crítica; la PPC insuficiente conduce a descompensación neurológica rápida. Si la PIC sube, la PPC baja, el cerebro recibe menos sangre y oxígeno produciendo una isquemia.
Para evitar la isquemia cerebral, el cuerpo responde con hipertensión sistémica, que a su vez general bradicardia refleja mediada por reflejo barorreceptor; éste reflejo puede acompañarse también de respiración irregular o paradójica. El conjunto de hipertensión sistémica, bradicardia y alteración del patrón ventilatorio se conoce como reflejo de Cushing o tríada de Cushing2, 6.
Factores que influyen en el FSC y la PIC
- Presión arterial (PAM): Gracias a la autorregulación cerebral, el FSC se mantiene constante en rangos de PAM entre 50 y 150 mmHg, lo que hace que la PIC apenas se modifique (Figura 2). La recomendación en pacientes con patologías intracraneales es mantener la PAM entre 80–100 mmHg para asegurar perfusión cerebral óptima, adaptando según comorbilidades7.
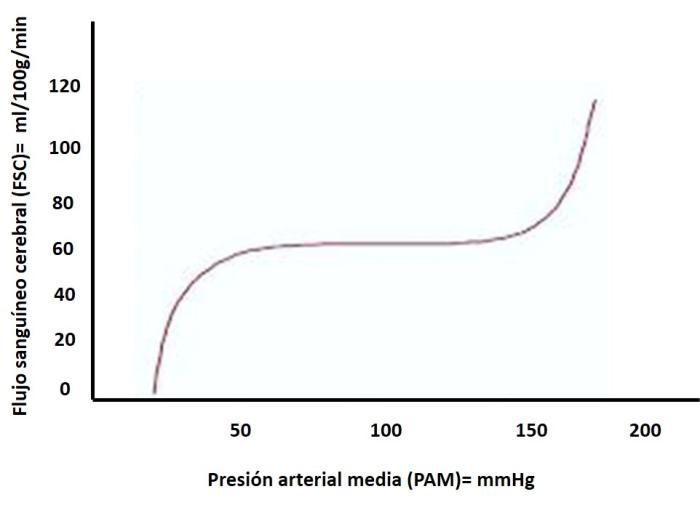
- Presión arterial de oxígeno (PaO₂): La hipoxemia severa (PaO₂ <60mmHg) produce vasodilatación cerebral, aumentando el FSC y la PIC (Figura 3), por lo que es esencial asegurar una adecuada oxigenación del paciente2, 4.
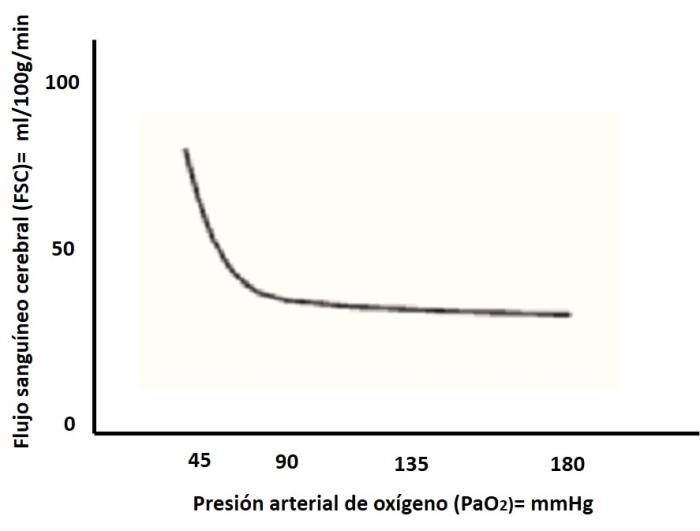
- Presión arterial de dióxido de carbono (PaCO₂): La PaCO₂ regula el tono vasomotor cerebral: la hipercapnia aumenta el FSC y la PIC mientras que la hipocapnia produce vasoconstricción y reducción rápida de la PIC. En estos pacientes se recomienda la reducción temporal de PaCO₂ a ≈30 mmHg para disminuir la PIC de forma rápida, limitando la hipocapnia prolongada por riesgo de isquemia cerebral2, 3 (Figura 4).
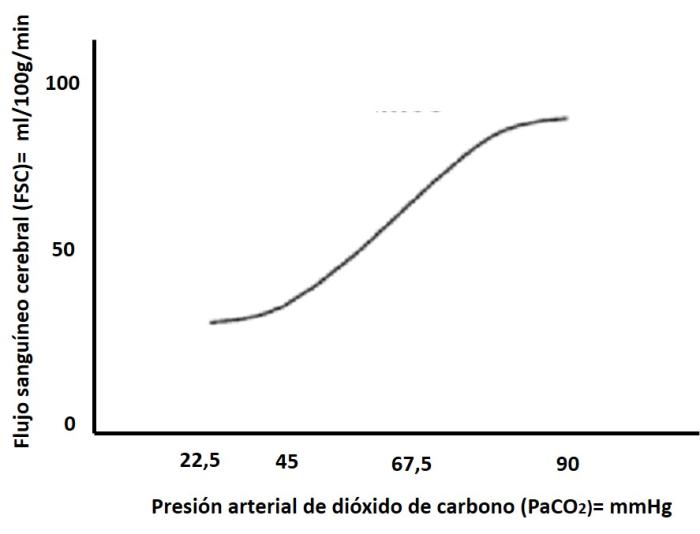
Metabolismo cerebral y lactato: Algunas lesiones intracraneales (p. ej. , meningiomas) muestran alteraciones del metabolismo de carbohidratos y pueden producir lactato localmente; además la disrupción de la barrera hematoencefálica puede alterar el intercambio de lactato entre el FSC y la sangre. En perros anestesiados, se ha observado hiperlactatemia asociada a meningiomas e hidrocefalia incluso con parámetros sistémicos de oxigenación normales; esto sugiere producción local o alteración del transporte y obliga a interpretar el lactato con cautela antes de administrar fluidos innecesarios que aumenten PIC8.
Manejo anestésico del paciente con aumento de PIC
Situaciones que pueden requerir anestesia general
Los pacientes con PIC elevada pueden requerir anestesia para procedimientos diagnósticos o terapéuticos: tomografía axial computerizada (TAC), resonancia magnética (RM), extracción de líquido cefalorraquídeo (LCR), biopsias, craneotomías, drenaje de hematomas, etc. La incidencia de complicaciones graves perioperatorias tras cirugía intracraneal puede alcanzar 10–20%, con impacto sobre mortalidad y morbilidad4, 5.
Estos pacientes pueden también requerir sedación o anestesia general para procedimientos no relacionados con la lesión intracraneal, lo que puede entrañar un riesgo anestésico incrementado por el compromiso cerebral preexistente.
Estabilización inicial
Antes de la anestesia es fundamental controlar los signos clínicos asociados a la patología intracraneal, tales como convulsiones y alteraciones del estado mental. Por ello, es habitual que estos pacientes ya se encuentren en el momento de la anestesia en tratamiento con fármacos anticonvulsivantes, corticoides, y que incluso requieran terapia para reducir el edema cerebral (manitol o suero hipertónico salino)2-4.
Otras medidas incluyen la administración de fluidoterapia intravenosa con cristaloides, para garantizar el retorno venoso y preservar la PPC, y asegurar el aporte de oxígeno con la cabeza del paciente elevada unos 30º9, 10.
Protocolo anestésico — elección de fármacos
- Agonistas adrenérgicos α-2: Como la dexmedetomidina. Reducen el FSC, evitando aumentos de la PIC y controlando la aparición de focos de hemorragia3, 7. Se ha descrito también su efecto neuroprotector y se cree que también de inhibición de las convulsiones11. Como desventaja, producen hipertensión sistémica transitoria y vómitos, aunque estos efectos son dosis-dependiente12 y se observan más por su uso en forma de bolos que como IIC.
- Opioides: Ayudan a suprimir respuestas hemodinámicas al dolor y nocicepción y no tienen efecto demostrado sobre la PIC12. Sin embargo, pueden causar depresión ventilatoria, y por ello aumento de la PaCO₂, y también náuseas y vómitos, lo que aumentaría la PIC12, 13. Aunque no está demostrado en medicina veterinaria, en humana se cree que pueden atravesar la BHE, alterar el estado mental y enlentecer la recuperación de estos pacientes14.Los más utilizados en veterinaria son butorfanol (para procedimientos diagnósticos y no dolorosos), metadona y fentanilo (para procedimientos dolorosos).
- Benzodiacepinas: tienen efecto ansiolítico, sedante y anticonvulsivante y sus efectos hemodinámicos son mínimos12. Como desventaja, producen depresión ventilatoria y consiguiente aumento de la PaCO₂, 12
- Ketamina: tradicionalmente se ha desaconsejado su uso ya que aumenta el FSC y la PIC por estimulación simpática, sin embargo, también tiene efecto neuroprotector por bloqueo de receptores de N-metildiaspartato (NMDA) en el sistema nervioso central, proporciona analgesia y es útil en pacientes con convulsiones refractarias12.
- Lidocaina: posee efecto analgésico, antiinflamatorio y antitoxémico demostrado en perros12, 15. Tradicionalmente no se ha empleado en gatos por su menor rango terapéutico, si bien esto parece empezar a ponerse en entredicho16. No reduce requerimientos de inductores17, pero su uso en forma de IIC si reduce la CAM de anestésicos inhalatorios16, 18.
- Inductores: el propofol, etomidato o alfaxalona son todos igualmente válidos en estos pacientes por su efecto reductor sobre FSC, la PIC y el metabolismo cerebral12, 19. Combinados con opioides y benzodiacepinas permiten inducciones suaves y con menor impacto hemodinámico1, 2, 12.
- Mantenimiento anestésico inhalatorio: los anestésicos inhalatorios (isoflurano, sevoflurano) tienen efectos dosis-dependiente a nivel cerebral: con valores >1 x CAM, producen vasodilatación cerebral y aumento del FSC, mientras que a valores < 1 x CAM, predomina su efecto reductor del metabolismo cerebral4, 7, 20. Por ello, si se usan anestésicos volátiles, es necesario mantener concentraciones bajas y combinar con IIC opioides, dexmedetomidina, lidocaína e incluso ketamina a dosis baja, que permitan reducción de dosis es recomendable1-3, 11, 12.
- Anestesia total intravenosa (TIVA): el mantenimiento mediante TIVA de propofol es de elección en perros por su mejor control sobre el FSC y la PIC, teniendo además una mejor estabilidad cardiovascular con respecto a los anestésicos inhalatorios4, 12, 19. La recuperación con TIVA es más tranquila que con anestesia inhalatoria y ha mostrado reducir la incidencia de complicaciones como el delirio de emergencia o las náuseas postoperatorias; pero, como desventaja, es más lenta comparada con la anestesia inhalatoria12, 21. En gatos, se desaconseja el uso de TIVA de propofol durante más de 30 minutos por estar asociado a recuperaciones muy prolongadas y desarrollo de anemia con cuerpos de Heinz22, 23. Una alternativa es el uso de TIVA de alfaxalona, que tiene efectos sobre el sistema nervioso y cardiovascular muy similares a la de propofol, pero igualmente, se asocia a recuperaciones muy prolongadas24. Es por ello que el mantenimiento con anestesia inhalatoria (preferiblemente sevoflurano) con (IIC) de dexmedetomidina y/o fentanilo es preferible en esta especie25.
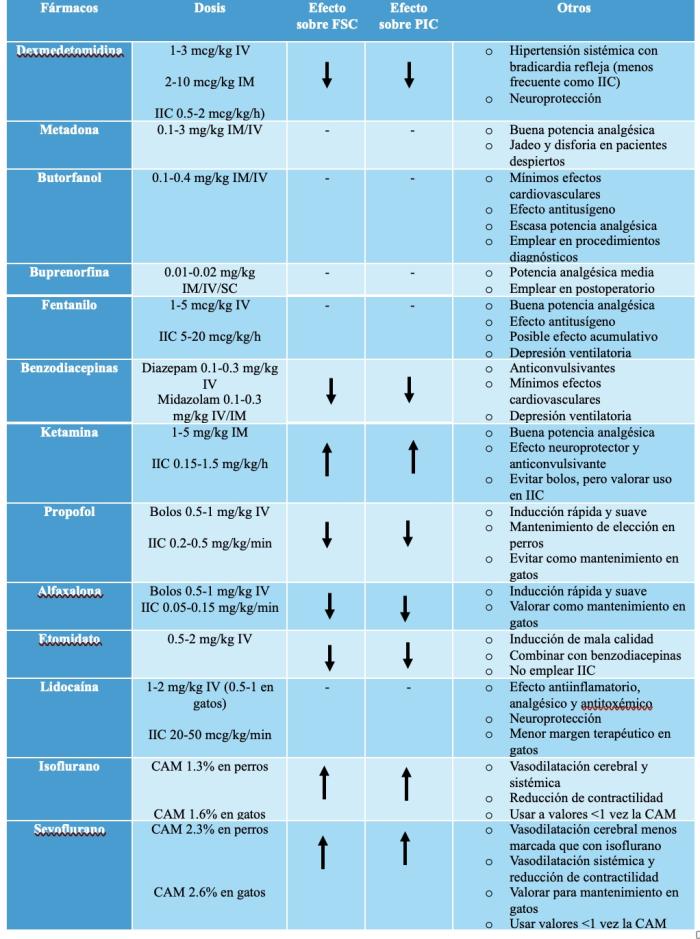
La Tabla 1 recoge los principales fármacos usados en pacientes con PIC con sus efectos sobre el FSC y la PIC, y los rangos de dosis recomendados.
Medidas para evitar la elevación de la PIC en la preparación del paciente
Existen una serie de medidas a considerar para evitar aumento de la PIC durante el manejo del paciente previo a y durante la anestesia
- Minimizar el estrés del paciente: en pacientes muy nerviosos o fácilmente estresables, será recomendable la premedicación intramuscular
- Evitar nausea y vómito: el uso de maropitant aproximadamente una hora antes de la anestesia previene el vómito asociado a fármacos como opioides y agonistas adrenérgicos α-2, así como las náuseas perioperatorias26. Su uso tiene también efectos analgésicos y de reducción de la CAM de anestésicos inhalatorios27, 28.
- Prevenir el reflejo tusígeno durante la intubación: La administración de 1 mg/kg de lidocaína 5 minutos antes de la inducción con propofol en perros, y la co-inducción con fentanilo en perros y gatos, inhiben el reflejo tusígeno durante la intubación de la tráquea29, 30. La aplicación de lidocaina tópica en gatos tiene efectos similares y además evita el riesgo de laringoespasmo en esta especie31.
- Evitar compresión de yugulares
- Asegurar un tiempo adecuado de preoxigenación, con la cabeza del paciente elevada 30º9, 10.
Monitorización intraoperatoria
La monitorización mínima debe incluir: presión arterial, capnografía, saturación de oxígeno de la hemoglobina (SpO₂), electrocardiograma (ECG) y temperatura.
Idealmente, la medición de la presión arterial debería hacerse de forma invasiva mediante la cateterización de un acceso arterial, para así poder detectar de forma rápida cualquier cambio en la PAM25. Si no fuese posible, se recomienda el uso de monitores de presión de alta precisión.
La SpO₂ permite monitorizar la adecuada oxigenación del paciente durante la anestesia. No obstante, esta técnica no es del todo útil para detectar hipoxemia en situaciones en las que se aportan fracciones elevadas de oxígeno (FiO2) elevadas10, 25, por lo que, si se sospecha de hipoxemia, estará indicado realizar gasometrías arteriales
La monitorización continua del ECG permitirá detectar arritmias, así como cambios repentinos en la FC, por ejemplo, bradicardia, la cuál puede indicar un reflejo de Cushing2, 6, 9.
La capnografía permite asegurar que el dióxido de carbono espirado (EtCO2), se mantenga en el rango deseado (30-35 mmHg), y también permite detectar anomalías como fugas en vía aérea, desacoplamiento del paciente del ventilador o hipoperfusión por bajo gasto cardíaco32.
Otros parámetros para monitorizar incluyen:
- Plano anestésico: el uso de monitores de Índice Biespectral (BIS) no está validado en pequeños animales y no se recomienda como único método para monitorizar plano anestésico33, 34. Por otro lado, en cirugía intracraneal, no hay acceso para valorar reflejos palpebral y deglutorio. Por ello, en estos pacientes, suelen emplearse los parámetros hemodinámicos para detectar falta de plano anestésico (aumentos de FC, FR y/o PAM)
- Espirometría
- Producción de orina: mediante cateterización uretral previa, como un indicativo de adecuada perfusión
- Lactato en sangre: puede aportar información adicional: en perros con meningioma o hidrocefalia se han observado lactatos elevados intraoperatorios, incluso con parámetros sistémicos normales, por lo que un lactato elevado no siempre indica hipoperfusión sistémica y debe interpretarse junto con la clínica y otros parámetros8.
Fluidoterapia
En pacientes anestesiados con aumento de PIC, la fluidoterapia debe mantener la volemia y preservar la presión de perfusión cerebral (PPC), evitando tanto la hipovolemia, ya que en casos extremos puede empeorar la evolución neurológica9, 10, 35.
En pacientes con aumento de PIC, se ha recomendado el uso de solución salina fisiológica (SSF) al 0.9% como fluido de elección, por su hipertonicidad (que podría ayudar evitar o tratar el edema cerebral). Sin embargo, el SSF puede potencialmente producir acidosis metabólica que llevaría a un mayor aumento de la PaCO212, 25. Por ello, en la práctica, las soluciones de elección para el mantenimiento deben ser cristaloides isotónicos como Ringer Lactato (RL) o Isofundin, que tienen una composición similar al plasma y efecto alcalinizante para compensar la acidosis respiratoria típica de la anestesia25.
Ventilación mecánica
Se debe emplear desde la intubación del paciente, con el fin de mantener el EtCO₂ en rango 30–35 mmHg.
En cuanto al modo ventilatorio a elegir, ninguno tiene ventajas o inconvenientes en lo que a estos pacientes se refiere36, por lo que los modos ventilación controlada por volumen (VCV) y por presión (VCP) serán igualmente válidos si los parámetros se programan adecuadamente para buscar la hipocapnia leve mencionada.
El uso de presión positiva al final de la espiración (PEEP) en estos pacientes tiene beneficios como el aumento de la PaO2 y la prevención de atelectasias, así como el mantenimiento de la oxigenación cerebral37, 38. Sin embargo, el uso de PEEP también puede aumentar potencialmente la PIC38, 39, por lo que, en la práctica, se recomienda emplear el mínimo valor de PEEP imprescindible (por ejemplo, el aportado por la propia estación de anestesia).
Complicaciones intraoperatorias: reflejo de Cushing y herniación
Si se detecta un reflejo de Cushing, será necesario aplicar medidas de forma inmediata:
- Hiperventilación para reducir PaCO₂ (objetivo PaCO₂ ≈30 mmHg).
- Administración de agentes hiperosmolares:
- Manitol: Su dosis varia entre los 0, 5 – 1, 5 g/kg IV en bolo durante 15-20 minutos. Actúa como diurético osmótico que desplaza el agua desde el intersticio cerebral al torrente vascular, lo que reduce el edema y la PIC25, 40. Por su efecto diurético, requiere administración conjunta con cristaloides para evitar deshidratación e hipovolemia, y monitorización de la producción de orina. Además, su efecto puede ser transitorio y hay riesgo de efecto rebote si atraviesa la barrera hematoencefálica dañada41.
- Solución salina hipertónica (SSH): Su dosis depende del tipo de solucion (3% NaCl: 5 – 5, 4 ml/kg IV en 15-20 y 7, 5% NaCl: 4 ml/kg IV en 15-20 min). Funciona también movilizando y agua desde el intersticio cerebral hasta la circulación, reduciendo la PIC41, 42. Como ventajas adicionales, puede mejorar la contractilidad cardíaca25. Como desventajas, puede inducir alteraciones electrolíticas si se administra repetidamente25, 41.
Actualmente no hay un consenso sobre si es preferible el uso de manitol o SSH en casos de aumento de PIC, por lo que su elección queda a criterio del clínico41, 42.
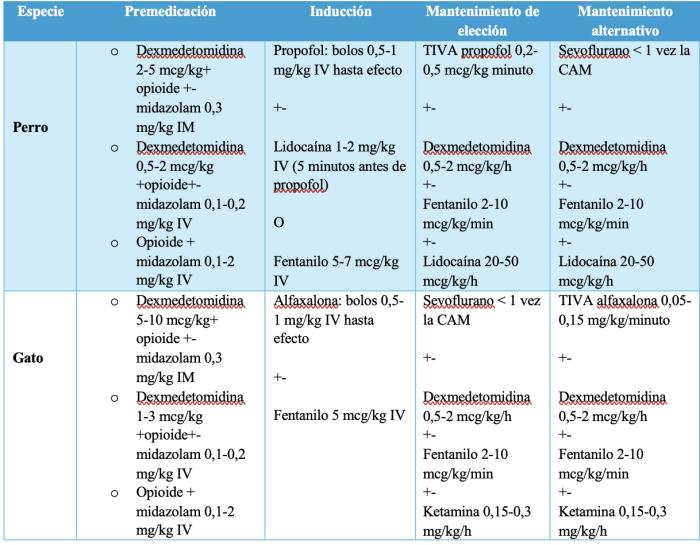
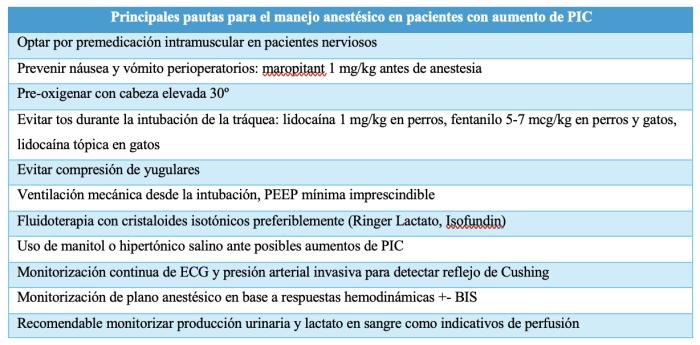
En la Tabla 2 se recogen ejemplos de protocolos de anestesia en perros y gatos con aumento de PIC, y en la Tabla 3, un resumen de los principales factores para tener en cuenta para el manejo anestésico de pacientes con aumento de PIC.
Cuidados posanestesia
El período postoperatorio inmediato constituye el intervalo de mayor riesgo clínico tras cirugía intracraneal en perros y gatos, debido a la alta probabilidad de hipertensión intracraneal secundaria, deterioro neurológico y complicaciones sistémicas4. Se debe garantizar una recuperación tranquila, manejo analgésico eficaz, oxigenoterapia y monitorización hemodinámica continua, así como evaluación neurológica seriada, por ejemplo, mediante la escala de Glasgow Modificada de Coma (MGCS)2, 3.
El empleo de IIC de dexmedetomidina puede ser útil para controlar o prevenir el delirio de emergencia en estos pacientes y favorecer una recuperación más suave. A dosis bajas, es poco probable que produzca vasoconstricción significativa o elevaciones adversas de presión arterial media (PAM), lo que podría contrarrestar efectos negativos sobre la perfusión cerebral3, 4. Además, su efecto sedante reduce el consumo metabólico cerebral y puede contribuir a la estabilidad neurológica en las primeras horas de recuperación11, 12.
Si se ha realizado una cirugía craneal, debe pautarse un adecuado plan de analgesia. Aunque el cerebro carece de nociceptores y su manipulación, por ello, no se asocia a un dolor relevante, las meninges y el periostio si tienen nociceptores, y de hecho el dolor postoperatorio en estos pacientes se asocia más a la manipulación de éstos25. El tipo de craneotomía también es determinante: las suboccipitales son las más dolorosas, seguidas de las transfrontales y transtemporales5.
El uso de opioides será útil, pero por su potencial efecto sobre el estado mental, la inducción de vómito y la depresión respiratoria o desarrollo de jadeo, es recomendable minimizar su uso y optar siempre por planes de analgesia multimodal25. En experiencia de los autores, la buprenorfina proporciona buena cobertura analgésica en estos pacientes con mínimos efectos secundarios.
El paracetamol proporciona buena cobertura analgésica en perros, pero debe evitarse en gatos por su toxicidad. La lidocaína en forma de IIC a 30-50 mcg/kg/min o parches transdérmicos también ha mostrado ser de utilidad. En casos de dolor postoperatorio severo, puede optarse también por IIC de ketamina a 0, 2-0, 3 mg/kg/h12, 25.
Las complicaciones postoperatorias más frecuentes en estos pacientes incluyen:
- Náuseas y vómitos, que pueden incrementar la presión intratorácica y, en consecuencia, la presión intracraneal. Se deben pautar antieméticos como maropitant y/o metoclopramida.
- Disforia y alteración del estado mental. Sí hay riesgo de que se produzcan, sería recomendable mantener la IIC de dexmedetomidina en las primeras horas4, 25.
- Hipertensión postoperatoria: en primer lugar, debe descartarse que ésta no se deba a dolor. Una vez descartado el dolor como causa, debe tratarse con fármacos que preserven la presión de perfusión cerebral (CPP). El labetalol ha demostrado eficacia clínica para reducir la presión arterial sin afectar desfavorablemente la presión intracraneal o la frecuencia cardíaca, especialmente cuando otros agentes sedantes fallan43. El uso de betabloqueantes como el esmolol también puede ser útil25.
- Convulsiones: son frecuentes tras cirugía intracraneal y están asociadas con peor pronóstico si no se controlan precozmente25. Habitualmente se pautan fármacos anticonvulsivantes como fenobarbital o levetiracetam.
- Estornudos o secreción nasal: típicamente ocurren tras craneotomías transfrontales por manipulación de los senos nasales5. Dado que los estornudos repetidos pueden aumentar la PIC, sería recomendable mantener al paciente ligeramente sedado hasta que se corrijan.
- Depresión ventilatoria: si es leve-moderada, puede compensarse con la administración de oxígeno. En casos severos, puede requerir incluso ventilación asistida36.
- Otras complicaciones posoperatorias descritas incluyen edema cerebral, hemorragias y neumonía por aspiración, las cuales aumentan la morbilidad y pueden prolongar el tiempo de hospitalización en cuidados intensivos veterinarios25.
Conclusiones
El manejo anestésico del paciente con aumento de la PIC es complejo y multimodal. Para minimizar los riesgos asociados, se debe tener una comprensión profunda de la fisiología cerebral, la interacción entre PAM, PaO₂ y PaCO₂ con la PIC, la farmacología anestésica y las alteraciones metabólicas asociadas a la lesión intracraneal.
Bibliografía
1. Seki S, Teshima K, Ito D, Kitagawa M, Yamaya Y. Impact of intracranial hypertension on the short-term prognosis in dogs undergoing brain tumor surgery; J. Vet. Med. Sci. 2019 81(8): 1205–1210, 2019
2. Abelson AL, Faissler D, Karas AZ. Anesthesia case of the month. Development of the Cushing reflex secondary to a dangerous increase in intracranial pressure. J Am Vet Med Assoc. 2008 May 1; 232(9): 1298-300
3. Marquez-Grados, F. , Vettorato, E. , & Corletto, F. Sevoflurane with opioid or dexmedetomidine infusions in dogs undergoing intracranial surgery: A retrospective observational study. Journal of Veterinary Science. 2020. 21(1).
4. Kohler RJ, Arnold SA, Eck DJ, Thomson CB, Hunt MA, Pluhar GE. Incidence of and risk factors for major complications or death in dogs undergoing cytoreductive surgery for treatment of suspected primary intracranial masses. J Am Vet Med Asso. 2018 Dec 15; 253(12): 1594-1603
5. Parker RL, Du J, Shinn RL, Drury AG, Hsu FC, Roberston JL, Cecere TE, Arendse AU, Rossmeisl JH. Incidence, risk factors, and outcomes for early post operative seizures in dogs with rostrotentorial brain tumors after intracranial surgery; J Vet Intern Med. 2022; 36: 694–701.
6. Fitch W, McDowall DG, Keaney NP, Pickerodt VW. Systemic vascular responses to increased intracranial pressure. 2. The 'Cushing' response in the presence of intracranial space-occupying lesions: systemic and cerebral haemodynamic studies in the dog and the baboon. J Neurol Neurosurg Psychiatry. 1977 Sep; 40(9): 843
7. Marchionne, G. , Alcoverro, E. , Spinillo, S. , & Louro, L. F. (2023). Anaesthetic management in a cat undergoing emergency craniotomy for meningioma excision. Journal of Feline Medicine and Surgery Open Reports, 9(2).
8. Sullivan LA, Campbell VL, Klopp LS, Rao S. Blood Lactate Concentrations in Anesthetized Dogs with Intracranial Disease. J Vet Intern Med 2009; 23: 488–492
9. Schizodimos T, Soulountsi V, Iasonidou C, Kapravelos N. An overview of management of intracranial hypertension in the intensive care unit. J Anesth. 2020 Oct; 34(5): 741-757.
10. Lee D, Pearson T, Proctor JL, Rosenthal RE, Fiskum G. Oximetry-Guided normoxic resuscitation following canine cardiac arrest reduces cerebellar Purkinje neuronal damage. Resuscitation. 2019 Jul; 140: 23-28.
11. Wang L, Shen J, Ge L, et al. Dexmedetomidine for craniotomy under general anesthesia: a systematic review and meta-analysis of randomized clinical trials. J Clin Anesth 2019; 54: 114–125.
12. Dugdale AHA, Beaumont G, Bradbrook C, Gurney M. Veterinary anaesthesia: principles to practice. 2nd edition. 2020. Ed. Willey Blackwell
13. Schregel W, Weyerer W, Cunitz G. Opioids, cerebral circulation and intracranial pressure. Anaesthesist. 1994 Jul; 43(7): 421-30
14. Wiener J, McIntyre A, Janzen S, Mirkowski M, MacKenzie HM, Teasell R. Opioids and cerebral physiology in the acute management of traumatic brain injury: a systematic review. Brain Inj. 2019; 33(5): 559-566.
15. Steagall PVM, Teixeira Neto FJ, Minto BW, Campagnol D, Corrêa MA. Evaluation of the isoflurane-sparing effects of lidocaine and fentanyl during surgery in dogs. J Am Vet Med Assoc. 2006; 229(4): 522-527
16. Comassetto F, Júnior GS, Iepsen LB, Cavagnari CFB, Oleskovicz N. Intravenous lidocaine may contribute to postoperative analgesia without detectable adverse effects in cats undergoing ovariohysterectomy: a randomized trial. J Am Vet Med Assoc. 2025 Oct 22: 1-8.
17. Braun C, Hofmeister EH, Lockwood AA, Parfitt SL. Effects of diazepam or lidocaine premedication on propofol induction and cardiovascular parameters in dogs. J Am Anim Hosp Assoc. 2007 Jan-Feb; 43(1): 8-12
18. Suarez MA, Seddighi R, Egger CM, Rohrbach BW, Cox SK, KuKanich BK, Doherty TJ. Effect of fentanyl and lidocaine on the end-tidal sevoflurane concentration preventing motor movement in dogs. Am J Vet Res. 2017 Jan; 78(1): 12-16.
19. Caines D, Sinclair M, Valverde A, Dyson D, Gaitero L, Wood D. Comparison of isoflurane and propofol for maintenance of anesthesia in dogs with intracranial disease undergoing magnetic resonance imaging. Vet Anaesth Analg. 2014 Sep; 41(5): 468-79.
20. Sakabe T, Matsumoto M (2010) Effects of anesthetic agents and other drugs on cerebral blood flow, metabolism, and intracranial pressure. In: Cottrell and Young’s Neuroanesthesia (5th ed). Cottrell JE, Young WL (eds). Mosby Elsevier, Philadelphia, USA. 78–94.
21. Tsai YC, Wang LY, Yeh LS. Clinical comparison of recovery from total intravenous anesthesia with propofol and inhalation anesthesia with isoflurane in dogs. J Vet Med Sci. 2007 Nov; 69(11): 1179-82
22. Pascoe PJ, Ilkiw JE and Frischmeyer KJ. The effect of the duration of propofol administration on recovery from anesthesia in cats. Vet Anaesth Analg 2006; 33: 2–7.
23. Andress JL, Day TK and Day DG. The effects of consecutive day propofol anesthesia on feline red blood cells. Vet Surgery 1995; 24: 277–282. 30.
24. Warne LN, Beths T, Fogal S, Bauquier SH. The use of alfaxalone and remifentanil total intravenous anesthesia in a dog undergoing a craniectomy for tumor resection. Can Vet J 2014 Nov; 55(11): 1083-8.
25. Duke-Novakovsky T, De Vries M, Seymour C. BSAVA Manual of canine and feline anesthesia and analgesia, 3th edition. 2016.
26. Martin-Flores M, Sakai DM, Learn MM, Mastrocco A, Campoy L, Boesch JM, Gleed RD. Effects of maropitant in cats receiving dexmedetomidine and morphine. J Am Vet Med Assoc. 2016 Jun 1; 248(11): 1257-61.
27. Niyom S, Boscan P, Twedt D. C, Monnet E, Eickhoff J. C, Effect of maropitant, a neurokinin-1 receptor antagonist, on the minimum alveolar concentration of sevoflurane during stimulation of the ovarian ligament in cats. Vet Anaesth Analg. 2013. 40 (4), 425–431.
28. Corrêa, J. M. X. , Soares, P. C. L. R. , Niella, R. v. , Costa, B. A. , Ferreira, M. S. , Silva, A. C. , Sena, A. S. , Sampaio, K. M. O. R. , Silva, E. B. , Silva, F. L. , & Lavor, M. S. L. Evaluation of the Antinociceptive Effect of Maropitant, a Neurokinin-1 Receptor Antagonist, in Cats Undergoing Ovariohysterectomy. Veterinary Medicine International, 2019
29. Cerasoli I, Nannarone S, Schauvliege S, Duchateau L, Bufalari A. The effects of intravenous lidocaine before propofol induction in premedicated dogs. J Small Anim Pract. 2016 Aug; 57(8): 435-40
30. Bravo, VR, Palomba N, Corletto F, Willis R, Vettorato. Comparison between intravenous lidocaine and fentanyl on cough reflex and sympathetic response during endotracheal intubation in dog. Vet Anaesth Analg. 2020 Jul; 47(4): 481-489.
31. Grubb T. , Sager J. , Gaynor J. S. , et al. 2020. 2020 AAHA Anesthesia and Monitoring Guidelines for Dogs and Cats. J Am Anim Hosp Assoc. 56(2): 59-82.
32. Hoff IE, Høiseth LØ, Kirkebøen KA, Landsverk SA. Volumetric and End-Tidal Capnography for the Detection of Cardiac Output Changes in Mechanically Ventilated Patients Early after Open Heart Surgery. Crit Care Res Pract. 2019 May 30; 2019
33. Bleijenberg EH, van Oostrom H, Akkerdaas LC, Doornenbal A, Hellebrekers LJ. Bispectral index and the clinically evaluated anaesthetic depth in dogs. Vet Anaesth Analg. 2011 Nov; 38(6): 536-43.
34. Lamont LA, Greene SA, Grimm KA, Tranquilli WJ. Relationship of bispectral index to minimum alveolar concentration multiples of sevoflurane in cats. Am J Vet Res. 2004 Jan; 65(1): 93-8.
35. Rossi S, Picetti E, Zoerle T, Carbonara M, Zanier ER, Stocchetti N. Fluid Management in Acute Brain Injury. Curr Neurol Neurosci Rep. 2018 Sep 11; 18(11): 74
36. Fantoni, D. T. , Ida, K. K. , Soares, J. H. N. , & Ambrosio, A. M. (2022). Mechanical ventilation in anesthesia and critical care small animal patients. Frontiers in Veterinary Science, 9, 942731.
37. Cotev, W L Paul, B C Ruiz, E J Kuck, J H Modell. Positive end-expiratory pressure (PEEP) and cerebrospinal fluid pressure during normal and elevated intracranial pressure in dogs. ntensive Care Med. 1981; 7(4): 187-91.
38. Aidinis SJ, Lafferty J, Shapiro HM. Intracranial responses to PEEP. Anesthesiology. 1976 Sep; 45(3): 275-86
39. Chambers D, Huang C, Matthews G. Basic physiology for anaesthetists. 2nd edition. Ed. Cambridge
40. Ballocco, I. , Evangelisti, M. A. , Deiana, R. , Cubeddu, F. , Pinna Parpaglia, M. L. , Serra, G. , Carta, G. , & Manunta, M. L. (2019). A pilot study evaluating the effect of mannitol and hypertonic saline solution in the treatment of increased intracranial pressure in 2 cats and 1 dog naturally affected by traumatic brain injury. Journal of Veterinary Emergency and Critical Care, 29(5), 578-584.
41. Bernhardt K, McClune W, Rowland MJ, Shah A. Hypertonic Saline Versus Other Intracranial-Pressure-Lowering Agents for Patients with Acute Traumatic Brain Injury: A Systematic Review and Meta-analysis Neurocrit Care. 2024 Apr; 40(2): 769-784
42. Hoehne SN, Yozova ID, Vidondo B, Adamik KN. Comparison of the effects of 7. 2% hypertonic saline and 20% mannitol on electrolyte and acid-base variables in dogs with suspected intracranial hypertension. J Vet Intern Med. 2021 Jan; 35(1): 341-351
43. Zublena F, De Gennaro C, Corletto F. BMC. Retrospective evaluation of labetalol as antihypertensive agent in dogs Vet Res. 2020 Jul 24; 16(1): 256
 by Multimédica
by Multimédica