Evaluación y cuidados pre y posquirúrgicos en pacientes con shunt portosistémico
Resumen breve
Cuando un animal va a ser sometido a una intervención quirúrgica, el equipo humano de la clínica veterinaria ha de prepararse para evaluar al paciente y ofrecer así el mejor servicio posible. En pacientes con patologías graves y con solución quirúrgica hemos de hacer una buena evaluación prequirúrgica para asegurar una anestesia lo más específica posible de acuerdo a su patología y al estado previo del animal a la intervención. Para hacer el proceso de forma segura, se hará un seguimiento…Índice de contenidos
Resumen
Cuando un animal va a ser sometido a una intervención quirúrgica, el equipo humano de la clínica veterinaria ha de prepararse para evaluar al paciente y ofrecer así el mejor servicio posible. En pacientes con patologías graves y con solución quirúrgica hemos de hacer una buena evaluación prequirúrgica para asegurar una anestesia lo más específica posible de acuerdo a su patología y al estado previo del animal a la intervención.
Para hacer el proceso de forma segura, se hará un seguimiento del paciente con monitores multiparamétricos y se prestará especial atención a diferentes valores de la misma.
En este artículo se hablará de pacientes con enfermedades hepáticas, tales como el shunt portosistémico (SPS), de la importancia del manejo pre y posoperatorio del mismo, así como también de la monitorización intraoperatoria de este.
Introducción
Los pacientes con patologías hepáticas suelen presentar diversos problemas preoperatorios tales como la delgadez, afecciones neurológicas, etc., que deben ser evaluadas antes de cualquier intervención y durante la misma. Es importante adecuar el tipo de monitorización, fármacos, así como una correcta valoración del riesgo anestésico en función del estado general del paciente.
Para evaluar dicho riesgo se dispone de una clasificación de riesgo anestésico de la Asociación Américana de Anestesiólogos. Se denomina clasificación ASA.
| Tabla 1. Tabla ASA |
| Categoría | Riesgo anestésico | Ejemplos |
| ASA I | Riesgo mínimo, paciente sano | Castración, ovariohisterectomía |
| ASA II | Riesgo leve, presencia de patología menor | Neonatos, geriátricos, obesidad |
| ASA III | Riesgo moderado, presencia de patología | Anemia, deshidratación, patología cardíaca |
| ASA IV | Riesgo alto, alteración severa, amenaza para la vida del animal | Cardiopatía no compensada, deshidratación severa |
| ASA V | Riesgo grave, moribundos | Shock extremo, trauma severo |
| ASA V-E | Operación de urgencia | Mal pronóstico |
Previa a la anestesia se han de realizar una serie de pruebas para evaluar riesgos durante la intervención y estudiar así pruebas complementarias.
La consulta preanestésica debe realizarse unos días antes y ha de tener unos objetivos concretos:
- Obtención de historial clínico, especialmente datos que afecten al riesgo anestésico. Por ejemplo, patologías previas, datos como peso, edad, o también consultas con informes de todas las visitas veterinarias anteriores.
- Determinar pruebas complementarias.
- Obtención de datos del estado actual del paciente.
- Explicar al propietario los riesgos que corre su mascota.
- Cuidados pre y posquirúrgicos.
En la exploración preanestésica hay que fijarse en diferentes parámetros:
- Mucosas: color y relleno capilar.
- Ojos: capacidad visual, por ejemplo.
- Hidratación: a través del pliegue cutáneo se podrà evaluar.
- Palpación abdominal: explorar si existen masas y distensibilidad abdominal.
- Auscultación: comprobar si el pulso es fuerte, si es rítmico, soplos, etc.
- Evaluación neurológica: esta es muy importante. Hay que buscar alteraciones mentales, tales como la encefalopatía hepática, que puedan influir en el efecto de los analgésicos que se usarán para premedicar e inducir al animal, así como durante la anestesia del mismo.
- Temperatura: fiebre o hipotermia.
- Raza: determinadas razas presentan peculiaridades que deben tenerse en cuenta, hay razas como por ejemplo Schnauzer miniatura, Yorkshire Terrier, Loberos Irlandeses, Cairns Terrier, Carlinos, Bichón Maltés o Pastores Australianos entre otros que están predispuestas a padecer patologías hepáticas.
- Edad: es importante para determinar la dosis de los fármacos.
- Peso y condición corporal: el sobrepeso ayuda a mantener la temperatura del paciente, pero por otra parte también genera otros problemas, como por ejemplo el tener más dificultades en ventilación, de ahí la importancia de usar ventilación mecánica y asegurar así un buen intercambio de gases.Por el contrario, un bajo peso también puede alterar y desestabilizar la anestesia, ya que estos pacientes sintetizan los fármacos de forma diferente y hay riesgo de sobredosificación de los mismos.
- Medicación que tome el paciente de forma habitual. Es aconsejable en estos pacientes establecer una medicación previa a la intervención.
- Anestesias previas: estás nos ayudarán a evaluar complicaciones que haya tenido en alguna cirugía anterior.
Toda esta información debe quedar registrada en la hoja de anestesia del paciente que se haya preparado previamente con sus datos y los del propietario. Est ayuda para que así cualquier miembro del equipo pueda disponer de la valoración del mismo.
Una vez hecha esta anamnesis se procederá a realizar una serie de pruebas médicas. Como pruebas básicas se optará por un electrocardiograma, para evaluar la función cardíaca, una bioquímica completa, control de electrolitos, un hemograma y por último una radiografía del tórax lateral y ventrodorsal.
Para completar este chequeo básico se hará:
- Análisis de orina.
- Pruebas de función hepática (ácidos biliares y amoníaco). Para medir los valores de ácidos biliares se extraerá sangre después de mantener al paciente con al menos 12 horas de ayuno (análisis prepandial) y posteriormente se facilitará comida y a las dos horas se procederá a volver a extraer sangre parte la evaluación del nivel postpandrial.
- Ecografía.
- TAC (angiografía por tomografía computarizada) con contraste.
Los pacientes hepáticos son animales con un alto riesgo anestésico, ya que suelen arrastrar complicaciones previas tales como el bajo peso y en consecuencia un mal desarrollo físico. También suelen padecer hipoalbuminemia, coagulopatías, hipoglucemias e hipotermia.
La hipoalbuminemia es una disminución de los niveles séricos de albúmina. La albúmina es la principal proteína de la circulación, responsable de un 60 % del total de la masa proteica del plasma. De ahí su importancia para adecuar una buena anestesia. No hay que olvidar que la mayoría de los fármacos anestésicos que se usan pasan a ser metabolizados por hígado, complicando así el estado de consciencia más aún que a un animal sin patologías. Para evitarlo se usarán fármacos de corta duración o reversibles, ayudando así a una metabolización más efectiva.
Shunt portosistémico
Este artículo se va a centrar en unos pacientes con patología hepática concreta: el shunt portosistémico (SPS).
Se podría definir el SPS, como la presencia de una comunicación entre la vena porta y la circulación sistémica que hace que la sangre procedente del tracto gastrointestinal se distribuya por el organismo sin haber sido detoxificada con anterioridad. Cuando estos casos están presentes desde el nacimiento, el hígado no se desarrolla de forma natural y el paciente suele presentar sintomatología muy inespecífica.
Algunos síntomas son:
- Crecimiento deficiente.
- Hipoglucemias.
- Diarreas.
- Cambios de comportamiento.
- Convulsiones.
- Encefalopatía hepática.
- Hipoalbuminemia
- Problemas de coagulación.
- Hipotermia.
La encefalopatía hepática es la causa principal de los síntomas que afectan al sistema nervioso central como: letargia, ataxia, estupor, circling, ceguera, convulsiones y coma. Este síndrome se desarrolla cuando existe una pérdida de más del 70% de la funcionalidad hepática. Muchas de las sustancias neurotóxicas absorbidas y producidas por el sistema gastrointestinal, que se vierten al sistema portal para ser filtradas por el hígado, son vertidas a la circulación sistémica a través del shunt.
Tipos de shunt
Se pueden distinguir dos tipos de shunt portosistémico. Puede ser congénito o adquirido.
Congénito
El SPS congénito puede ser intrahepático o extrahepático, siendo este último de componente hereditario en un 70 % de los casos.
Hay razas con predisposición a padecerlo, como por ejemplo el Yorkshire Terrier o el Schnauzer miniatura.
Las comunicaciones se pueden dar entre la vena porta y la cava, vena porta y vena ácigos o vena porta y vena frénica.
Adquirido
El SPS adquirido es consecuencia de una hipertensión portal (secundaria a enfermedades hepáticas crónicas) en la que se generan múltiples vasos extrahepáticos como " válvulas de escape". Cuando la presión de la vena porta es más elevada que la de la vena cava caudal se genera este tipo de SPS, siendo este un 30 % de los casos.
Debido a que el flujo portal se ve disminuido se producirá una atrofia hepática y una reducción de la actividad metabólica hepática, dando lugar a un aprovechamiento ineficaz de los nutrientes del organismo y por tanto un crecimiento anómalo.
Diagnóstico
Para diagnosticar la patología se realizará una anamnesis completa. Posteriormente serealizarán pruebas sanguíneas como la evaluación de los ácidos biliares pre y postprandiales. Entre los hallazgos de alteraciones en pruebas de laboratorio se encontrarán microcitosis, hipoalbuminemia y aumento leve de la fosfatasa alcalina (ALP) Y de la Alanina aminotransferasa (ALT), hipocolesterolemia y niveles bajos de urea en sangre.
La concentración de ácidos biliares en ayunas puede estar normal o alto, pero los valores postprandiales estarán siempre elevados. La concentración del amoníaco en ayunas pueden estar altos o normales. Estos hallazgos se dan en más del 50 % de los perros afectados, pero son inespecíficos. Los pacientes con SPS tienden a formar cristales de urato amónico, siendo la valoración de la orina otro parámetro más a tener en cuenta.
Para confirman que se trata de un SPS hay que hacer diferentes pruebas para visualizar la comunicación vascular anómala. Se usarán pruebas de diagnóstico por imagen tales como la ecografía o el TAC. Se pueden realizar las dos pruebas, aunque sería imprescindible el TAC al menos como prueba única (Figura 1).
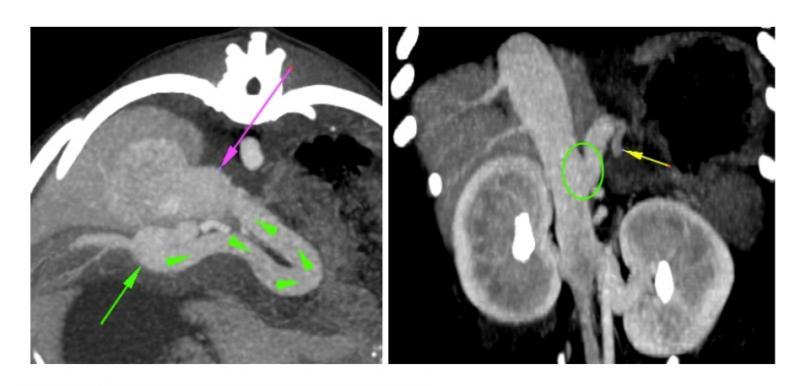
La angiografía por tomografía computarizada es el método de diagnóstico de preferencia para la localización del SPS, presentando una mayor sensibilidad que la ecografía abdominal. Es un procedimiento no invasivo y rápido que proporciona una buena visualización de los vasos portales y ramas intrahepáticas mediante una inyección intravenosa de contraste iodado a una dosis de 600mg/kg. El TAC es muy útil para la localización de vasos anómalos no visibles mediante ecografía y proporciona datos anatómicos más específicos para la planificación quirúrgica.
En el TAC se evaluará el grado de desarrollo de la vascularización hepática, siendo conveniente realizar nuevamente la prueba al finalizar la intervención para la comprobación de una buena resolución de la patología del paciente.
En el TAC se puede visualizar una sobrecarga de volumen en la vena cava caudal prehepática, la vena porta no estaría desarrollada y por lo tanto no sería visible en el TAC previo. También han de evaluarse riñones, y vesícula biliar para ver páncreas, bazo, y comprobar si hay alguna complicación, tales como una insuficiencia renal o algún otro tipo de malformación.
Para realizar estas pruebas habrá que sedar al animal, sobre todo para el TAC ya que se requiere que el paciente esté absolutamente quieto. Hay que tener muy claro que no hay un protocolo para sedar y anestesiar a un paciente hepático, por ello se seguirán una serie de recomendaciones.
Hay que evitar las benzodiacepinas, ya que se metabolizan principalmente vía hepática. Para realizar el TAC, se monotorizará con un pulsioxímetro al animal durante la realización de este. Hay que de preoxigenar con oxígeno al 100 % al menos durante 3 minutos antes de la realización de la misma. La inducción se realizará con propofol 1 % a dosis de 2-3 MG/ kg y fentanilo a 3-5 microgramos/ kg.
Posteriormente, durante la realización del TAC, se mantendrá al paciente con gases inhalados, preferiblemente sevoflorano, ya que este es de metabolización rápida y ayudará al paciente a despertar con un poco más de seguridad, aunque no sin riesgos. Con el sevoflorano el paciente alcanza la hipnosis más rápido y se recupera más rápido, aunque no hay que olvidar que estos animales, debido a su patología, metabolizan todo de forma más lenta. Para asegurar también una mejor anestesia durante la prueba del TAC, sería ideal que el paciente estuviese asistido a través de una ventilación controlada/mecánica, asegurándonos de esta forma una buena oxigenación, tan importante en nuestros pacientes.
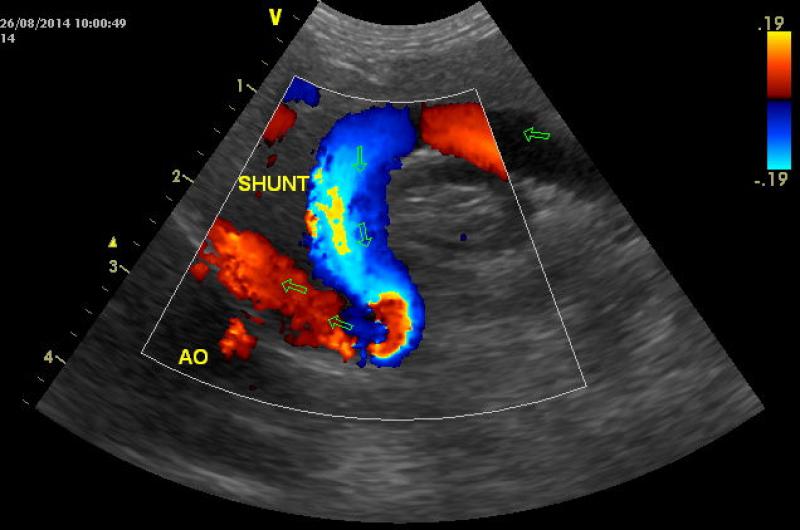
Es también recomendable repetir esta prueba después de la intervención, ya que esta ayudaría a verificar la eficacia de la intervención y poder detectar posibles comunicaciones no cerradas con totalidad.
Otra prueba que nos sirve para completar el diagnóstico es la ecografía del animal, pero al ser más inespecífica se recomienda la realización del TAC como prueba concluyente (Figura 2).
Una vez diagnosticado nuestro paciente con la patología del shunt portosistémico, hay que tener especial cuidado con diferentes parámetros, como alteraciones en la coagulación. Las posibles complicaciones deben ser identificadas y tratadas, en lo posible, antes de la anestesia. La restricción proteica en la dieta, el tratamiento con metronidazol previo a la intervención, son dos herramientas que podemos usar en nuestros pacientes con anterioridad a la intervención quirúrgica. Estos pacientes suelen tener retardos en la coagulación. La administración de vitamina K mejoraría este problema, por lo que su uso unos días antes de la cirugía también estaría indicado.
Hay que intentar compensar los síntomas del paciente antes de la intervención para que llegue a ella lo más estable posible.
Los pacientes con hepatopatía pueden ser particularmente susceptibles a los efectos de los anticoagulantes de las soluciones coloides, por lo que se usará, si es necesario, la administración de plasma en su lugar y así mejorar los retardos de coagulación y la presión oncótica (es una forma de presión osmótica debida a la diferencia de concentración de proteínas plasmáticas que existe entre el plasma sanguíneo, en el interior de los vasos sanguíneos y el líquido intersticial, en el intersticio celular). Esta presión oncótica se ve afectada al alterarse la albúmina. Algunos autores recomiendan el uso de levitiracetam durante los dos o tres días previos para prevenir los signos neurológicos, especialmente se recomienda en casos con pacientes que padecen encefalopatía hepática con antecedentes de convulsiones, ya que se reduciría el índice de mortalidad posoperatoria, así como también reduciría la severidad del síndrome neurológico postulación (PLNS) si el animal lo padeciese.
Los efectos de las drogas que se administran para sedar a este tipo de animales con tales patologías hepáticas, son imprevisibles. El metabolismo de las drogas suministradas depende del flujo sanguíneo y de la fracción de extracción hepática. Si a esto se añade una hipoalbuminemia, la respuesta al fármaco suele ser imprevisible, ya que se exarceba los efectos farmacológicos de los mismos porque la ligadura proteica es menor. Por todo esto los efectos de los fármacos suelen prolongarse y es así su efectividad más continua en el tiempo.
Tratamiento
El tratamiento del SPS congénito incluye la ligadura total o parcial del conducto anómalo. Esto podría suponer la curación total del animal, aunque hay riesgos asociados como la hipertensión portal secundaria o incluso complicaciones posteriores que llevasen al animal al fallecimiento.
El shunt portosistémico adquirido, por lo general, no tiene una resolución quirúrgica, pero el congénito sí. Una vez el animal esté lo más compensado posible de sus alteraciones ya descritas, se procederá a la fijación de la intervención.
Una dieta compensatoria con un pienso creado para esta patología, tratamiento antibiótico como metronidazol o amoxicilina y un protector gástrico como la famotidina, junto con la vitamina K en días previos, puede ayudar a tener un paciente más estable de cara a la cirugía.
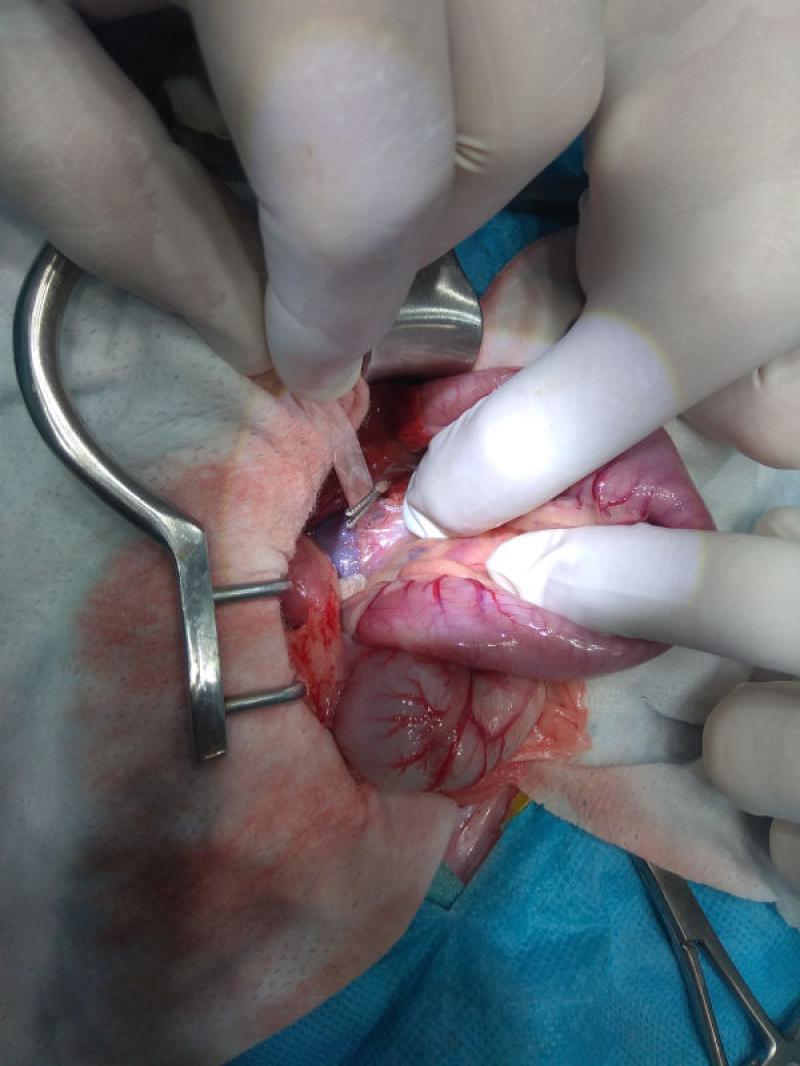
El tratamiento de elección para un SPS es el estrechamiento quirúrgico o ligadura completa progresiva del vaso con la derivación anormal.
La ligadura se puede realizar con:
- Inyección intravenosa de un émbolo de un pegamento especial.
- Banda de celofán.
- Espiral embolia intravenosa.
- Anillo aneroide.
Una presión del sistema porta excesivamente elevada (hipertensión portal) puede provocar la muerte, por eso la importancia de las pruebas previas para evaluar el grosor del mismo y así también si viabilidad quirúrgica.
La hipertensión portal provoca:
- Distensión abdominal.
- Dolor.
- Diarrea sanguinolenta.
- Éxtasis del intestino con acumulación de gas.
- Choque endotóxico.
La ligadura parcial se realizará su hay riesgo de hipertensión portal (Figura 3).
Anestesia e intervención
Para la intervención hay que anestesiar al animal, aunque no haya un protocolo exacto, se describirán una serie de pautas que son adecuadas para este tipo de pacientes.
Estos pacientes suelen ser jóvenes y tienen un riesgo elevado de padecer hipoglucemia, de ahí que el ayuno previo debe de ser corto, en torno a 4-6 horas, y controlar por esto la glucosa de forma recurrente.
Una vez obtenidos todos sus parámetros de referencia como frecuencia cardíaca, frecuencia respiratoria, temperatura, color de mucosas, etc., se pasará a la premedicación del paciente. Para estos pacientes está indicado el uso de un opiáceo puro como es la metadona. Se dejará que haga su efecto y en los siguientes minutos previos a la intervención, se oxigenará al paciente sin estresarlo con oxígeno al 100 % durante unos 3 minutos.
Para inducir la anestesia se usará propofol a una dosis de 2-3 MG/kg y fentanilo a 3-5 microgramos/kg. Una vez inducidos y rasurados para la intervención, se hará el mantenimiento con gases inhalatorios, en este caso con sevoflorano al 2-3 %. Para mantener la analgesia intraoperatoria se usará el remifentanilo a 0.1-0.3 MG/kg.
Es preferible que el paciente posea una vía central y otra periférica, para posibles transfusiones de plasma durante la intervención.
En la medida de lo posible se intentará tener un catéter arterial para controlar la presión arterial por vía invasiva y también hay que controlarla por el método más usado y más accesible, la oscilometría, ya que el mantenimiento de una buena presión arterial es de vital importancia en estos pacientes. También hay que vigilar la oxigenación, capnografía o temperatura entre otras.
Hay que prestar especial atención a la temperatura. Hay que intentar mantenerla por encima de 37° C. Los pacientes con SPS suelen ser razas pequeñas, con lo que las temperaturas tienden a disminuir cuando entran a quirófano. A través de calor externo, tales como mantas térmicas hay que hacer lo posible para que esta no descienda. Como consecuencia de la hipotermia (tan habitual en estos perros), aumenta el consumo de oxígeno, disminuyendo así los requerimientos anestésicos y prolongando aún más los efectos de los fármacos. Hay que evitar a toda costa que esto suceda, ya que empeorará el pronóstico.
Los niveles de CO2 han de ser controlados también con atención. Estos nos indican si existe un buen intercambio de gases y por lo tanto si hay un buen funcionamiento del sistema circulatorio.
Se deben evitar aquellos fármacos que tengan mucho metabolismo hepático o bien usar fármacos de acción corta y reversibles. Benzodiacepinas o acero acuna están totalmente contraindicados.
Postoperatorio
Una vez finalizada la intervención quirúrgica se pasará al paciente a una jaula especialmente preparada para la recuperación. Se debe estar pendiente de los diferentes parámetros para evitar un mal desenlace, ya que estos pacientes son animales críticos que pueden fallecer si no se controlan las posibles complicaciones.
Dentro de las complicaciones posteriores a la cirugía, puede producirse un shock hipovolémico, dolor abdominal, distensión abdominal y vómitos o diarreas hemorrágicas. La ascitis también puede presentarse ante una hipertensión portal leve. Otra complicación posible son las convulsiones, que se presentan entre un 7-18 % de los pacientes y que deben ser tratadas en función de la intensidad y frecuencia.
Conociendo todas las posibles complicaciones, cuando el animal pase a hospitalización en su box, se podrá predecir cualquier adversidad con la observación del mismo y registrando diferentes parámetros tales como la presión arterial, frecuencia cardíac
a, frecuencia respiratoria, temperatura, etc., y valorar también si el paciente siente algún dolor tras la intervención. El control de la temperatura es vital en estos pacientes.
Se pueden establecer unos requerimientos mínimos para una buena recuperación:
- Jaulas de recuperación de tamaño adecuado y acceso fácil.
- Material acolchado y aislante (cama) y mantas.
- Ambiente cálido y medios de calentamiento activo.
- Pulsioxímetro.
- Medios para obtener una vía aérea permanente.
- Medios para administrar oxígeno y ventilación controlada.
- Hoja de cuidados postoperatorios que incluya la monitorización regular y medicación (analgesia, antibióticos, etc.)
De esta forma será más exhaustivo el seguimiento y se podrá actuar de forma más rápida ante cualquier problema, aunque hay también que tener en cuenta otros factores que pueden influir en la recuperación del animal:
- Técnica anestésica: los anestésicos inyectables suelen eliminarse más lentamente que los inhalados. Una técnica para evitar el dolor intra y posoperatorio son los bloqueos anestésicos (TAP-block, vaina del transverso abdominal) de los nervios que intervienen en la zona implicada.
- Duración de la anestesia: cuanto más duradera sea la intervención, más larga será la recuperación.
- Estado físico del paciente.
- Capacidad de eliminación de los anestésicos: la insuficiencia hepática retrasa la eliminación de los fármacos que se metabolizan en el hígado.
- Hipotermia: implica una recuperación prolongada y reducción del nivel de consciencia. Se produce vasoconstricción periférica, arritmias y reducción de la contractilidad miocárdica, así como también un aumento de consumo de oxígeno.
El periodo postanestésico es considerado como uno de los más conflictivos del periodo anestésico y dónde la mortalidad es más elevada. Aquí será necesario aumentar la vigilancia y los cuidados en la hospitalización. Durante este periodo se verificarán los parámetros relacionados con el sistema cardíaco y respiratorio. Se anotará la frecuencia cardíaca y calidad de pulso periférico. Si el paciente lo permite se usará el pulsioxímetro. La frecuencia cardíaca se puede ver alterada por el dolor, el cual hay controlar y evitar vacíos analgésicos en el animal. La hipotensión es uno de los problemas que hay que vigilar. Alteraciones respiratorias pueden ser causadas por fármacos que se están usando para controlar el dolor, o bien por una mala permeabilidad de las vías aéreas, e incluso por edemas producidos por una elevada fluidoterapia durante la cirugía.
El índice de mortalidad perioperatoria en la cirugía del SPS extrahepático reducido mediante banda de celofán se sitúa alrededor del 6-9 %, si hsy complicaciones este índice aumenta al 10-28 %. Las principales complicaciones son:
- Hipoglucemias.
- Anemia.
- Hemorrágicas.
- Coagulopatías.
- Hipertensión portal.
- Convulsiones.
- Formación de trombos.
- Recurrencia de los síntomas.
- Muerte súbita.
Tratamiento
No existe un consenso claro sobre el tratamiento y control posoperatorio del SPS, ya que debe ser evaluado en función del paciente.
Generalmente el tratamiento ambulatorio consiste en antibioterapia (metronidazol, ampicilina o neomicina) , lactulosa y dieta. La duración del tratamiento se considerará en función de la sintomatología y de los niveles de amoníaco previos a la intervención. Hayaq que hacer también un control de análisis de sangre. Este control analítico debe realizarse al mes de la intervención, valorando principalmente el amoníaco y ácidos biliares ( pre y posprandiales). Estos deben ser valorados nuevamente a los 3 meses, en función de los resultados anterioridad siempre, ya que estos deben tender a disminuir.
Ante la presencia de niveles anormales se debe considerar la presencia de un flujo residual a través de un shunt secundario a un cierre incompleto, el cual puede ser evaluado por ecografía o a través de un TAC de revisión, que ha de proponerse al propietario para su nueva evaluación.
Conclusión
En conclusión, el SPS es una anomalía vascular hepática que debe ser tratadas de forma quirúrgica. Previo a la intervención es necesario la estabilización del paciente para mejorar el pronóstico perioperatorio. Con las debidas pruebas tales como el TAC se podrá llegar al diagnóstico, evaluando así el tratamiento quirúrgico del mismo. Estos pacientes son críticos y no se puede establecer unos pasos a seguir que certifiquen que se va a obtener un buen resultado, ya que son bastantes imprevisibles, no hay por ejemplo un protocolo anestésico específico, solo recomendaciones anestésicas. Para una buena valoración de la intervención quirúrgica son de gran utilidad los monitores multiparamétricos, teniendo especial cuidados con parámetros como la presión arterial para una buena evolución de la intervención. Esta monitorización ha de llevarse a cabo pre, intra y postoperatoriamente. Los cuidados y exploración posquirúrgica son de vital importancia, ya que los pacientes con patologías hepáticas tienen una evolución muy imprevisible y por ello el propietario del animal ha de estar siempre informado de las posibles complicaciones adyacentes a esta patología.
Bibliografía
J. Engel Manchado, L. García Guasch. Manual del ATV. Multimédica Edicones Veterinarias 2019. Barcelona.
Ignacio Sánchez Cordero. Manual clínico de monitorización anestésica en pequeños animales. 2019 Zaragoza.
Colegio americano de cirujanos veterinarios. Revista ACVS. 2022.
Margaret Moore, Hill Simpson. Manual para auxiliares técnicos veterinarios. 2003. Gloucester, Reino Unido.
Eva Rioja, Verónica Salazar Nussio, Miguel Martínez Fernández, Fernando Martínez Tablada. Manual de anestesia y analgesia de pequeños animales. 2013. Zaragoza, España.
 by Multimédica
by Multimédica