Caso clínico: dermatofitosis por Microsporum canis en dos Jack Russell y un gato Persa, con transmisión al propietario
Resumen breve
Se presentan en consulta dos perros de raza Jack Russel, un gato de raza Persa y la propietaria con lesiones cutáneas numulares y eritematosas en diferentes localizaciones. Este caso representa una situación compleja de dermatofitosis por Microsporum canis con contagio al propietario y supone un desafío terapéutico.Índice de contenidos
Resumen
Se presentan en consulta dos perros de raza Jack Russell, un gato de raza Persa y la propietaria con lesiones cutáneas numulares y eritematosas en diferentes localizaciones. Al examen clínico, los animales no presentan signos sistémicos evidentes. Se realiza un estudio minucioso y rutinario de la piel de cada paciente. La fluorescencia de la lámpara de Wood, el tricograma y la citología nos confirman una infección por Microsporum canis. Tras estos hallazgos se procede a empezar con un tratamiento multimodal con antifúngicos sistémicos, tópicos y un control ambiental. El protocolo y la monitorización en este caso consiste en un tratamiento tópico y sistémico de 6 semanas con la realización de un cultivo fúngico de cada animal 2 semanas después de la parada de la pauta médica. Los dos perros se tratan con ketoconazol y el gato con itraconazol, y de forma tópica a todos se les trata con enilconazol. Los tres animales responden favorablemente a los antifúngicos, con una mejoría clínica de las lesiones. Sin embargo, tras realizar el cultivo fúngico 2 semanas después de finalizar el tratamiento, el gato presenta un cultivo positivo mientras que los dos perros tienen un resultado negativo. Por ello, se empieza de nuevo el protocolo completo de tratamiento durante otras 6 semanas para los tres animales, lo que supone un reto en el seguimiento clínico.
Este caso representa una situación compleja de dermatofitosis con contagio al propietario y supone un desafío terapéutico.
Introducción
La dermatofitosis es una infección fúngica de la piel causada por hongos queratinofílicos. Microsporum canis (M. canis) es el patógeno que se aísla de forma más común representando el 90 % de las dermatofitosis en los gatos. Tiene un carácter zoonótico y es muy contagioso entre animales1.
Aunque la dermatofitosis puede afectar a cualquier raza los más susceptibles son los gatos de pelo largo, en particular el gato Persa2,3. Las razas de perro que más predisposición racial tienen son el Yorkshire terrier4,5 (M. canis) y los perros de caza y trabajo entre los que se encuentra el Jack Russell terrier, aunque estos últimos tienen principalmente una predisposición al dermatofito Trichophyton mentagrophytes6.
Para detectar la infección se utilizan métodos de diagnóstico de fácil alcance para el clínico como el examen bajo la lámpara de Wood, el examen directo del pelo al microscopio o tricograma, la citología de la lesión por aposición y el cultivo fúngico. La lámpara de Wood es una herramienta rápida en la que el valor predictivo negativo y positivo es de una media del 93 %6. Se trata de una prueba de sensibilidad moderada. Tradicionalmente se ha considerado que solamente el 50 % de las cepas de M. canis presentan fluorescencia bajo esta luz ultravioleta7 aunque recientemente, en un artículo de revisión, se estipula que el porcentaje de fluorescencia es incluso del 80 % cuando este examen se realiza en condiciones correctas6. El tricograma por su lado es otra técnica rápida y sencilla que se utiliza para detectar esporas e hifas fúngicas en el tallo piloso para confirmar el diagnóstico. Este método tiene una baja sensibilidad (59 %) por sí sola, pero si se combina con la fluorescencia de la lámpara de Wood para seleccionar los pelos, presenta una sensibilidad del 76 %8. El cultivo fúngico en agar dextrosa de Sabouraud es la técnica más sensible, actualmente considerada como el gold standard, y se utiliza principalmente para confirmar la infección, diagnosticar el tipo de dermatofito y monitorizar la enfermedad9.
El tratamiento tiene un enfoque multimodal, se deben utilizar antifúngicos de uso tópico y sistémico junto a una buena limpieza del ambiente para llegar a la cura micológica6,10.
Caso clínico
Se presentan en consulta dos perros macho y hembra de raza Jack Russel, de 4 años de edad, esterilizados. Protocolos vacunales correctamente cumplimentados y desparasitaciones con milbemicina y fluralaner trimestralmente. Los dos viven en una casa con jardín con libre acceso al exterior junto a un gato de raza Persa de 13 años y pueden estar en contacto de manera ocasional con los perros del vecindario. Tanto los perros como el gato fueron adoptados por la propietaria a los dos meses de vida y, en ese momento, al gato se le realizaron test serológicos rápidos para leucemia e inmunodeficiencia felina, siendo ambos negativos.
Comen pienso comercial y, de forma eventual, restos de alimentos caseros. Ninguno de los animales ha realizado viajes fuera de su entorno recientemente. Desde hace unos días la propietaria ha observado que los dos pacientes caninos presentan una pérdida de pelo multifocal con lesiones redondeadas y eritematosas que parecen cada día más numerosas en diferentes localizaciones (cabeza, belfos y patas delanteras). Además, al interrogar a la propietaria, esta nos comenta que ella también presenta una lesión circular en la pierna izquierda de aparición espontánea cinco días antes de la consulta.
Ninguno ha recibido tratamientos médicos previos, solo desinfección local con clorhexidina tópica dos veces al día los dos días antes de la consulta. Tampoco se conocen enfermedades aparentes.
La propietaria acusa una presentación espontánea del cuadro en los dos perros y no había observado lesiones en el gato, por lo que considera no traerlo junto a los dos perros en la primera visita. Sin embargo, debido al contexto de contagiosidad se exige verlo en consulta para evaluarlo al día siguiente.
Se realiza un examen físico general y dermatológico de cada paciente individualmente.
Perro 1
Examen físico
- Estado mental alerta, peso de 10.400 kg, índice de condición corporal (ICC) de 5/9.
- Mucosas rosadas, tiempo de relleno capilar menor a 2 segundos.
- Examen cavidad oral: correcta.
- Auscultación cardiorrespiratoria: correcta.
- Palpación abdominal sin hallazgos reseñables.
- Examen linfonodos: tamaño correcto.
Examen dermatológico
- Lesión numular de 1 cm de diámetro, alopécica y erosivoulcerativa en la cara medial del dedo II del miembro anterior derecho (Figura 1A).
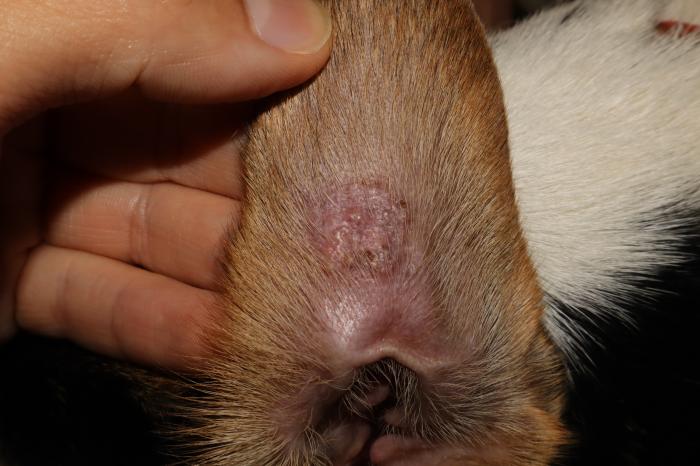
- Lesión nodular bien delimitada de 3 cm de diámetro, prominente, alopécica, erosiva, eritematosa y costrosa (tipo querion) en el labio superior derecho (Figura 1B).
- Lesión numular de 2 cm de diámetro, alopécica, eritematosa y descamativa en la cara interna del miembro torácico derecho (Figura 1C).
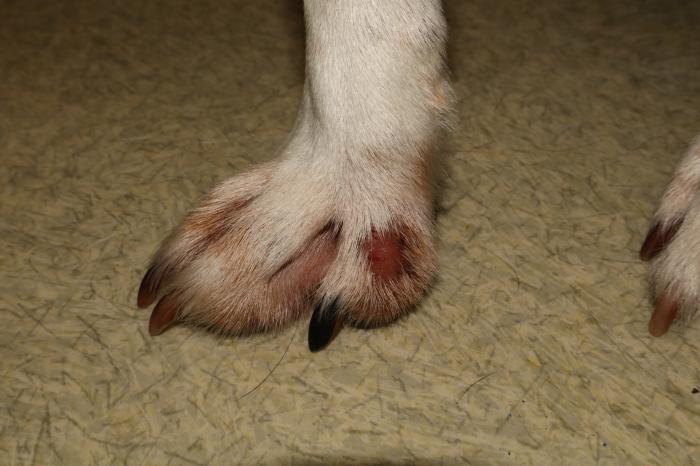
Figura 1. Perro 1 primera consulta. (A) Lesión numular, alopécica y erosivoulcerativa en la cara medial del dedo II del miembro anterior derecho. (B) Lesión nodular, prominente, alopécica, erosiva, eritematosa y costrosa. Querion dermatofítico. (C) Lesión numular, alopécica, eritematosa y descamativa en la cara interna del miembro torácico derecho.

Perro 2
Examen físico
- Estado mental alerta, peso de 7.900 kg, ICC de 5/9.
- Mucosas sonrosadas, tiempo de relleno capilar menor a 2 segundos.
- Examen cavidad oral: correcta.
- Auscultación cardiorrespiratoria: correcta.
- Palpación abdominal: sin hallazgos reseñables.
- Examen linfonodos: tamaño correcto.
Examen dermatológico
- Lesión numular bien delimitada de 3 cm de diámetro, alopécica, eritematosa y erosiva, en la cara medial del dedo II del miembro anterior derecho (Figura 2A).
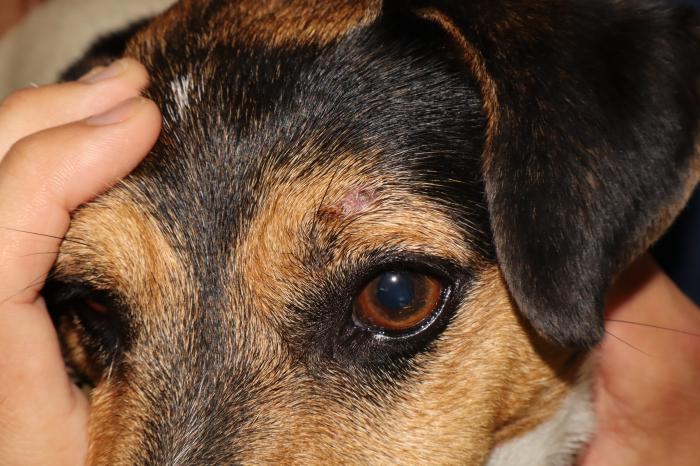
- Lesión de 1 cm alopécica y descamativa encima del párpado superior izquierdo (Figura 2B).
- Lesión bien delimitada de 2 cm, alopécica, papulosa y descamativa en la región nasal izquierda sin invadir la región mucocutánea de la trufa (Figura 2C).
- Lesión numular de 2 cm de diámetro, alopécica, papulosa, descamativa y eritematosa en la cara interna del pabellón auricular izquierdo (Figura 2D).
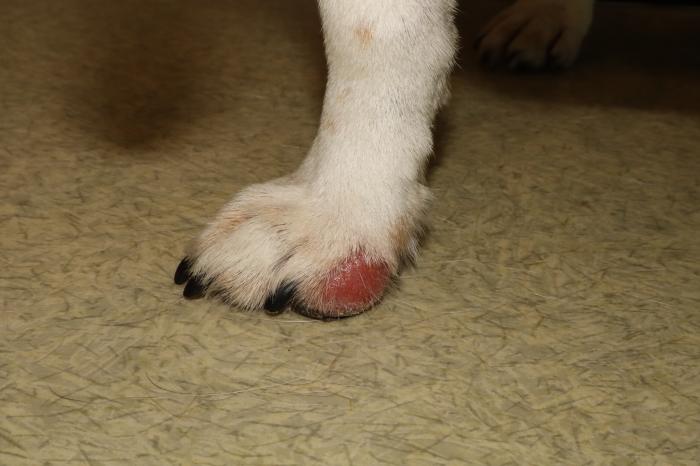
Figura 2. Perro 2 primera consulta. (A) Lesión numular, alopécica, eritematosa y erosiva, en la cara medial del dedo II del miembro anterior derecho. (B) Lesión alopécica y descamativa encima del párpado superior izquierdo. (C) Lesión alopécica, papulosa y descamativa en la región nasal. (D) Lesión numular, alopécica, papulosa, descamativa y eritematosa en la cara interna del pabellón auricular.

Gato
Examen físico
- Estado mental alerta, peso de 4.500 kg, índice de condición corporal (ICC) de 5/9.
- Mucosas sonrosadas, tiempo de relleno capilar menor a 2 segundos.
- Examen cavidad oral: correcta.
- Auscultación cardiorrespiratoria: correcta.
- Palpación abdominal: sin hallazgos reseñables.
- Examen linfonodos: tamaño correcto.
- Epífora bilateral más marcada en el ojo derecho.
Examen dermatológico
- Lesión alopécica descamativa en la región cervical de 2 cm.
- Lesión numular de 1 cm de diámetro, alopécica y descamativa en la cara externa de la oreja izquierda (no se dispone de fotos del gato).
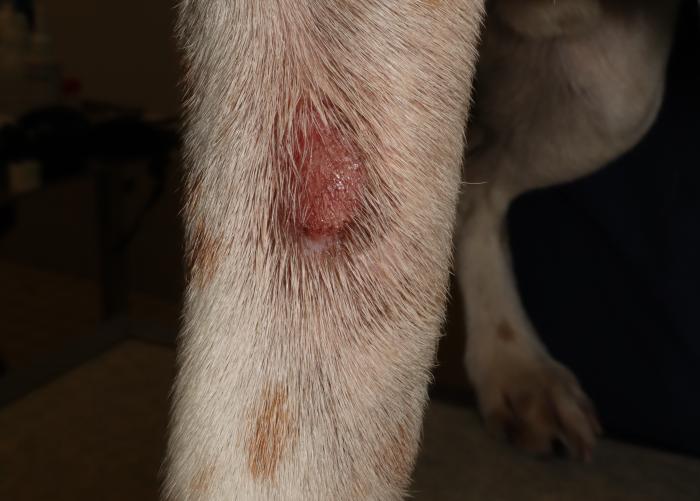
La dueña también presenta una lesión numular de 1 cm de diámetro de bordes eritematosos en el muslo de la pierna izquierda (Figura 3).
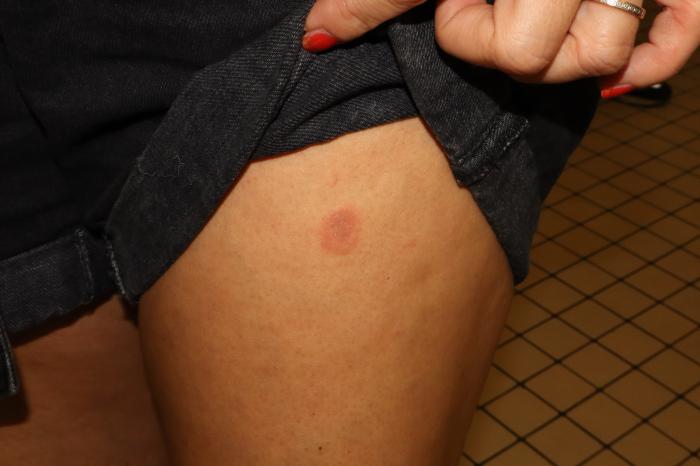
Figura 3. Lesión circular y eritematosa en la pierna de la propietaria.
Listado de problemas y diagnóstico diferencial
Se consideran los siguientes problemas principales:
- Lesiones numulares, alopécicas y no pruriginosas.
- Contagiosidad animal-animal.
- Zoonosis.
Teniendo en cuenta la anamnesis y las lesiones presentes en los 3 animales se realiza el diagnóstico diferencial con las hipótesis ordenadas de mayor a menor probabilidad:
- Dermatofitosis.
- Demodicosis.
- Foliculitis bacteriana.
- Otras ectoparasitosis con contagiosidad.
Se realizan tricogramas, citologías de superficie y se usa la lámpara de Wood para cada paciente por separado para confirmar y/o descartar los posibles diagnósticos diferenciales. Al estar correctamente desparasitados con un antiparasitario de largo espectro y tras realizar un examen microscópico del cepillado del pelo con un resultado negativo, la hipótesis de ectoparasitosis queda excluida. El tricograma para cada animal descarta la presencia de Demodex spp, mientras que resulta positivo para dermatofitosis en los 3 pacientes, con la presencia de hifas fúngicas invadiendo la médula y el córtex del pelo y la presencia de esporas fúngicas en periferia (dermatofito endoectothrix). También se toman muestras citológicas mediante aposición de la lesión nodular del labio superior y su posterior tinción con Diff-Quik revela la presencia de neutrófilos fagocitando estructuras basófilas redondas con un halo claro compatibles con esporas fúngicas. No se observan agentes bacterianos en la citología por lo que la foliculitis bacteriana queda descartada. Finalmente, se examina a cada paciente bajo la lámpara de Wood, uno de los perros y el paciente felino presentan una fluorescencia de color verde-manzana en los pelos de la periferia de las lesiones y en las vibrisas.
Diagnóstico
Tras los resultados inmediatos se pudo concluir como diagnóstico definitivo una dermatofitosis y más específicamente una infección por M. canis, debido a la fluorescencia positiva observada bajo la lámpara de Wood. De este modo no fue necesario enviar muestras para cultivo fúngico en la primera consulta.
Tratamiento y seguimiento
Se decide instaurar un tratamiento tópico a base de enilconazol (Imaveral® solución topica 100 mg/ml) para los 3 animales, utilizando una posología de dilución 1/50 (20 ml de producto en un litro de agua). Se prescribe pulverizar la totalidad del pelaje de cada animal 2 veces por semana durante 6 semanas.
Para cada perro se pauta un tratamiento sistémico por vía oral a base de ketoconazol (Fungiconazol® 200 mg comprimidos; Dechra) a una posología de 10 mg/kg/24 h durante 6 semanas.
Para el gato se instaura también un tratamiento sistémico por vía oral a base de itraconazol (Itrafungol® 10 mg/ml solución oral; Virbac) a una dosis de 5 mg/kg. La frecuencia de administración consiste en 3 periodos alternantes de 7 días consecutivos, cada uno de ellos con 7 días de reposo entre cada tratamiento. Lo que hace un total de 6 semanas de tratamiento para el felino.
Junto a esto, se aconseja emplear un sistema de aspiración para limpieza de las superficies del hogar, desinfectar el entorno con lejía doméstica y lavar los textiles en la lavadora poco cargada a una temperatura de 60 ºC, dos veces seguidas para descontaminar de manera mecánica.
La primera revisión se pauta a las 4 semanas de empezar el tratamiento para evaluar de manera general la respuesta a este último.
Se recomienda a la propietaria de los animales consultar a su médico de cabecera para el tratamiento de sus lesiones probablemente de origen dermatofítico.
Primera revisión: 4 semanas de tratamiento
Tras el primer mes de tratamiento, la respuesta es buena. El examen físico general de los 3 pacientes es normal y en el dermatológico se evidencia ausencia del eritema observado anteriormente en las lesiones y observándose hiperpigmentación (Figuras 4 a 6A-C).
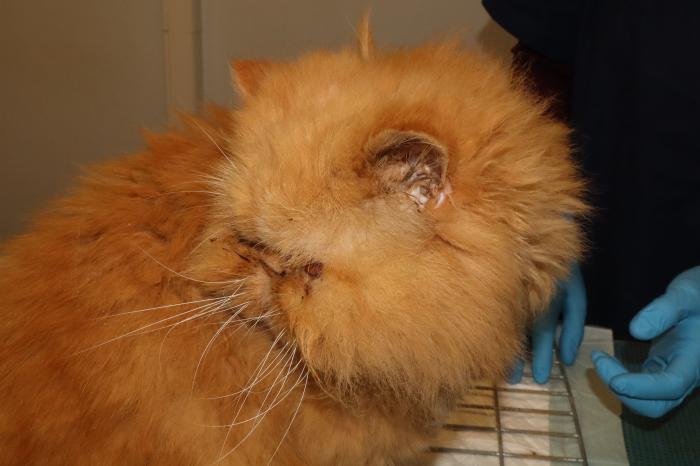
Figura 4. Gato Persa primera revisión. Ausencia de lesiones.
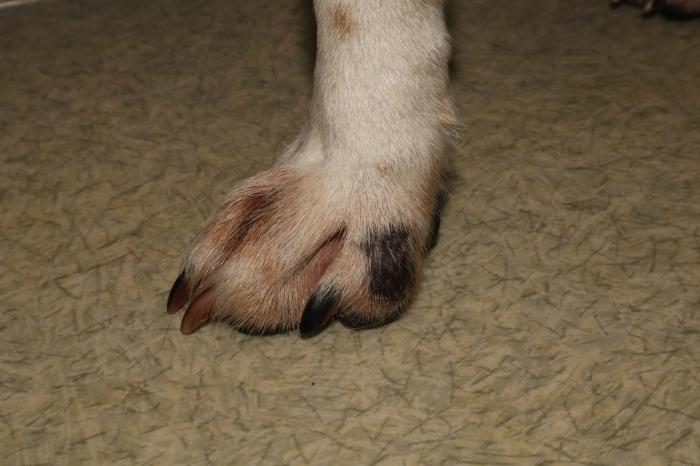
Figura 5. Perro 1 primera revisión. (A) Lesión hiperpigmentada y alopécica, en la cara medial del dedo II del miembro anterior derecho tras 4 semanas de tratamiento. (B) Alopecia e hiperpigmentación en el labio superior derecho. (C) Lesión hiperpigmentada y alopécica en la cara interna del miembro torácico derecho.

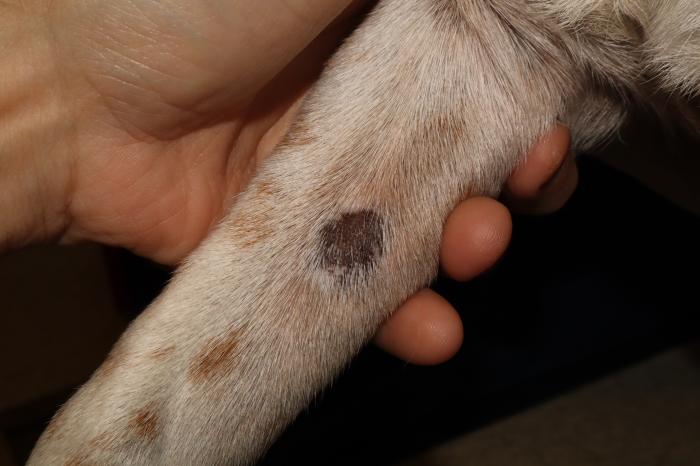
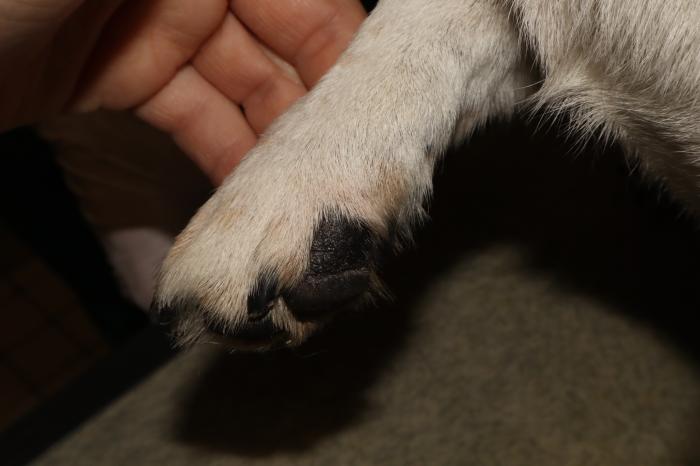
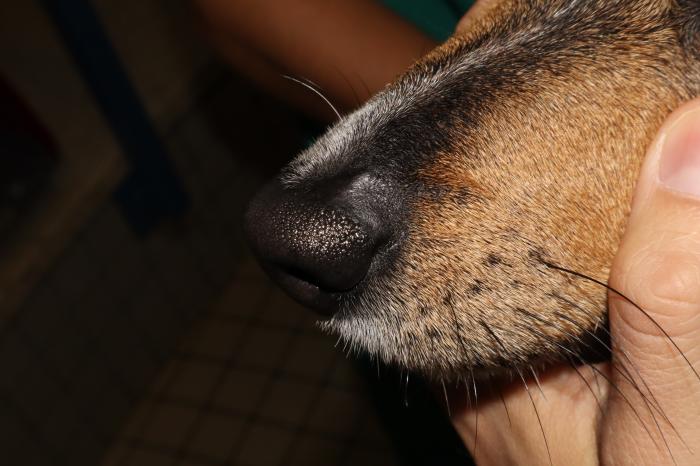
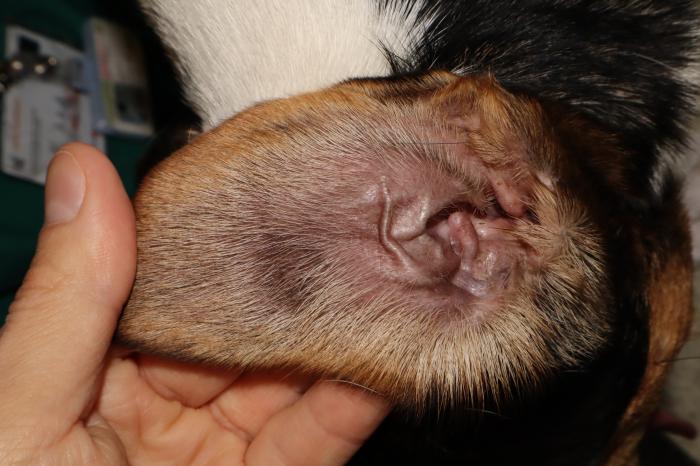
Figura 6. Perro 2 primera revisión. (A) Lesión hiperpigmentada y alopécica en la cara medial del dedo II del miembro anterior derecho. (B) Lesión hiperpigmentada en la región nasal. (C) Pabellón auricular sin anormalidades.
Se someten al examen bajo lámpara de Wood, siendo este negativo en los 3 casos. Se pauta continuar el tratamiento a la misma frecuencia para los 3 animales hasta completar 6 semanas y se prevé una revisión a las 8 semanas (15 días tras la finalización del tratamiento) para realizar el primer cultivo fúngico de control.
Segunda revisión: 2 semanas tras terminar el tratamiento. Realización de cultivo fúngico
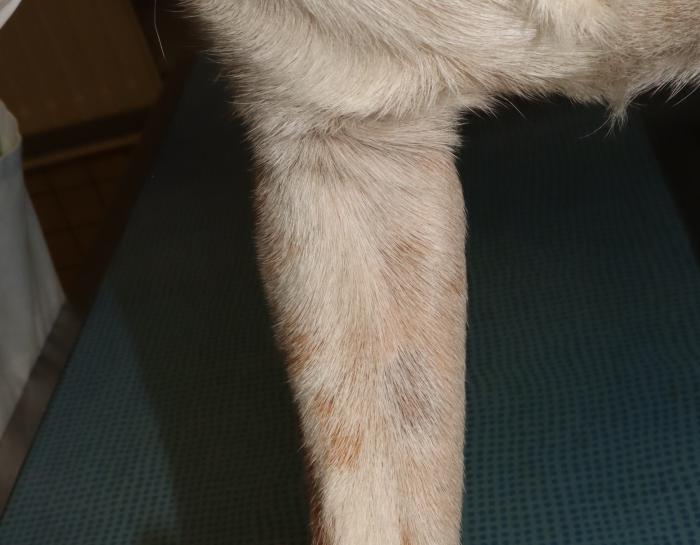
Pasados dos meses y tras 2 semanas sin tratamiento tópico y sistémico, el examen general es normal y en el dermatológico se aprecia una resolución de las lesiones cutáneas en los 3 pacientes con un crecimiento progresivo del pelo (Figura 7A-B).

Figura 7A-B. Perro 1 segunda revisión. Se aprecia un crecimiento del pelo en el lugar de las lesiones.
Se procede entonces a la toma de muestras utilizando para cada animal un trozo de moqueta estéril específico para cultivo fúngico y se envía a un laboratorio francés especializado en micología.
Resultados:
- Perros 1 y 2: negativo tras 10 días de cultivo en Agar dextrosa de Sabouraud.
- Gato: positivo tras 8 días de cultivo en Agar dextrosa de Sabouraud con 2 colonias de M. canis.
Tras estos resultados, para el gato se decide retomar el tratamiento tanto tópico como sistémico durante 6 semanas a la misma dosis y frecuencia, mientras que para los perros solo se pauta el tratamiento tópico.
- Enilconazol (Imaveral® solución tópica 100 mg/ml) para los 3 animales, utilizando una posología de 20 ml de producto en un litro de agua durante 6 semanas.
- Itraconazol (Itrafungol® 10 mg/ml solución oral; Virbac) para el gato a una dosis de 5 mg/kg de nuevo 3 periodos alternantes de 7 días consecutivos, cada uno de ellos con 7 días de reposo entre cada tratamiento.
Se prevé una nueva revisión 2 semanas tras la finalización de la pauta médica con el objetivo de realizar un segundo cultivo fúngico.
Tercera revisión. 2 semanas tras terminar el segundo ciclo de tratamiento. Realización del segundo cultivo fúngico.
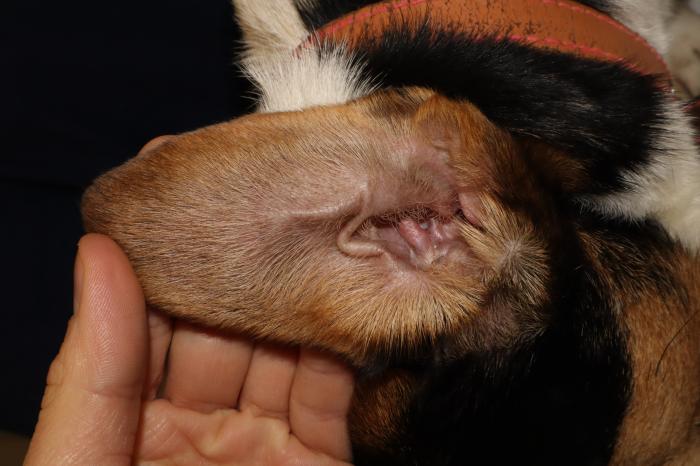
El examen clínico general y dermatológico es normal (Figuras 8A-B y 9A-B), únicamente en el perro uno se pueden apreciar lesiones cicatriciales con una hipotricosis en la zona del labio superior derecho en la lesión tipo querion (ver Figura 8A).

Figura 8. Perro 1 última revisión. (A) Se aprecia una lesión cicatricial con una hipotricosis en la zona del labio superior derecho. (B) Ausencia de lesiones.
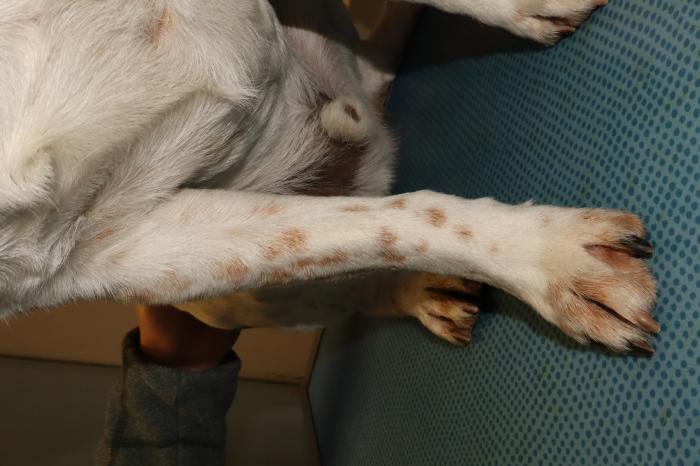
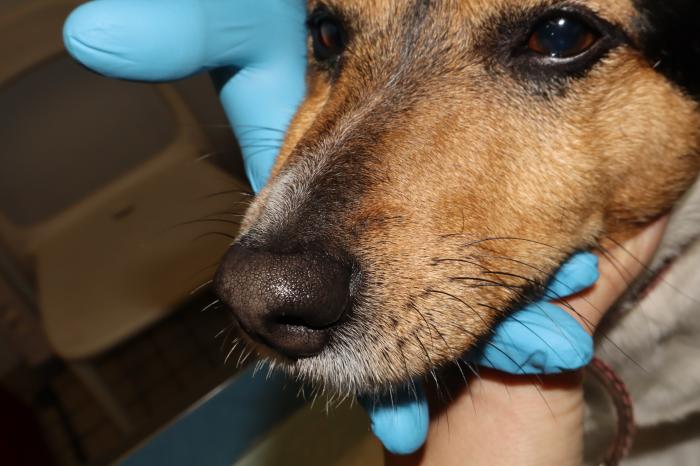
Figura 9A-B. Perro 2, última revisión. Ausencia de lesiones.
Se procede a la toma de muestras con una moqueta estéril para enviar para cultivo fúngico al mismo laboratorio. Por motivos económicos y habiendo obtenido un resultado negativo en el primer cultivo de ambos perros, se lleva a cabo la toma de muestras para cultivo solamente en el gato Persa.
El resultado es negativo tras 20 días de cultivo en agar dextrosa de Sabouraud. En base a este resultado, se recomienda a la propietaria realizar un segundo cultivo con un mes de intervalo para confirmar la cura micológica.
Discusión
Para el diagnóstico de una dermatofitosis es necesario una confirmación rápida para comenzar con un tratamiento que limite el contagio entre animales y personas. Existen numerosas pruebas diagnósticas y aunque el cultivo fúngico se considera el gold standard tiene la desventaja de proporcionar un resultado diferido. Por ello, los otros exámenes, aunque son menos sensibles, resultan muy interesantes para el clínico. Se pueden realizar múltiples exámenes complementarios de fácil alcance y ejecución para el clínico que nos pueden dar resultados fiables de inmediato. Entre ellos y, los que se realizan más comúnmente en clínica veterinaria, son el examen bajo la lámpara de Wood que emplea luz ultravioleta de onda larga y el tricograma para análisis del pelo al microscopio. El principal dermatofito de interés veterinario que produce fluorescencia verde-manzana bajo la lámpara de Wood es M. canis. La fluorescencia se debe a la producción y a la interacción química de un metabolito llamado pteridina tras la invasión fúngica11,12. En el presente caso, al visualizarse una fluorescencia verde manzana y tras confirmar la infección fúngica del tallo piloso al microscopio se concluye una infección activa por M. canis en los 3 animales del hogar, por lo que no se considera necesario el diagnóstico mediante cultivo fúngico.
Para el seguimiento de la respuesta clínica al tratamiento se tienen en cuenta principalmente la clínica y el cultivo fúngico. La lámpara de Wood puede dar resultados positivos por persistencia de pteridina en el ápex del pelo. Además, los autores indican también la importancia de mirar el número de unidades formadoras de colonias para monitorizar el tratamiento13,15. Hasta hace unos años, se consideraba como cura micológica la obtención de 2 cultivos negativos separados de 2 semanas. Sin embargo, recientemente se ha demostrado que, si se cumplen las recomendaciones de tratamiento tópico y sistémico junto a una buena limpieza ambiental, asociado a la obtención de un único cultivo fúngico negativo en un animal sin lesiones, se puede determinar la cura micológica en el 90 % de los casos en una infección por M. canis16. En nuestro caso, el gato Persa no presenta lesiones clínicas aparentes tras la finalización del primer tratamiento, pero el primer cultivo es positivo con el crecimiento de 2 unidades formadoras de colonias. En este caso, tras evaluar el correcto cumplimiento del protocolo establecido se valora la repetición de un nuevo ciclo de tratamiento de 6 semanas y se lleva a cabo un segundo cultivo de seguimiento tras 8 semanas. Ante esta situación compleja (contagio de dos perros, un gato de pelo largo y su propietaria) se considera oportuno la obtención de dos cultivos fúngicos negativos a un mes de intervalo para confirmar la cura micológica.
Desde un punto de vista clínico, la limpieza rutinaria profunda del hogar junto a una terapia multimodal resulta esenciales para el éxito del tratamiento. La limpieza y desinfección medioambiental minimiza el riesgo de contagio entre animales y personas, así como la obtención de resultados falsos positivos provocados por los residuos fúngicos ambientales presentes en el hogar17.
Los gatos de pelo largo, y especialmente el gato Persa, aparecen predispuestos a la dermatofitosis por M. canis6,18. Por ello se valora el interés del rasurado. Algunos autores proponen esta técnica como un método eficaz en la limitación de la propagación de las esporas en el medio ambiente, minimizando así el contagio a las personas y entre animales19,21. Además, podría facilitar la aplicación del tratamiento tópico, aumentando así la penetración de los antifúngicos. Sin embargo, la ejecución de esta técnica genera cierta controversia. Por un lado, provoca estrés y en muchos casos debe acompañarse de una sedación del paciente. Además, requiere una precisión minuciosa, para evitar ocasionar microtraumatismos en la piel que podrían favorecer la propagación de la infección, así como una escrupulosa limpieza y desinfección del material y el espacio de intervención con el fin de parar la circulación de residuos contagiosos9,15,22. Por consiguiente, en este caso, se decide no llevar a cabo la técnica de rasurado.
Aunque M. canis cause generalmente lesiones superficiales debido a su invasión del estrato córneo, del pelo y del folículo piloso, en ocasiones este patógeno también puede provocar lesiones más inflamatorias que cursan con la destrucción del folículo piloso (forunculosis) dando lugar a lesiones nodulares denominadas querion23. Es probable que esto haya sucedido en la lesión presente en el labio superior del perro uno (ver Figura 1B). En estas circunstancias no se debe esperar el crecimiento completo del pelo en la zona afectada tras la cura sino más bien el desarrollo de una lesión cicatricial, como se observa en este caso.
Bibliografía
- Moriello KA and DeBoer DJ. Dermatophytosis. In: Greene CE (ed). Infectious diseases of the dog and cat. 4th ed. St Louis: Elsevier, 2012, pp 588–602
- Scott, D. W., & Paradis, M. (1990). A survey of canine and feline skin disorders seen in a university practice: Small Animal Clinic, University of Montréal, Saint-Hyacinthe, Québec (1987-1988).The Canadian veterinary journal = La revue veterinaire canadienne, 31(12), 830–835.
- Lewis DT, Foil CS, Hosgood G. Epidemiology and clinical fea- tures of dermatophytosis in dogs and cats at Louisiana State University: 1981–1990. Vet Dermatol 1991; 2: 53–58.
- MacKay B, Johnstone I, OBoyle D et al. Severe dermatophyte infections in a dog and cat. Aust Vet Pract 1997; 27: 86–90.
- Cafarchia, C., Romito, D., Sasanelli, M., Lia, R., Capelli, G., & Otranto, D. (2004). The epidemiology of canine and feline dermatophytoses in southern Italy. Mycoses,47(11- 12), 508–513. https://doi.org/10.1111/j.1439-0507.2004.01055.x
- Moriello, K. A., Coyner, K., Paterson, S., & Mignon, B. (2017a). Diagnosis and treatment of dermatophytosis in dogs and cats.: Clinical Consensus Guidelines of the World Association for Veterinary Dermatology. Veterinary dermatology, 28(3), 266– e68. https://doi.org/10.1111/vde.12440
- Sparkes, A. H., Werrett, G., Stokes, C. R., & Gruffydd-Jones, T. J. (1994). Improved sensitivity in the diagnosis of dermatophytosis by fluorescence microscopy with calcafluor white. The Veterinary record, 134(12), 307–308. https://doi.org/10.1136/vr.134.12.307
- Sparkes, A. H., Gruffydd-Jones, T. J., Shaw, S. E., Wright, A. I., & Stokes, C. R. (1993). Epidemiological and diagnostic features of canine and feline dermatophytosis in the United Kingdom from 1956 to 1991. The Veterinary record, 133(3), 57–61. https://doi.org/10.1136/vr.133.3.57
- Frymus, T., Gruffydd-Jones, T., Pennisi, M. G., Addie, D., Belák, S., Boucraut-Baralon, C., Egberink, H., Hartmann, K., Hosie, M. J., Lloret, A., Lutz, H., Marsilio, F., Möstl, K., Radford, A. D., Thiry, E., Truyen, U., & Horzinek, M. C. (2013). Dermatophytosis in cats: ABCD guidelines on prevention and management. Journal of feline medicine and surgery, 15(7), 598–604. https://doi.org/10.1177/1098612X13489222
- Colombo, S., Cornegliani, L., & Vercelli, A. (2001). Efficacy of itraconazole as a combined continuous/pulse therapy in feline dermatophytosis: preliminary results in nine cases. Veterinary dermatology, 12(6), 347–350. https://doi.org/10.1046/j.0959- 4493.2001.00274.x
- Wolf, F.T., Jones, E.A., & Nathan, H.A. (1958). Fluorescent Pigment of Microsporum. Nature, 182, 475-476.
- Foresman, A. H., & Blank, F. (1967). The location of the fluorescent matter in Microsporon infected hair. Mycopathologia et mycologia applicata, 31(3), 314–318. https://doi.org/10.1007/BF02053431
- Dawson, C. O., & Noddle, B. M. (1968). Treatment of Microsporum canis ringworm in a cat colony. The Journal of small animal practice, 9(12), 613–620. https://doi.org/10.1111/j.1748-5827.1968.tb06784.x
- Carlotti, D. N., Guinot, P., Meissonnier, E., & Germain, P. A. (2010). Eradication of feline dermatophytosis in a shelter: a field study. Veterinary dermatology, 21(3), 259– 266. https://doi.org/10.1111/j.1365-3164.2009.00789.x
- Moriello K. (2014). Feline dermatophytosis: aspects pertinent to disease management in single and multiple cat situations. Journal of feline medicine and surgery, 16(5), 419–431. https://doi.org/10.1177/1098612X14530215
- Stuntebeck, R. L., & Moriello, K. A. (2020). One vs two negative fungal cultures to confirm mycological cure in shelter cats treated for Microsporum canis dermatophytosis: a retrospective study. Journal of feline medicine and surgery, 22(6), 598–601. https://doi.org/10.1177/1098612X19858791
- Moriello KA. Decontamination of 70 foster family homes exposed to Microsporum canis infected cats: a retrospective study. Vet Dermatol. 2019 Apr;30(2):178-e55. doi: 10.1111/vde.12722. Epub 2019 Feb 6. PMID: 30729598
- Zimmerman, K., Feldman, B., Robertson, J., Herring, E. S., & Manning, T. (2003). Dermal mass aspirate from a Persian cat. Veterinary clinical pathology, 32(4), 213– 217. https://doi.org/10.1111/j.1939-165x.2003.tb00339.x
- DeBoer, D. J., & Moriello, K. A. (1994). Development of an experimental model of Microsporum canis infection in cats. Veterinary microbiology, 42(4), 289–295. https://doi.org/10.1016/0378-1135(94)90060-4
- DeBoer, D. J., & Moriello, K. A. (1995). Inability of two topical treatments to influence the course of experimentally induced dermatophytosis in cats. Journal of the American Veterinary Medical Association, 207(1), 52–57.
- Moriello, K. A., & DeBoer, D. J. (1995). Efficacy of griseofulvin and itraconazole in the treatment of experimentally induced dermatophytosis in cats. Journal of the American Veterinary Medical Association, 207(4), 439–444.
- Moriello K. A. (2017b). Decontamination of carpet exposed to Microsporum canis hairs and spores. Journal of feline medicine and surgery, 19(4), 435–439. https://doi.org/10.1177/1098612X16634390
- Cornegliani, L., Persico, P., & Colombo, S. (2009). Canine nodular dermatophytosis (kerion): 23 cases. Veterinary dermatology, 20(3), 185–190. https://doi.org/10.1111/j.1365-3164.2009.00749.
 by Multimédica
by Multimédica