Diabetes mellitus felina: emergencias más frecuentes y estrategias de intervención
Resumen breve
En la primera parte del artículo publicado en el número 15 de Clinfelivet se publicó un repaso sobre la diabetes mellitus (DM) felina y los avances más recientes en el manejo exitoso de esta enfermedad. En esta segunda parte, se abordarán las presentaciones más frecuentes en felinos diabéticos que acuden a la sala de urgencias, y se revisará la literatura sobre el mejor abordaje terapéutico en estos casos.Índice de contenidos

Introducción
En la primera parte del artículo publicado en el número 15 de Clinfelivet se publicó un repaso sobre la diabetes mellitus (DM) felina y los avances más recientes en el manejo exitoso de esta enfermedad. En esta segunda parte, se abordarán las presentaciones más frecuentes en felinos diabéticos que acuden a la sala de urgencias, y se revisará la literatura sobre el mejor abordaje terapéutico en estos casos.
Las complicaciones más comunes encontradas en la sala de urgencias son:
- Hipoglucemia.
- Cetoacidosis diabética.
- Síndrome hiperglucémico hiperosmolar.
- Cetoacidosis diabética euglucémica.
Hipoglucemia
Es la complicación más frecuente en humanos diabéticos en tratamiento con insulina, con una prevalencia del 30 %¹.
El manejo de la DM en gatos presenta múltiples desafíos. Uno de los objetivos principales al iniciar el tratamiento con insulina es mantener la glucemia dentro de un rango ideal, evitando episodios de hipoglucemia (<65 mg/dl). Al mismo tiempo, es fundamental prevenir episodios prolongados de hiperglucemia, ya que estos pueden desencadenar complicaciones metabólicas.
Evitar la hipoglucemia es de suma importancia, no solo por sus implicaciones clínicas y el riesgo vital que representa, sino también porque los episodios crónicos de hipoglucemia moderada pueden generar consecuencias adicionales. En humanos, se ha descrito la incapacidad para activar una respuesta contrarreguladora, la ausencia de signos clínicos previos al desarrollo de neuroglucopenia y un mayor riesgo de hipoglucemia severa. Estos efectos adversos también han sido observados en otras especies, y actualmente se investigan en gatos.
La hipoglucemia episódica puede inducir una adaptación progresiva del organismo a niveles de glucosa inferiores al umbral normal. Este fenómeno reduce gradualmente el umbral hipoglucémico, lo que permite que el paciente tolere concentraciones más bajas sin signos clínicos leves. Como consecuencia, pueden presentarse signos graves de forma súbita, como convulsiones, coma o muerte secundaria a neuroglucopenia. Este mecanismo adaptativo explica por qué algunos pacientes con glucosa de 40 mg/dl no muestran signos clínicos, mientras que otros, con valores inferiores a 20 mg/dl, solo presentan letargia, ataxia y depresión mental. En pacientes con una respuesta contrarreguladora normal, una glucemia de ese nivel se asociaría típicamente a coma o estupor².
Otros signos clínicos observados en felinos hipoglucémicos incluyen vocalización, jadeo, hipotermia, bradicardia, convulsiones, contracciones musculares involuntarias, diarrea e hipersalivación².
Viebrock et al. describieron que la mayoría de los pacientes con DM e hipoglucemia habían presentado vómito posterior a la ingesta, seguido por la administración de la dosis habitual de insulina. Algunos casos correspondían a sobredosis de insulina, mientras que otros pacientes habían ingerido una cantidad menor de alimento de lo habitual, sin un ajuste en la dosis de insulina.
Para detectar y tratar oportunamente episodios de hipoglucemia, es fundamental educar a los propietarios sobre los signos clínicos, así como la forma adecuada de actuar mientras se dirigen a un centro veterinario.
Como manejo inicial en el hogar, ante la sospecha de una crisis hipoglucémica, se recomienda aplicar miel o gel de glucosa sobre las mucosas del paciente. Al llegar al centro veterinario, el tratamiento debe comenzar con la colocación de un catéter intravenoso y la administración de glucosa a razón de 0.5-1 ml/kg de dextrosa al 50 %, diluida 1:2 con solución salina. Es importante tener en cuenta que esta solución es hipertónica y puede ocasionar flebitis.
El objetivo del tratamiento es eliminar los signos clínicos, recordando que la neuroglucopenia severa y prolongada puede causar daño neuronal irreversible.
Si el paciente está alerta y puede ingerir alimento, se recomienda ofrecer pequeñas cantidades de comida de forma frecuente. En caso de que el paciente no pueda comer o si la hipoglucemia persiste a pesar de la alimentación, se debe iniciar una infusión continua de dextrosa al 2.5-5 %, hasta que el paciente mantenga niveles adecuados de glucosa sérica sin requerir suplementación.
En los casos en los que la hipoglucemia sea secundaria a una sobredosis de insulina, se debe suspender su administración hasta que los niveles séricos de glucosa indiquen su reintroducción. El efecto hipoglucemiante puede durar horas o incluso días, independientemente del tipo o la cantidad de insulina utilizada³. Durante este periodo, el paciente debe permanecer hospitalizado con suplementación de dextrosa intravenosa y monitoreo continuo de la glucemia.
Estudios sugieren que los felinos obesos y aquellos que reciben más de 6 U de insulina en total, una o dos veces al día, tienen mayor predisposición a desarrollar crisis hipoglucémicas³.
Asimismo, es importante considerar que la insulina puede alterar el equilibrio de diversos electrolitos. En casos de sobredosis, estos desequilibrios deben corregirse adecuadamente, ya que concentraciones bajas pueden provocar complicaciones metabólicas adicionales. En estas situaciones, también puede ser necesario el uso de antagonistas de la insulina, como glucagón o corticosteroides.
El glucagón debe administrarse siguiendo las instrucciones del fabricante para su correcta dilución. Se recomienda un bolo inicial de 50 ng/kg IV, seguido de una infusión continua de 5-10 ng/kg/min, ajustado según efecto. Un estudio reciente demostró que la administración transmucosa de glucagón (intranasal o intrarectal) incrementa los niveles de glucosa plasmática en felinos sanos³. Entre los efectos adversos observados se incluyen estornudos, vómitos, hipersalivación y blefaroespasmo. Se requieren más estudios para evaluar la eficacia de esta vía en pacientes diabéticos e hipoglucémicos, ya que podría convertirse en una herramienta útil para crisis hipoglucémicas en casa.
En cuanto a los esteroides, puede administrarse dexametasona a una dosis inicial de 0.1-0.2 mg/kg IV, seguida por 0.05-0.1 mg/kg/12 h.
Cuando el paciente requiere nuevamente la administración de insulina, es prudente reiniciar con una dosis reducida del 25 al 50 % de la dosis previa, con monitorización estrecha para evaluar la respuesta inicial.
Es importante recordar que algunos felinos diabéticos pueden entrar en remisión. En estos casos, una crisis de hipoglucemia puede desencadenarse como consecuencia de la administración de insulina en un paciente normoglucémico que previamente era diabético. Por este motivo, es fundamental evaluar y monitorizar de forma individual cada caso, a fin de identificar aquellos pacientes que ya no requieren insulina debido a una remisión clínica.
Los pacientes que muestran mejoría clínica dentro de las primeras 12 horas de hospitalización tienen un pronóstico más favorable, independientemente de su estado neurológico al ingreso o de sus niveles iniciales de glucosa⁴.
Si es necesario, se debe ampliar el protocolo diagnóstico con el objetivo de identificar posibles comorbilidades, y el tratamiento debe ajustarse en función de los hallazgos. Asimismo, es fundamental reevaluar el tipo de dieta ofrecida, priorizando una alimentación palatable y adaptada a las preferencias del paciente, con el fin de garantizar una ingesta nutricional adecuada y sostenida.
Cetoacidosis diabética (CAD)
La American Diabetes Association la define como una condición en la que hay glucosa >200 mg/dl, acidemia (pH <7.3), bicarbonato disminuido (<15 mmol/l), acompañada de cetonemia y cetonuria.
La insulina facilita el ingreso de glucosa al interior de la célula, donde es utilizada para la producción de trifosfato de adenosina, generando energía. Simultáneamente, la insulina también promueve el transporte de electrolitos, como el potasio plasmático, hacia el interior celular.
Cuando existe una deficiencia absoluta o relativa de insulina, la glucosa no puede ingresar a las células, lo que genera un estado de inanición celular. En respuesta, el organismo recurre a fuentes alternativas de energía, entre ellas la lipólisis, activada por la enzima lipasa sensible a hormonas (LSH). Este proceso produce la oxidación de ácidos grasos libres, generando cuerpos cetónicos (CC) a nivel hepático, los cuales son utilizados como fuente energética.
Existen tres tipos principales de CC: β -hidroxibutirato (BHB), acetoacetato y acetona. Cuando hay una sobreproducción de CC, el sistema buffer plasmático se satura, dando lugar a acidosis metabólica, que a su vez compromete el metabolismo celular. La hiperglucemia y el aumento en la filtración renal de cuerpos cetónicos provocan una diuresis osmótica marcada, la cual conduce a deshidratación y desequilibrio electrolítico. En los casos más graves, la CAD puede ser potencialmente fatal.
El examen físico suele revelar signos compatibles con hipoperfusión, tales como alteración del estado mental, pulso débil y tiempo de llenado capilar prolongado. También se observan signos de deshidratación, y en algunos casos, un característico olor dulce proveniente de la boca, atribuible al aumento de acetona⁵.
Desde el punto de vista laboratorial, se identifica hiperglucemia severa, cetonemia y/o cetonuria, con acidosis metabólica.
Es fundamental tener en cuenta que los pacientes con CAD pueden presentar comorbilidades, tales como pancreatitis aguda, lipidosis hepática, colangiohepatitis, infección del tracto urinario o enfermedad renal crónica, las cuales deben ser identificadas y tratadas de forma simultánea a la CAD.
El manejo principal de la cetoacidosis diabética se divide en tres componentes fundamentales:
- Fluidoterapia.
- Reemplazo de electrolitos.
- Administración de insulina.
A diferencia de los perros, los felinos tienen una mayor predisposición a desarrollar sobrecarga de fluidos, por lo que la resucitación debe ser más restrictiva y monitorizada cuidadosamente. Además, es importante considerar el efecto de la hipotermia sobre la circulación vascular.
En pacientes con hipotensión (presión sistólica <60 mmHg), se recomienda administrar un bolo intravenoso de cristaloides isotónicos (p. ej., Hartmann) a una dosis de 10 ml/kg en un lapso de 10 a 15 minutos. La fluidoterapia debe continuar de acuerdo con los cálculos de deshidratación en base con la fórmula siguiente:
Deshidratación (ml): % deshidratación x peso corporal (kg) x 1000 ml
Así como los requerimientos de mantenimiento y pérdidas activas (vómito, diarrea).
El calentamiento activo debe iniciarse una vez que la presión sistólica alcance al menos 60 mmHg. Al alcanzar una temperatura rectal de 36.7 °C, se debe reevaluar la presión sistólica. Si la hipotensión persiste, se administrará un segundo bolo de cristaloides. En caso de continuar hipotenso con temperatura rectal normal, se debe considerar la administración de vasopresores.
Como cristaloides isotónicos preferidos se recomienda el uso de Hartmann®, Plasmalyte® o Normosol-R®. No se aconseja el uso de solución salina al 0.9 %, debido a la ausencia de buffer y su efecto acidótico, que puede empeorar la acidemia y retardar la mejoría clínica.
Algunos clínicos prefieren la solución salina para corregir la hiponatremia que presentan estos pacientes; sin embargo, esta hiponatremia es frecuentemente pseudohiponatremia causada por la hiperglucemia. La hiperglucemia eleva la osmolaridad plasmática, lo que provoca un desplazamiento de líquido hacia el espacio extracelular como mecanismo compensatorio, diluyendo el sodio plasmático. Esta pseudohiponatremia no requiere corrección directa, ya que el sodio plasmático regresa a niveles normales conforme disminuye la glucosa con el tratamiento adecuado.
Para distinguir entre hiponatremia real o dilucional, se recomienda calcular el sodio corregido con la siguiente fórmula:
Na+ corregido: Na+ medido (mEq/l) + [1.6 x [(glucosa plasmática (mg/dl) – 100)/100]]
Se recomienda realizar hematología, bioquímica sanguínea con electrolitos, medición de cuerpos cetónicos plasmáticos, lactato, gasometría venosa y perfil tiroideo. La medición de CC plasmáticos (β-hidroxibutirato) es más precisa para el diagnóstico y seguimiento (Figura 1); un valor >2.4 mmol/l es indicativo de cetonemia significativa. El uso de tiras reactivas en orina para la detección de CC evalúa la reacción con nitroprusiato, detectando acetoacetato, pero no mide β-hidroxibutirato, que es el cuerpo cetónico más importante.
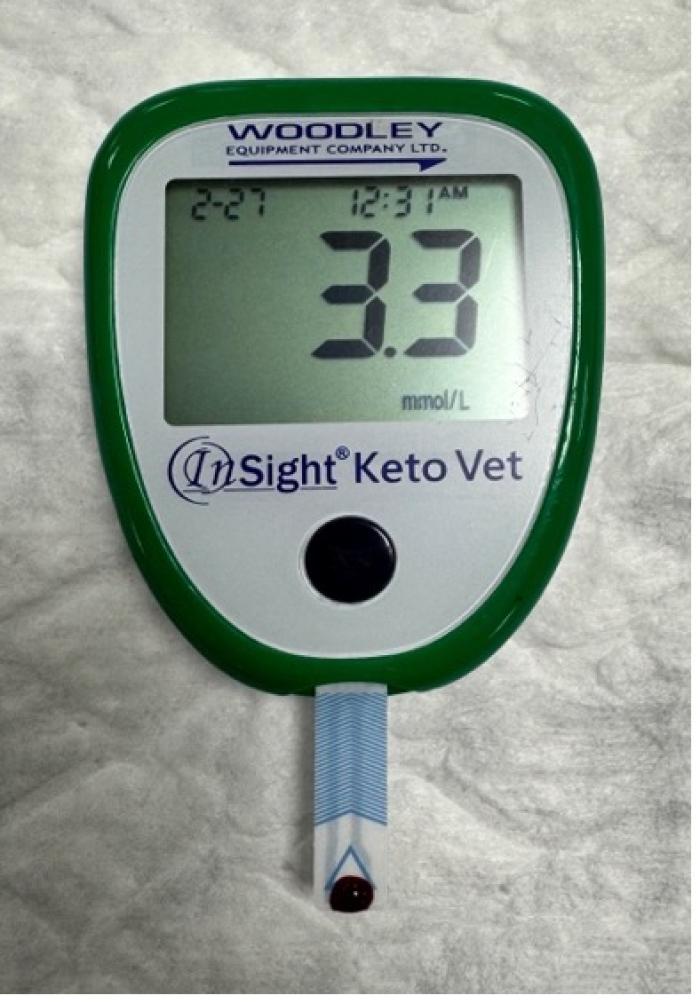
Figura 1. Medición de β-hidroxibutirato en sangre utilizando un medidor portátil InSight® Keto Vet (Woodley Equipment Company Ltd.). El resultado muestra una concentración de 3.3 mmol/l, compatible con cetonemia significativa.
Se debe tener precaución con la toma frecuente de sangre, pues puede inducir anemia. Como alternativa, se pueden utilizar sistemas de monitorización continua de glucosa (p. ej., Freestyle®) (Figura 2) o glucómetros portátiles (p. ej., AlphaTrak®), que requieren un volumen pequeño de sangre (0.3 µl).
Figura 2. Sensor FreeStyle Libre 3®, un sistema de monitoreo continuo de glucosa diseñado originalmente para humanos, que también puede emplearse en gatos diabéticos. Este dispositivo permite la medición en tiempo real de los niveles de glucosa intersticial, facilitando un manejo más preciso y menos invasivo de la diabetes felina.
Las anomalías en potasio, fósforo y sodio son frecuentes. Los déficits de potasio se deben a diuresis osmótica, vómito y pérdidas urinarias. La deficiencia de insulina y la acidosis metabólica producen un desplazamiento de potasio desde el espacio intracelular hacia el extracelular, lo que puede enmascarar la verdadera deficiencia corporal de potasio. Al iniciar el tratamiento con fluidoterapia e insulina, el potasio retorna al espacio intracelular, pudiendo producir hipocalemia.
La hipocalemia severa puede ocasionar debilidad muscular, arritmias cardíacas, insuficiencia respiratoria e incluso la muerte. Se recomienda iniciar la suplementación de potasio cuando sus niveles están bajos o en el límite inferior, salvo en pacientes anúricos o con hipercalemia. Es aconsejable utilizar una línea de fluidoterapia separada para potasio, evitando sobredosis cuando la fluidoterapia se ajuste. En casos de hipocalemia refractaria acompañada de debilidad progresiva, letargia, anorexia o convulsiones, es necesario medir los niveles de magnesio.
Los niveles bajos de fósforo son atribuibles a la diuresis osmótica; valores <1.5 mg/dl pueden provocar hemólisis. Se recomienda la suplementación antes de iniciar la insulinoterapia (Tabla 1).
| Electrolito | Suplementación IV | Contraindicaciones |
|---|---|---|
| K+ sérico mEq/l | ||
| >5 4-5 3.5-4 3-3.5 2.5-3 2-2.5 <2 | No suplementar No suplementar 20 mEq/l 30 mEq/l 40 mEq/l 60 mEq/l 80 mEq/l | Hipercalemia asociada con fallo renal oligúrico |
| PO43- sérico mg/dl | ||
| 2-2.9 <2 | 0.06 mmol/kg/h 0.12 mmol/kg/h | Hiperfosfatemia, hipercalcemia, oliguria, necrosis de los tejidos |
| Mg3- sérico mg/dl | ||
| 1.6-1.9 <1.6 | 0.5 mEq/kg/24 h 1 mEq/kg/24 h | Pacientes con daño miocárdico Bloqueo cardíaco atrio ventricular Enfermedad renal |
| La suplementación de K+ no debe exceder de 0.5 mEq/kg/h Suplementar PO₄³⁻ con fluidos libres de calcio. Se puede encontrar como una solución que contiene K+; en ese caso, se debe calcular la cantidad total de K+ que se administrará para evitar sobredosis |
Tabla 1. Guía para la suplementación de electrolitos en pacientes con CAD.
La terapia con insulina debe iniciarse cuando la perfusión y las alteraciones electrolíticas hayan sido corregidas; no es necesario esperar a que el paciente esté completamente hidratado. El objetivo es mantener la glucemia entre 100-250 mg/l, con una disminución gradual de 50 a 75 mg/dl/h, evitando cambios bruscos en la osmolaridad plasmática. En caso de ser necesario, se administra dextrosa por vía intravenosa para evitar hipoglucemias. Con este manejo, se restaura la utilización normal de glucosa a nivel celular y se estimula el metabolismo de los CC, contribuyendo a la resolución de la acidemia.
Se ha observado que la administración de insulina después de las primeras 6 horas de admisión retrasa la resolución de la cetonemia, en comparación con la administración temprana dentro de las primeras 6 horas6.
Existen diversos protocolos publicados para la administración de insulina:
- Insulina intravenosa en infusión continua:esta técnica fue descrita por primera vez en 1993 por el Dr. Douglas MacIntire y es considerada el estándar de cuidado en humanos y en muchos hospitales veterinarios. Se utiliza insulina regular con dosis entre 1.1 y 2.2 U/kg/24 h. Un estudio reciente demostró que una dosis de 2.2 U/kg/24 h no produjo efectos adversos. También se han publicado estudios con insulina lispro7, mostrando buenos resultados sin efectos adversos. La glucemia se monitoriza cada 1-2 horas y la administración de insulina se ajusta según los valores de glucosa plasmática (Tabla 2).
| |||
| Glucosa sanguínea (mg/dl) | Suplementación con dextrosa | Dosis de insulina (U/kg/h) | Velocidad infusión insulina |
| >250 | Cristaloide solo | 0.09 | 10 ml/h |
| 200-250 | 2.5 % | 0.064 | 7 ml/h |
| 150-199 | 2.5 % | 0.045 | 5 ml/h |
| 100-149 | 5 % | 0.045 | 5 ml/h |
| <100 | 5 % | Suspender | Suspender |
Tabla 2. Protocolo de insulina regular en infusión continua intravenosa. Esta tabla es una guía solamente, el objetivo es reducir la glucosa 50-75 mg/dl/h para evitar el riesgo de edema cerebral. Fuente: Gal A, Odunayo A. Diabetes Ketoacidosis and Hyperosmolar Hyperglycemic Syndrome in Companion Animals. Vet Clin North Am Small Anim Pract. 2023 May;53(3):531-550.
- Insulina glargina subcutánea con insulina regular8: glargina 0.25 U/kg/12 h y se administra insulina regular dependiendo de la glucemia:
- Si la glucosa es >250 mg/dl: insulina regular 1 U/gato/6 h IM.
- Si la glucosa está entre 80 y 249 mg/dl: se suplementa la fluidoterapia con dextrosa al 2.5 %.
- Si la glucosa es <80 mg/dl: se administra un bolo intravenoso de dextrosa 50 % (0.5-1 ml/kg) y se suplementan la fluidoterapia con dextrosa al 5 %.
- Glargina intramuscular, con o sin administración concurrente de glargina subcutánea9. El estudio recomienda una dosis inicial de glargina subcutánea de 1-2 U/gato/12 h, concurrentemente con glargina intramuscular 0.5-1 U/gato/4 h hasta alcanzar un control glucémico adecuado (180-252 mg/dl). Se recomienda iniciar la administración de insulina después de algunas horas con fluidoterapia, ya que la absorción puede verse afectada en casos de deshidratación. Lo más relevante de este estudio es que todos los pacientes resolvieron la CAD y fueron dados de alta, algunos entraron en remisión, lo que ofrece una alternativa a la eutanasia cuando las limitaciones financieras son un factor.
- Insulina regular intramuscular: dosis inicial de 0.1-0.2 U/kg IM seguida de 0.1 U/kg/1-2 h IM; cuando la glucemia es <250 mg/dl, continuar con 0.1-0.3 U/kg/4-6 h IM o SC 6-8 h. Se añade dextrosa 5 % a la fluidoterapia cuando la glucemia está entre 150-300 mg/dl hasta que se resuelva la CAD.
La fluidoterapia y la administración de insulina suelen ser efectivas para resolver la acidosis. La administración de bicarbonato de sodio solo está recomendada en casos específicos, cuando el bicarbonato plasmático continúa siendo <11 mEq/l después de varias horas de fluidoterapia.
La literatura recomienda la monitorización de hidratación, electrolitos y cuerpos cetónicos cada 4 horas, y gasometría cada 8-12 horas, para evaluar la evolución del paciente y ajustar la terapia según sea necesario. Sin embargo, en muchos casos existen limitaciones económicas que requieren adaptaciones individualizadas.
Síndrome hiperglucémico hiperosmolar (SHH)
El SHH se caracteriza por hiperglucemia severa (>600 mg/dl), hiperosmolaridad plasmática (>330-350 mOsm/kg) (que se calcula mediante la fórmula para calcular la osmolaridad plasmática efectiva, detallada a continuación) y deshidratación, en ausencia de cetoacidosis marcada. A diferencia de lo que se creía anteriormente, no todos los pacientes se presentan comatosos y pueden manifestar cierto grado de acidosis y cetosis.
Osmolaridad plasmática efectiva (mOsm/kg): 2 x Na+ (mmol/l) + (glucosa (mg/dl) / 18)
Debido al rápido equilibrio del BUN a través de las membranas, es recomendable la medición de la osmolaridad plasmática efectiva en lugar de la total. Signos neurológicos han sido observados en pacientes con valores superiores a 340 mOsm/kg.
En este síndrome, el paciente aún conserva algo de insulina funcional, lo que evita la activación de la LSH, disminuyendo la lipólisis y la producción de CC, y frenando así la acidemia. Sin embargo, la concentración de insulina es insuficiente para controlar la hiperglucemia severa, que se debe a un aumento en la gluconeogénesis, glucogenólisis y un uso inadecuado de glucosa por los tejidos periféricos.
La hiperglucemia e hipernatremia elevan considerablemente la osmolaridad plasmática, generando un gradiente osmótico que atrae agua fuera de las células cerebrales, provocando su deshidratación y causando alteraciones neurológicas. Inicialmente, la filtración glomerular está aumentada debido a la diuresis osmótica y glucosuria; con el tiempo, la reducción del volumen plasmático empeora la filtración glomerular y limita la excreción de glucosa, agravando la hiperglucemia plasmática.
Las enfermedades concomitantes más frecuentes que contribuyen al desarrollo del SHH incluyen patologías renales, cardíacas, respiratorias, infecciosas y neoplasias10.
Los pacientes pueden presentar anorexia o inapetencia, letargo, vómito, poliuria/polidipsia, cambios en el comportamiento, diarrea, deshidratación severa y alteraciones neurológicas como depresión, coma, convulsiones y ataxia. Generalmente, estos pacientes llegan en estado crítico y algunos presentan enfermedad renal aguda concurrente.
El objetivo principal del tratamiento es reemplazar los déficits hídricos, reducir lentamente los niveles de glucosa sérica, corregir los desbalances electrolíticos y tratar las enfermedades subyacentes.
Para el manejo hídrico, se recomienda iniciar con un bolo de cristaloide isotónico si existen déficits vasculares. Luego, debe continuarse con la reposición de la deshidratación, mantenimiento y las pérdidas continuas, evitando variaciones bruscas en la natremia. La corrección del sodio debe ser gradual (0.5-1 mEq/l/h), por lo que se requiere monitoreo frecuente de electrolitos y ajuste de la fluidoterapia según los resultados. Dado el riesgo de correcciones inadecuadas, los pacientes con alteraciones del sodio requieren un manejo clínico cuidadoso, por lo que se recomienda consultar literatura especializada.
Una corrección rápida de la deshidratación puede inducir edema cerebral y deterioro neurológico, cuyos signos pueden manifestarse varios días después. Por ello, la rehidratación debe realizarse de forma gradual durante 24-48 horas, al igual que la corrección de la hiperglucemia, con el fin de minimizar el riesgo de edema cerebral iatrogénico.
La administración de insulina no debe ser prioritaria en la fase inicial. Se recomienda retrasarla hasta que el volumen vascular esté restaurado, el paciente esté más hidratado y la glucemia no disminuya más de 50 mg/dl/h solo con fluidoterapia. En pacientes con cetonemia, dosis bajas de insulina sí son necesarias para metabolizar los cuerpos cetónicos. El protocolo de insulina es similar al de la cetoacidosis diabética (CAD), pero con dosis reducidas a la mitad para evitar cambios bruscos en la osmolaridad plasmática.
Se deben medir y suplementar potasio, fósforo y magnesio según sea necesario. Al igual que en la CAD (ver Tabla 1), es recomendable normalizar estos electrolitos antes de iniciar la insulinoterapia. Asimismo, se sugiere medir los CC al menos una vez al día para detectar el desarrollo de CAD. La osmolaridad plasmática debe calcularse periódicamente para monitorizar la resolución de la hiperosmolaridad.
Cuando el paciente se encuentre comiendo y bebiendo normalmente, se puede reiniciar el tratamiento con insulina de acción prolongada y monitorizar como un paciente diabético estándar.
Un estudio reportó una mortalidad intrahospitalaria del 64.7 % y una supervivencia a largo plazo (>2 meses) del 12 %. El pronóstico no se asoció con la presencia de signos neurológicos, glucemia, concentración de sodio medido o corregido, ni con la osmolaridad total o efectiva. Los pacientes sobrevivientes tenían enfermedades concurrentes curables10.
Cetoacidosis diabética euglucémica (CDE)
La CDE es una complicación exclusiva de felinos tratados con inhibidores del cotransportador sodio-glucosa tipo 2 (SGLT-2). Estos fármacos actúan inhibiendo la reabsorción de glucosa en el túbulo renal proximal, lo que facilita la excreción urinaria de glucosa y reduce la hiperglucemia severa habitual en la CAD. Además, los inhibidores SGLT-2 aumentan el glucagón plasmático y la producción endógena de glucosa, promoviendo lipólisis y cetoacidosis sin elevación marcada de glucosa en sangre.
La CDE se define por la presencia de CAD con glucemia menor a 200-250 mg/dl.
Actualmente, no existe un protocolo establecido para el tratamiento de la CDE en felinos, ya que se trata de una condición relativamente reciente en esta especie. Por lo tanto, el manejo se basa en extrapolaciones de la medicina humana, con énfasis en una suplementación agresiva con glucosa que permita la administración segura de insulina para facilitar el metabolismo de los cuerpos cetónicos.
- Algunos autores recomiendan usar el mismo protocolo que para la CAD, pero con inicio inmediato de suplementación con dextrosa.
- Otros sugieren administrar primero un bolo inicial intravenoso de dextrosa al 50 % diluido (0.25 ml/kg), antes de iniciar la infusión de insulina (0.1 U/kg/h), y posteriormente, se continúa con una infusión de dextrosa al 2.5-5 % para mantener niveles adecuados de glucosa.
Es importante recordar que en pacientes euglucémicos, por cada 0.1 U de insulina administrada debe acompañarse la administración de 0.2 gramos de dextrosa para evitar hipoglucemia.
También se debe considerar que el efecto glucosúrico de los inhibidores SGLT-2 puede persistir hasta 5 días después de la suspensión del medicamento, por lo que la monitorización y suplementación con dextrosa pueden ser necesarias durante varios días.
Se recomienda la medición y corrección continua de electrolitos (potasio, fósforo, magnesio) según sea necesario, y una monitorización frecuente de la glucemia, cuerpos cetónicos y estado ácido-base para adaptar el tratamiento.
Las complicaciones agudas en felinos diabéticos representan emergencias médicas complejas que requieren un enfoque terapéutico individualizado, basado en una adecuada resucitación hídrica, corrección de electrolitos, y administración controlada de insulina. La monitorización estrecha y el reconocimiento temprano de estas condiciones son esenciales para mejorar el pronóstico. Comprender la fisiopatología subyacente y adaptar los protocolos disponibles a las necesidades clínicas y recursos del paciente permite no solo estabilizar al felino críticamente enfermo, sino también ofrecer una oportunidad real de recuperación y, en algunos casos, remisión de la diabetes.
Bibliografía
- Miller CD, Phillips LS, Ziemer DC, Gallina DL, Cook CB, El-Kebbi IM. Hypoglycemia in patients with type 2 diabetes mellitus. Arch Intern Med. 2001 Jul 9;161(13):1653-9. doi: 10.1001/archinte.161.13.1653. PMID: 11434798.
- Viebrock KA, Dennis J. Hypoglycemic episodes in cats with diabetes mellitus: 30 cases (2013-2015). J Feline Med Surg. 2018 Jun;20(6):563-570. doi: 10.1177/1098612X17722853. Epub 2017 Aug 17. PMID: 28816090; PMCID: PMC11104079.
- Cohen EA, Porter L, Crews CD, Mott J, Tardo AM, Gilor C. Transmucosal glucagon rapidly increases blood glucose concentration in healthy cats. J Feline Med Surg. 2024 Nov;26(11):1098612X241280516. doi: 10.1177/1098612X241280516. PMID: 39614598; PMCID: PMC11607742.
- Whitley NT, Drobatz KJ, Panciera DL. Insulin overdose in dogs and cats: 28 cases (1986-1993). J Am Vet Med Assoc. 1997 Aug 1;211(3):326-30. PMID: 9262672.
- Rudloff E. Diabetic ketoacidosis in the cat: Recognition and essential treatment. J Feline Med Surg. 2017 Nov;19(11):1167-1174. doi: 10.1177/1098612X17735762. Erratum in: J Feline Med Surg. 2018 Aug;20(8):NP4. doi: 10.1177/1098612X18781683. Erratum in: J Feline Med Surg. 2019 Aug;21(8):NP4. doi: 10.1177/1098612X19853190. PMID: 29068248; PMCID: PMC10816619.
- DiFazio J, Fletcher DJ. Retrospective comparison of early- versus late-insulin therapy regarding effect on time to resolution of diabetic ketosis and ketoacidosis in dogs and cats: 60 cases (2003-2013). J Vet Emerg Crit Care (San Antonio). 2016 Jan-Feb;26(1):108-15. doi: 10.1111/vec.12415. Epub 2015 Nov 9. PMID: 26551019.
- Malerba E, Mazzarino M, Del Baldo F, Corradini S, Carotenuto G, Giunti M, Fracassi F. Use of lispro insulin for treatment of diabetic ketoacidosis in cats. J Feline Med Surg. 2019 Feb;21(2):115-123. doi: 10.1177/1098612X18761696. Epub 2018 Mar 7. PMID: 29513157; PMCID: PMC10814606.
- Gallagher BR, Mahony OM, Rozanski EA, Buob S, Freeman LM. A pilot study comparing a protocol using intermittent administration of glargine and regular insulin to a continuous rate infusion of regular insulin in cats with naturally occurring diabetic ketoacidosis. J Vet Emerg Crit Care (San Antonio). 2015 Mar-Apr;25(2):234-9. doi: 10.1111/vec.12269. Epub 2014 Dec 24. PMID: 25546713.
- Marshall RD, Rand JS, Gunew MN, Menrath VH. Intramuscular glargine with or without concurrent subcutaneous administration for treatment of feline diabetic ketoacidosis. J Vet Emerg Crit Care (San Antonio). 2013 May-Jun;23(3):286-90. doi: 10.1111/vec.12038. Epub 2013 Mar 26. PMID: 23530935.
- Koenig, A., Drobatz, K.J., Beale, A.B. and King, L.G. (2004), Hyperglycemic, hyperosmolar syndrome in feline diabetics: 17 cases (1995–2001). Journal of Veterinary Emergency and Critical Care, 14: 30-40.
- HaddMJ,BienhoffSE, LittleSE, et al.Safety and effectiveness of the sodium-glucose cotransporter inhibitor bexagliflozin in cats newly diagnosed with diabetes mellitus.J Vet Intern Med.2023;37(3):915-924. doi:10.1111/jvim.16730
- Bonner C, Kerr-Conte J, Gmyr V, Queniat G, Moerman E, Thévenet J, Beaucamps C, Delalleau N, Popescu I, Malaisse WJ, Sener A, Deprez B, Abderrahmani A, Staels B, Pattou F. Inhibition of the glucose transporter SGLT2 with dapagliflozin in pancreatic alpha cells triggers glucagon secretion. Nat Med. 2015 May;21(5):512-7. doi: 10.1038/nm.3828. Epub 2015 Apr 20. PMID: 25894829.
- Marques PL, Mendoza B, Dias MJ, Carvalho M, Niessen SM, Leal RO. Clinical Management of Euglycemic Ketoacidosis in a Cat With Congenital Diabetes Mellitus Treated With Insulin and Dapagliflozin. J Vet Emerg Crit Care (San Antonio). 2025 Mar-Apr;35(2):162-170. doi: 10.1111/vec.13458. Epub 2025 Apr 20. PMID: 40254974.
 by Multimédica
by Multimédica