Abordaje diagnóstico y terapéutico de la cetoacidosis diabética en urgencias de pequeños animales
Resumen breve
La cetoacidosis diabética es una patología secundaria a la diabetes mellitus, constituyendo una de sus complicaciones más graves. Consiste en una hiperglucemia persistente debido a la falta de insulina o a una insulinorresistencia, produciéndose cuerpos cetónicos de forma secundaria para asegurar un aporte energético a las células, lo que provoca una acidosis metabólica secundaria a su acumulación.Los signos clínicos más habituales son aquellos asociados a la diabetes mellitus,…
Índice de contenidos
Resumen
La cetoacidosis diabética es una patología secundaria a la diabetes mellitus, constituyendo una de sus complicaciones más graves. Consiste en una hiperglucemia persistente debido a la falta de insulina o a una insulinorresistencia, produciéndose cuerpos cetónicos de forma secundaria para asegurar un aporte energético a las células, lo que provoca una acidosis metabólica secundaria a su acumulación.
Los signos clínicos más habituales son aquellos asociados a la diabetes mellitus, así como signos secundarios a la acidosis, como vómitos, decaimiento o anorexia. En la exploración física general el hallazgo más relevante será la deshidratación, además de signos de hipovolemia (taquicardia, hipotensión, alteración del estado mental, etc.) en los casos más graves.
Para su diagnóstico es esencial la determinación de hiperglucemia, cetonemia, glucosuria y cetonuria; y para su clasificación y posterior tratamiento es necesario realizar una analítica de sangre completa que incluya una gasometría, para la valoración de posibles alteraciones electrolíticas, del equilibrio ácido-base y otros parámetros renales y hepáticos. Será imprescindible realizar controles analíticos seriados que permitan ajustar el tratamiento en función de las necesidades electrolíticas, que pueden ir variando a medida que se comienza el tratamiento específico con insulinoterapia.
Introducción
La cetoacidosis diabética (CAD) es una complicación de la diabetes mellitus relativamente habitual en perros y gatos. La diabetes mellitus es un síndrome caracterizado por una hiperglucemia secundaria a una falta relativa o absoluta de insulina. La falta absoluta de insulina se debe a una pérdida o alteración de la producción de la misma por parte de las células beta pancreáticas, mientras que una falta relativa se refiere a una pérdida de sensibilidad (resistencia) a la misma por parte de los tejidos. Esta resistencia se debe a diferentes factores: obesidad, ciertas enfermedades (hiperadrenocorticismo, hipotiroidismo, hipertiroidismo, enfermedad renal, enfermedad periodontal, pancreatitis, infecciones sistémicas, etc.) o medicaciones3,6.
La diabetes mellitus es una patología relativamente frecuente en perros y gatos, ya que afecta en torno a un 0.5-1 % de la población3, y puede desencadenar una cetoacidosis diabética en animales con la enfermedad no diagnosticada o mal controlada, o cuando hay enfermedades concurrentes como las anteriormente mencionadas. La cetoacidosis es un cuadro grave asociado a una alta mortalidad, aunque esta se relaciona más habitualmente a las enfermedades concurrentes que presenta el paciente más que a la propia cetoacidosis1,6,7,11.
En un cuadro de diabetes mellitus controlado, ya sea debido a un déficit relativo o absoluto de insulina, se pueden producir ciertas situaciones que aumenten la resistencia a la insulina y que predispongan al desarrollo de una cetoacidosis diabética. Estas situaciones, ya descritas, estimulan la liberación de hormonas reguladoras (glucagón, cortisol, epinefrina, hormona de crecimiento), de citoquinas proinflamatorias (TNFalfa, IL-6), de ácidos grasos libres y aminoácidos, y/o el desarrollo de acidosis metabólica6. Este escenario favorece el desarrollo de resistencia a la insulina en los tejidos, lo que provoca una disminución en la capacidad de las células para captar y utilizar la glucosa. De esta forma, las células requerirán de un aporte de energía alternativo para mantener su metabolismo, y la concentración de glucosa en sangre será cada vez mayor al no poder ser utilizada. Este aporte alternativo de energía se realiza a través del metabolismo de los ácidos grasos, y en este proceso se producen cuerpos cetónicos y ácidos carboxílicos como residuo. Los cuerpos cetónicos, así como la glucosa en exceso del espacio intravascular, son inicialmente excretados por la orina, dando lugar a glucosuria y cetonuria, pero llegado un punto el riñón excede su capacidad de filtración, con lo que estos componentes pasan a acumularse en el plasma. Tanto los cuerpos cetónicos como los ácidos carboxílicos derivados del proceso de oxidación de grasas provocan una disminución del pH sanguíneo al producir la liberación de hidrogeniones, y esto deriva en una acidosis metabólica, más severa cuanto mayor sea la producción de cetonas.2,6,10,12
La sintomatología con la que se presentan los pacientes varía considerablemente dependiendo del grado de gravedad del cuadro, pero los signos más habituales son aquellos secundarios a la diabetes mellitus per se (poliuria, polidipsia, polifagia, pérdida de peso)3, aquellos secundarios a la acidosis tras el desarrollo de la cetosis (vómitos, diarreas, decaimiento, hiporexia/anorexia, etc.), y pueden llegar a observarse otros signos secundarios a patologías concurrentes (polaquiuria, dolor abdominal, fiebre, etc.)1,6,12.
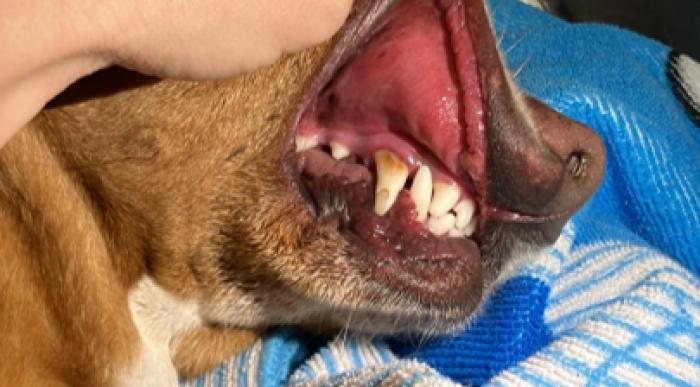
La exploración física del paciente en el ingreso es esencial, y podrá aportar información muy distinta en función de la gravedad del cuadro y el tiempo de evolución. La característica más relevante es la deshidratación con la que se presentan (Figura 1), secundaria a la diuresis osmótica y a la hiperosmolaridad sérica, que puede ir desde un 5 % hasta 10-15 %, apareciendo entonces signos de hipovolemia (taquicardia, hipotensión, estado mental alterado, etc.)12.
El diagnóstico de una cetoacidosis diabética se basa en la presencia de los signos clínicos característicos de la diabetes mellitus (poliuria, polidipsia, polifagia, pérdida de peso, etc.)3 así como un empeoramiento de los mismos y la posible aparición de vómitos, anorexia y decaimiento; junto con un valor de glucemia aumentado (200-1000mg/dL6, siendo el rango de referencia en perros de 55- 110 mg/dL y en gatos de 56-124 mg/dL), la detección de glucosuria, y la presencia de cuerpos cetónicos en sangre (con un valor de >3.5 mmol/L en perros y > 2.4 mmol/L en gatos), y en orina10.
El tratamiento específico de la cetoacidosis depende de la gravedad del cuadro, que nos lo aporta el estado del paciente y la gravedad de la acidosis. En pacientes aparentemente sanos y con una acidosis “leve” (valor de bicarbonato >16mEq/L)6, el tratamiento se puede plantear conservador y ambulatorio, pero en pacientes con sintomatología evidente y/o una acidosis grave (valor de bicarbonato < 12mEq/L)6, el tratamiento será hospitalario, ya que requiere de la resolución de la acidosis, que conlleva asimismo la resolución de la hiperglucemia y cetosis.
Pruebas laboratoriales para el diagnóstico
Glucemia
El valor de glucosa en sangre de pacientes con CAD oscila entre 200 y 1000 mg/dl, siendo más alta en gatos que en perros. El valor promedio oscila alrededor de los 500 mg/dl6. Este valor determinará la intensidad terapéutica inicial con fluidoterapia e insulinoterapia. Cuanto más alto es el valor de glucosa en sangre, existe mayor riesgo de desarrollar un edema cerebral por un descenso brusco en la osmolaridad del plasma12. Es por esto por lo que se deberá ser especialmente cauto a la hora de bajar la glucemia durante la primera etapa del tratamiento, intentando realizarlo de la forma más progresiva posible, teniendo como objetivo ideal un descenso de 50mg/dl de glucosa por hora6.
Electrolitos
Sodio
La concentración suele estar disminuida (hiponatremia)en la mayoría de los casos (aproximadamente un 60 % en perros y un 80 % en gatos)1,6,11 debido a 3 mecanismos de acción principalmente:
- Los cuerpos cetónicos arrastran sodio al ser excretados por la orina.
- La hiperglucemia provoca un aumento de la diuresis osmótica al liberarse glucosa a través de los túbulos renales, lo que provoca una mayor pérdida de sodio a través de la orina.
- Lahiperglucemia causa además un aumento de osmolaridad plasmática importante, que provoca el arrastre de agua del espacio intracelular al intravascular, disminuyendo la concentración de sodio por dilución del mismo.
Potasio
Sus valores dependen fundamentalmente de la duración del proceso, de la funcionalidad renal y del estado general del paciente. Pueden estar aumentados (en casos graves de pacientes con anuria/oliguria), normales o disminuidos, aunque lo más habitual es encontrar valores disminuidos (hipopotasemia)1,6,10,12. Los mecanismos de acción que producen esta alteración son los siguientes:
- Pérdida a nivel renal, debido al aumento del potasio en sangre por la falta de insulina que permita su entrada dentro de la célula y la diuresis osmótica inducida por la glucosuria y cetonuria)
- Por liberación de epinefrina (uno de los causantes de la resistencia a la insulina en casos de enfermedades concurrentes) y la presencia de acidosis, que promueven la entrada del potasio dentro de las células.
- Por la administración de insulina una vez empezada la terapia (permite la entrada del potasio dentro de las células).
Fósforo
Normalmente se evidencia hipofosfatemia ligera (mayoritariamente en gatos) o normofosfatemia1,6,10,12. Se puede llegar a observar hiperfosfatemia en casos de enfermedad renal presente en el paciente.
Magnesio
En casos de CAD los pacientes se suelen presentar con hipomagnesemia (<1.5mg/dL)1,6. Esto se debe a una pérdida renal importante causada por la diuresis osmótica, y debido a una translocación del magnesio intravascular al espacio intracelular, siguiendo mecanismos similares a los descritos para el potasio. Sin embargo, no se observará sintomatología asociada a esta alteración electrolítica hasta valores graves con un magnesio total sérico menor de 1 mg/dl6.
Calcio
En la mayoría de los casos observaremos normocalcemia6, salvo en animales con enfermedades concomitantes como pancreatitis o alteraciones como hipomagnesemia e hipoproteinemia, en los que podremos observar hipocalcemia.
Gasometría
Debido a la sobreproducción de cuerpos cetónicos, el aumento de iones H+ en sangre y la disminución de bicarbonato, el paciente presentará unaacidosis metabólica en la que podremos observar pH < 7.3, y valores de bicarbonato <16meq/l4,6,7,11,12 (Figura 2). Esta situación se agrava por la incapacidad renal de excreción de niveles tan altos de ácidos, al saturarse su límite de acidificación de la orina.

Hemograma
Generalmente se observa leucocitosis neutrofílica marcada en estos pacientes, secundaria bien al cuadro de “estrés” al que están sometidos, bien a una enfermedad inflamatoria/infecciosa concurrente (pancreatitis, infección urinaria, etc.) o ambas4,6. También se podrá evidenciar hemoconcentración en la mayoría de los casos, secundaria a la deshidratación. En gatos es frecuente la presencia de cuerpos de Heinz6.
Bioquímica
Lo más habitual es observar alteraciones a nivel de los parámetros hepáticos (aumento de transaminasas, hiperbilirrubinemia, etc.) como consecuencia de la hipoperfusión secundaria a la hipovolemia, de forma secundaria por enfermedades concurrentes (ej. pancreatitis) o primaria por alteraciones hepáticas (ej. lipidosis hepática, colangiohepatitis, etc), que pueden ser causa o consecuencia de la CAD3,6. A su vez, se podrá observar hipercolesterolemia e hiperlipidemia secundarias al aumento del metabolismo de las grasas a nivel hepático3. En pacientes con cetoacidosis que presentan enfermedades concomitantes (p. ej., renales o digestivas), ya sean primarias o secundarias al proceso metabólico subyacente, puede observarse una disminución de las proteínas totales atribuible a hipoalbuminemia. Por el contrario, en ausencia de alteraciones orgánicas concomitantes, la hiperproteinemia observada suele ser relativa y secundaria a hemoconcentración asociada a la deshidratación6.
En el caso de la CAD los pacientes pueden presentar azotemia (aumento de los valores de BUN y creatinina), con mayor incidencia en gatos6,8,11. Para diferenciar un origen primario de secundario (o prerrenal) de esta azotemia, se deberán contrastar estos valores con la densidad urinaria, de tal forma que se observará una densidad urinaria normal o aumentada en casos de azotemia prerrenal, secundaria a la deshidratación e hipovolemia.
Urianálisis y urocultivo
Como se ha comentado anteriormente, enfermedades concomitantes como infecciones del tracto urinario inferior (ITU) o enfermedad renal aguda/crónica pueden producir una resistencia a la insulina al liberar hormonas de estrés que provoquen o agraven la CAD del paciente10. Por ello, y de cara a investigar la causa de la azotemia en caso de presentarse, o con el objetivo de descartar una ITU como origen del cuadro, debemos realizar un urianálisis, en el que podremos observar las siguientes alteraciones:
- Densidad urinaria (DU): Informan sobre todo del origen renal o prerrenal de la azotemia en caso de presentarse. Densidades urinarias menores a 1020-1025 hacen sospechar de una enfermedad renal primaria asociada6.
- Sedimento urinario: Aunque no se observe bacteriuria es conveniente realizar un cultivo, ya que la poliuria y la glucosuria presentes en cuadros de diabetes mellitus favorecen la proliferación bacteriana3,6,12.
- Glucosuria y cetonuria: En animales con cetoacidosis puede encontrarse glucosuria de moderada a severa, así como la presencia de cuerpos cetónicos en orina6,12. La detección de estos últimos puede resultar complicada, ya que las tiras de orina sólo son sensibles a acetona y no β-hidroxibutirato (presente en los estadíos iniciales de la CAD), pudiendo pasar desapercibido un cuadro inicial de cetoacidosis. Algunos estudios sugieren el uso de una muestra de plasma o suero en tiras de orina para establecer la presencia de estos ácidos de forma más precisa que en la orina5. Valores de β hidroxibutirato >3.5 mmol/L en perros y >2.4 mmol/L en gatos están asociados a CAD7.Actualmente existen glucómetros que también miden cetonemia en sangre validados para el uso en pequeños animales, que facilitan su detección.
- Otros: También se podrá observar en estos casos proteinuria, hemoglobinuria y UPC elevado6, aunque este último valor no será demasiado relevante ya que se puede ver aumentado en casos de ITU, con lo que será imprescindible descartar una infección mediante un urocultivo antes de valorarlo.
La gravedad de estas alteraciones laboratoriales depende del grado de hiperglucemia en sangre, el tiempo de progresión de la enfermedad, la causa del desarrollo de la cetoacidosis y la presencia de enfermedades concomitantes, entre otras causas.
Cuando el paciente se encuentre estable, es importante plantear una serie de pruebas diagnósticas de cara a identificar la causa de la descompensación de la diabetes mellitus: radiografías torácicas, ecografía abdominal, lipasa pancreática específica, pruebas de funcionalidad endocrina, etc3,6,12.
Tratamiento y monitorización terapéutica
Fluidoterapia
El primer paso para la estabilización del paciente cetoacidótico, y el más importante, es la administración de fluidoterapia6,10,12. Esta es imprescindible para corregir la hipovolemia en los casos en los que sea necesario, así como para corregir la deshidratación, las alteraciones electrolíticas, y mejorar la perfusión renal para una mayor excreción de glucosa, iones H+ y cuerpos cetónicos, y en consecuencia, facilitar la resolución de la acidosis metabólica10. La velocidad de la fluidoterapia instaurada dependerá del grado de deshidratación, del estado del paciente y de las pérdidas que haya podido tener, siendo recomendable el sondaje urinario durante las primeras 24-48 horas para asegurar un mejor control de la producción urinaria y de la reposición de pérdidas6.
En la mayoría de los casos se recomienda el uso de un cristaloide isotónico (ej. Ringer Lactato) debido a la alta deshidratación que presentan los pacientes, ya que asegura una rehidratación tanto del espacio intersticial como del intracelular de forma rápida (20-30 minutos tras su administración)6,12. Estudios más antiguos recomiendan el uso de otro cristaloide isotónico, el NaCl 0.9 %, debido a su alta concentración de sodio de cara a la resolución de la hiponatremia10. Sin embargo, y pese a corregir esta alteración electrolítica de forma más eficiente, la administración de este fluido en altas cantidades para responder al alto requerimiento de estos pacientes debido a la deshidratación y pérdidas abundantes, puede dar lugar a acidosis hiperclorémica como consecuencia de la gran cantidad de cloro administrada junto con el sodio8,9. Es por esto por lo que el uso de un cristaloide isotónico que contenga un sistema tampón (ej. Ringer Lactato, Plasmalyte 148, Isofundin, etc.) es más recomendable en estos casos10.
Para iniciar con la fluidoterapia se debe estimar el grado de deshidratación que presenta el paciente, con el objetivo de reponer la mitad del déficit de hidratación en las primeras 4-6 horas10. Siempre se deberá tener en cuenta el estado del paciente, pudiendo necesitar velocidades de reposición más altas (en pacientes hipovolémicos) o más bajas (en pacientes con enfermedades concomitantes como, por ejemplo, cardiopatías)6. Por el momento, y hasta que el paciente no esté más hidratado, no se iniciará la terapia con insulina, ya que la sola administración del cristaloide provocará un movimiento de electrolitos y agua, favoreciendo la entrada de agua en las células y disminuyendo la dilución del sodio a nivel intravascular, diluyendo así mismo la hiperglucemia inicial6,10,12.
Una vez pasadas esas 4-6 horas de reposición de fluidos, se reevaluará de nuevo al paciente y se volverán a medir tanto constantes vitales como parámetros laboratoriales, de cara a establecer una correcta insulinoterapia y reposición de electrolitos. El resto de volumen de fluidos necesarios para subsanar la deshidratación se administrarán en las próximas 12-24 horas, reevaluando al paciente de forma continua y reajustando según sea necesario6.
Se recomienda monitorizar el grado de deshidratación del paciente con un examen físico completo, teniendo en cuenta el peso del animal, las pérdidas urinarias (se espera una poliuria marcada debido a la diuresis osmótica: diuresis mayor de 1-2 ml/kg/hr, que será necesario reponer con la fluidoterapia) y las pérdidas digestivas10.
Corrección de alteraciones electrolíticas
Es importante monitorizar periódicamente (cada 6-12 h) los valores de electrolitos para ajustar su suplementación en los fluidos y minimizar la sintomatología clínica asociada6,10,12. Se deberá realizar un control electrolítico al ingreso del paciente, y otro de nuevo pasadas las primeras 4-6 horas de rehidratación intensiva del mismo, con el objetivo de comenzar a ajustar la suplementación electrolítica tras este último.
- Sodio: Para evaluar la hiponatremia real que presenta el paciente es necesario corregir el valor de Na+ obtenido en función de la hiperglucemia que presente6,10,11. Hay que tener en cuenta que la hiponatremia será más grave cuanto mayor sea la hiperglucemia, de tal forma que por cada 100 mg/dl de incremento en la glucosa sérica se produce un descenso del Na+ de 1.6 meq/l. Mediante la siguiente fórmula se obtiene la concentración de Na+ corrigiendo el error que induce la presencia de hiperglucemia:
Na+ corregido (mEq/L) = 1.6 x (concentración de glucosa [mg/dL] – 100)/100 + Na+ medido [mEq/L]
Un aumento agresivo del sodio puede producir sintomatología neurológica grave (secundaria a un edema cerebral), por lo que deberá hacerse de forma progresiva y monitorizar esta corrección de forma estrecha, intentando realizar un aumento de 1mEq/L por hora aproximadamente.6,10,11
- Potasio. La suplementación de potasio en estos pacientes debe ser monitorizada con frecuencia y suplementada de forma correcta, ya que, al comenzar con fluidoterapia, insulinoterapia y corregir la acidosis se podrá agravar la hipopotasemia inicial6,10,12. En animales oligúricos, anúricos o muy deshidratados, los niveles de potasio pueden estar aumentados o normales, y en estos casos primero se debe corregir el estado general del paciente y restablecer la función renal antes de suplementar el potasio. De cualquiera de las formas, una vez comenzada la terapia con insulina, la suplementación con potasio será imprescindible incluso en casos de que se encuentre en niveles adecuados en sangre, ya que la entrada de glucosa en las células estimulada por la insulina también promoverá la entrada de potasio en las mismas, produciendo hipopotasemia o agravando la preexistente6,10. La monitorización electrocardiográfica de estos animales es importante, ya que podremos observar alteraciones en el electrocardiograma (ECG) en pacientes con hipo o hiperkalemia6. Se recomienda suplementar el potasio siguiendo las indicaciones de la Tabla 1.
Tabla 1. Suplementación de potasio a la fluidoterapia intravenosa en perros y gatos (modificada de Silverstein & Hopper (2023)).
| Potasio sérico medido (mEq/L) | mEq de KCL añadidos a 250ml de solución cristaloide | mEq de KCl añadidos a 1L de solución cristaloide | Velocidad máxima de administración (ml/kg/hora) |
|---|---|---|---|
| <2.0 | 20 | 80 | 6 |
| 2.1-2.5 | 15 | 60 | 8 |
| 2.6-3.0 | 10 | 40 | 12 |
| 3.1-3.5 | 7 | 28 | 18 |
| 3.6-5.0 | 5 | 20 | 25 |
- Fósforo. Al igual que sucede con el caso del potasio, al iniciar la insulinoterapia se puede agravar la hipofosfatemia inicial o producirse si no estaba presente, debido al movimiento del fósforo hacia el espacio intracelular que promueve la insulina6,10. Los síntomas más típicos de este déficit son debilidad, ataxia, estado mental alterado y alteraciones miocárdicas y respiratorias. Se pueden observar estos síntomas cuando los niveles de fósforo son menores de 1.5 mg/dl, y es el valor a partir del cual se recomienda inicial suplementación del mismo2,6. Se recomienda suplementar el fósforo mediante el uso de fosfato potásico (monopotásico o dipotásico) o fosfato monosódico, en función de si existe hipopotasemia o hiponatremia, respectivamente. Se recomienda administrar de forma diluida en infusión continua a razón de 0.01-0.03mmol/kg/h durante 6 horas, y realizar mediciones seriadas de fósforo para plantear finalizar la suplementación cuando se alcancen valores de P>2.5mg/dL en perro y >3.1mg/dL en gato2. Se recomienda asimismo la medición de iCa para evitar posibles hipocalcemias secundarias, y la administración de la suplementación en cristaloides libres de calcio, para evitar precipitaciones2.
- Bicarbonato sódico. Sólo se planteará su administración en casos de acidemia grave, con un pH inferior a 7.0 tras la administración de al menos una hora de fluidoterapia4,6,8,10,12. Debido a los efectos secundarios asociados a la administración del mismo (acidosis respiratoria, hipocalcemia, hipernatremia, etc), y al hecho de que habitualmente se suele corregir la acidosis de forma progresiva tratando de forma directa la cetosis, el tratamiento con bicarbonato no suele ser necesario en estos casos6,8.
Insulinoterapia
La terapia con insulina debe iniciarse tras la rehidratación del paciente, lo antes posible, ya que es conveniente disminuir la concentración de glucosa y detener la producción de cuerpos cetónicos cuanto antes6,7,12. En las primeras fases de tratamiento se recomiendan insulinas de acción rápida y potencia elevada. La administración deberá ser de forma intravenosa (IV) o intramuscular (IM) preferiblemente, ya que en pacientes deshidratados la absorción vía subcutánea (SC) es más lenta6,10.
La frecuencia de administración varía dependiendo del protocolo, desde la infusión continua hasta su administración cada 1-4 horas6. El objetivo es mantener una glucosa sérica alrededor de 100 - 250 mg/dl3,6,10, pero intentando hacer un descenso progresivo para evitar efectos secundarios (la velocidad de descenso debe encontrarse entre 50-75 mg/dl/hr aprox.)6,7. La frecuencia de monitorización de la glucemia dependerá de la frecuencia de administración, siendo mayor cuando la administración es continua, pero de forma general se recomienda realizar cada 2 horas2,3.
Por otro lado, es imprescindible la suplementación con dextrosa una vez se haya conseguido reducir los valores de glucosa a menos de 250 mg/dl, de tal forma que se pueda continuar la administración de insulina sin producir una hipoglucemia refractaria2,6,10,12. La administración constante de insulina estimulará la entrada de cuerpos cetónicos dentro de las células junto con la glucosa, con lo que de esta forma tanto la cetosis como la acidosis se resolverán con mayor facilidad cuanta más insulina se administre al paciente10.
En los protocolos de infusión intravenosa continua de insulina de acción rápida se han descrito distintos métodos de preparación y esquemas de administración. La dosis recomendada es de 2.2 UI/kg/día en perros y de 1.1 UI/kg/día en gatos. Esta dosis menor en gatos se ha propuesto para reducir el riesgo de efectos neurológicos asociados a una corrección rápida de la hiperglucemia. Una de las posibles preparaciones consiste en añadir 2.2 UI/kg de insulina a 250 ml de NaCl al 0.9 %¹˒⁶˒¹⁰˒¹² y administrarla según la Tabla 2. En gatos, puede añadirse 1.1 UI/kg y utilizar la misma tabla o, alternativamente, emplear la descrita anteriormente, con la velocidad de infusión reducida a la mitad. Cabe señalar que la velocidad de infusión dependerá del volumen de diluyente utilizado.
Tabla 2. Ejemplo de administración de glucosa e insulina de acción rápida en infusión continua de forma intravenosa en función de la glucemia en gatos y perros en CAD (modificada de Silverstein & Hopper (2023)).
| Glucemia sérica (mg/dl) | Suplementación de glucosa a la fluidoterapia intravenosa | Velocidad de administración de insulina (ml/h) |
|---|---|---|
| >250 | Sin suplementación | 10 |
| 200-250 | 2.5 % dextrosa | 7 |
| 150-200 | 2.5 % dextrosa | 5 |
| 100-150 | 5 % dextrosa | 5 |
| <100 | 5 % dextrosa | Sin insulina |
Tratamiento de las patologías concomitantes
Es importante que, una vez estabilizado el paciente, se realicen pruebas diagnósticas más avanzadas de cara a identificar la causa de la descompensación de la diabetes mellitus que haya originado el cuadro de cetoacidosis, o aquellas enfermedades concomitantes que puedan dificultar la recuperación del paciente. Una vez identificadas es importante añadir tratamiento específico para cada una de ellas: antibiótico en caso de ITU, analgesia y protectores gástricos en caso de pancreatitis, etc1,3,6.
Monitorización (Tabla 3)
Tabla 3. Monitorización de pacientes con CAD en hospitalización.
| Parámetros | Frecuencia* |
|---|---|
| Estado general del animal (mucosas, estado mental, grado de deshidratación, ACP, PANI, peso…) | Continua las primeras 24-48 h, después cada 4 - 6 h dependiendo de la evolución del paciente ** |
| Fluidoterapia y electrolitos (potasio, sodio, cloro, fósforo) | Cada 6 - 12 h |
| Control diuresis (control + reposición de pérdidas) | Cada 4-6 h (valorar sondaje) |
| ECG | Constante |
| Glucemia | Al inicio cada 1-2 h, después cada 2 - 4 h dependiendo de la evolución del paciente |
| Valores renales y hepáticos | Cada 24 - 48 h |
| Gasometría | Cada 12 - 24 h |
*Todas las frecuencias son aproximadas y dependen de la evolución, del estado del paciente y de la respuesta al tratamiento.
**Se recomienda realizar una monitorización más continua y exhaustiva en las primeras horas de tratamiento.
La monitorización de la glucosa sanguínea suele realizarse mediante glucómetros portátiles de uso clínico validados para perros y gatos (Figura 3).

Los sistemas de monitorización continua de glucosa (CGM) permiten registrar la concentración de glucosa en el espacio intersticial y estimar la glucemia a intervalos cortos (Vídeo1).
Vídeo 1. Medición de glucosa sanguínea mediante dispositivo de medición contínua.
Diversos estudios han demostrado una buena correlación entre las concentraciones de glucosa intersticial y las determinaciones repetidas de glucosa en sangre, incluso en perros y gatos con cetoacidosis diabética. Estos sistemas presentan algunas limitaciones. Dado que la medición se realiza en el espacio intersticial, puede existir un cierto retraso respecto a los cambios rápidos en la glucemia. La precisión también puede disminuir en el rango hipoglucémico y en pacientes con deshidratación significativa. Por ello, cuando los valores registrados por el sensor no concuerden con la situación clínica del paciente, se recomienda confirmar la glucemia mediante una determinación directa en sangre.
Síndrome hiperglucémico hiperosmolar: diagnóstico diferencial con la cetoacidosis diabética
El síndrome hiperglucémico hiperosmolar (SHH) es una complicación poco frecuente pero grave de la diabetes mellitus descrita en perros y gatos. Se caracteriza por hiperglucemia extrema, hiperosmolaridad sérica marcada y ausencia o mínima cetosis. En medicina veterinaria se han propuesto como criterios diagnósticos concentraciones de glucosa sérica superiores a 600 mg/dl, osmolalidad sérica elevada (generalmente >325 mOsm/kg en perros y >350 mOsm/kg en gatos) y ausencia de cetonuria significativa.
La fisiopatología comparte algunos mecanismos con la CAD, como la deficiencia relativa o absoluta de insulina y el aumento de hormonas contrarreguladoras (glucagón, cortisol, epinefrina y hormona del crecimiento), que favorecen la gluconeogénesis y la glucogenólisis. Sin embargo, a diferencia de la CAD, en el SHH suele persistir una pequeña cantidad de insulina circulante suficiente para inhibir la lipólisis y la cetogénesis, lo que explica la ausencia o escasa producción de cuerpos cetónicos.
La hiperglucemia intensa induce diuresis osmótica con pérdidas importantes de agua libre, lo que conduce a deshidratación marcada, hipovolemia y aumento progresivo de la osmolalidad plasmática. La reducción secundaria de la tasa de filtración glomerular favorece la acumulación adicional de glucosa en sangre y perpetúa el estado hiperosmolar. Clínicamente, el SHH suele asociarse a deshidratación más grave y mayor alteración neurológica que la CAD, mientras que la acidosis metabólica suele ser leve o inexistente. Las principales diferencias entre ambas crisis diabéticas se resumen en la Tabla 4.
Tabla 4. Diferencia entre CAD y SHH.
| Parámetro | CAD | SHH |
|---|---|---|
| Glucosa sérica | Elevada | Muy elevada (puede superar 1000 mg/dl) |
| Cetonemia / cetonuria | Marcada | Ausente o mínima |
| pH sanguíneo | Acidosis metabólica | Normal o ligeramente acidótico |
| Bicarbonato | Disminuido | Normal o ligeramente disminuido |
| Osmolalidad sérica efectiva | Normal o moderadamente aumentada | Marcadamente aumentada (>325–350 mOsm/kg) |
| Mecanismo fisiopatológico predominante | Deficiencia grave de insulina con lipólisis y cetogénesis | Deficiencia relativa de insulina suficiente para inhibir la lipólisis |
| Deshidratación | Moderada a grave | Grave a extrema |
| Signos neurológicos | Poco frecuentes | Frecuentes por hiperosmolaridad |
Conclusión
Como conclusión, tanto para el diagnóstico como para la monitorización terapéutica de la CAD es esencial la realización de pruebas diagnósticas básicas: analítica de sangre completa y gasometrías.
Para una monitorización estrecha de las alteraciones electrolíticas, que serán una de las principales complicaciones asociadas tanto a la patología en sí como al tratamiento instaurado, es importante realizar controles electrolíticos seriados. De esta forma se podrá ajustar la suplementación de cada uno de ellos de forma precisa, evitando así los signos clínicos derivados de las alteraciones electrolíticas graves, algunos de los cuales pueden llegar a ser mortales.
De igual forma tendrá una gran importancia la posterior investigación tras la estabilización del paciente, de cara a identificar la causa de la descompensación de la diabetes, o enfermedades concurrentes que puedan agravar el cuadro de cetoacidosis. Para ello serán necesarias más pruebas diagnósticas, algo más avanzadas, como urocultivo, ecografía abdominal, radiografías torácicas o pruebas endocrinas.
Finalmente, de forma resumida se puede afirmar que la CAD es una enfermedad metabólica grave, que no requiere grandes pruebas complementarias para su diagnóstico, pero sí para su monitorización y tratamiento, que será intrahospitalario en la mayoría de los casos.
Bibliografía
- Anderson, J. D., Rondeau, D. A., & Hess, R. S. (2019). Lispro insulin and electrolyte supplementation for treatment of diabetic ketoacidosis in cats. J. Vet. Intern. Med., 33(4), 1593–1601. https://doi.org/10.1111/jvim.15518
- Fragío Arnold, C. (2025). Manual de urgencias en pequeños animales, 2ª edición. Multimédica Ediciones Veterinarias. ISBN:978-84-18636-31-8
- Behrend, E., Holford, A., Lathan, P. et al. (2018). AAHA Diabetes Management Guidelines for Dogs and Cats. J.Am. Anim. Hosp. Assoc., 54(1), 1–21. https://doi.org/10.5326/jaaha-ms-6822
- Chiasson, J., Aris-Jilwan, N., Bélanger, R., et al. (2003). Diagnosis and treatment of diabetic ketoacidosis and the hyperglycemic hyperosmolar state. CMAJ.168(7):859-66. PMID: 12668546
- Chong, S. K., & Reineke, E. L. (2016). Point-of-Care glucose and ketone monitoring. Top. Companion Anim. Med., 31(1), 18–26. https://doi.org/10.1053/j.tcam.2016.05.005
- Feldman, E. C., Nelson, R. W., Reusch, C., & Scott-Moncrieff, J. C. (2014). Canine and feline endocrinology. Ed. Saunders.
- Gant, P., Barfield, D., & Florey, J. (2023). Comparison of insulin infusion protocols for management of canine and feline diabetic ketoacidosis. J. Vet. Emerg. Crit. Care, 34(1), 23–30. https://doi.org/10.1111/vec.13354
- Goad, N. T., Bakhru, R. N., Pirkle, J. L., & Kenes, M. T. (2019). Association of hyperchloremia with unfavorable clinical outcomes in adults with diabetic ketoacidosis. J. Intensive Care Med, 35(11), 1307–1313. https://doi.org/10.1177/0885066619865469
- Mahler, S. A., Conrad, S. A., Wang, H., & Arnold, T. C. (2010). Resuscitation with balanced electrolyte solution prevents hyperchloremic metabolic acidosis in patients with diabetic ketoacidosis. Am. J. Emerg. Med., 29(6), 670–674. https://doi.org/10.1016/j.ajem.2010.02.004
- Thomovsky, E. (2016). Fluid and electrolyte therapy in diabetic ketoacidosis. Vet. Clin. North Am. Small Anim. Pract., 47(2), 491–503. https://doi.org/10.1016/j.cvsm.2016.09.012
- Schermerhorn, T., & Barr, S. C. (2006). Relationships between glucose, sodium and effective osmolality in diabetic dogs and cats. J. Vet. Emerg. Crit. Care, 16(1), 19–24. https://doi.org/10.1111/j.1476-4431.2005.00161.x
- Silverstein, D., & Hopper, K. (2023). Small animal critical care medicine, 3rd edition. Ed. Elsevier. DOI:10.1016/C2017-0-04165-4
 by Multimédica
by Multimédica