Aproximación al paciente en shock
Resumen breve
El shock es un síndrome potencialmente mortal y multifactorial, a lo que habrá que enfrentarse, con toda probabilidad y en más de una ocasión, a lo largo de la carrera profesional como ATV. Al encontrarse frente a un paciente en shock es de vital importancia una actuación rápida, pero a la vez metódica y precisa.Para que esto sea posible es necesario que tanto el veterinario como el/la auxiliar, que será la mano derecha del mismo, conozcan las bases tanto teóricas como prácticas…
Índice de contenidos
Introducción
El shock es un síndrome potencialmente mortal y multifactorial, a lo que habrá que enfrentarse, con toda probabilidad y en más de una ocasión, a lo largo de la carrera profesional como ATV. Al encontrarse frente a un paciente en shock es de vital importancia una actuación rápida, pero a la vez metódica y precisa.
Para que esto sea posible es necesario que tanto el veterinario como el/la auxiliar, que será la mano derecha del mismo, conozcan las bases tanto teóricas como prácticas de dicha situación.
Por tanto, este artículo estará dedicado a conocer qué es el shock y las distintas teorías que lo definen. Una vez claro a nivel terminológico, se describirán los tipos de shock que existen con sus respectivas definiciones, sintomatología y tratamientos y los distintos tipos de monitoreo esenciales que se ponen en práctica en caso de encontrarnos con un animal en shock.
De esta manera, en el presente artículo, se hará un recorrido por el mundo del shock partiendo desde lo más general (definición) a lo más concreto y específico (tipos y tratamiento), encontrándose así ante un trabajo plenamente bibliográfico sin entrar a describir ningún caso clínico.
Definiciones
En primer lugar y antes de entrar de lleno en materia es importante aportar una definición del shock en general.
A lo largo de la historia se han ido produciendo diferentes definiciones que se han modificado y completado con el avance de la ciencia. A día de hoy, y tras una serie de interminables discusiones (pues se está frente a un proceso complejo y multifactorial), se puede señalar una serie de características consensuadas por la mayoría de los autores.
La Sociedad Europea de Cuidados Intensivos, habla de un desorden circulatorio agudo que se produce cuando la circulación no es capaz de entregar oxígeno suficiente para cubrir las demandas de los tejidos, provocando así una disfunción celular.
Por tanto, se está hablando de una producción inadecuada de energía celular que suele ocurrir de manera secundaria a una mala perfusión celular, debido a un flujo sanguíneo bajo o mal distribuido, lo que causa una disminución crítica de la entrada de oxígeno a los tejidos y por consiguiente daño celular, en primera instancia reversible pero posteriormente irreversible.
En condiciones normales, el consumo celular es mucho menor que la liberación que se produce de oxígeno y nutrientes a los tejidos, incluso en situaciones de necesidad la extracción de oxígeno puede verse aumentada. Sin embargo, habrá ocasiones donde la demanda de oxígeno supere su suministro, provocando así una hipoxia celular, es decir un shock. Por lo tanto, independientemente del tipo de shock que haya que enfrentarse, habrá un desequilibrio entre la liberación de oxígeno y el consumo de oxígeno celular.
SIRS, sepsis, CARS y MODS
SIRS o síndrome de respuesta inflamatoria sistémica: se trata de una reacción inflamatoria grave del cuerpo a una influencia externa, pudiendo ser o no, un patógeno determinado el desencadenante.
Esta respuesta inflamatoria puede producirse por multitud de factores, como, por ejemplo:
- Quemaduras.
- Lesiones.
- Daño importante a los órganos.
- Reacciones alérgicas graves (anafilaxia).
- Inflamación de órganos como pancreatitis.
- Sangrado abundante.
- Insuficiencia de oxígeno en tejidos u órganos (isquemia): por ejemplo, un accidente cerebrovascular o un ataque cardíaco.
Se deben cumplir al menos dos (en perros) o tres (en gatos) de los siguientes cuatro criterios para poder hablar de SIRS:
- Temperatura:
- Perro: < 37.2 - > 39.2 ºC
- Gato: < 37.8 - >40 ºC
- Frecuencia cardíaca
- Perro: > 140 lpm
- Gato: < 140 - >225 lpm
- Frecuencia respiratoria
- Perro: > 30 rpm
- Gato: > 40 rpm
- Leucocitos:
- Perro: < 6 - >19 / µL
- Gato: < 5 - >19 / µL
Se habla de sepsis cuando el SIRS tiene un origen infeccioso, pudiendo ser este tanto bacteriano como vírico, fúngico o parasitario.
Paralelamente a la respuesta inflamatoria que se produce, se pone en marcha una respuesta antiinflamatoria, conocida como CARS (the Compensatory Anti-inflammatory Response Syndrome), teniendo como resultado a un paciente con inmunidad comprometida.
El resultado final si no se toman medidas a tiempo, puede llegar a ser un MODS (Multiple Organ Dysfunction Dyndrome), es decir la presencia de dos o más fallos orgánicos (Figura 1).
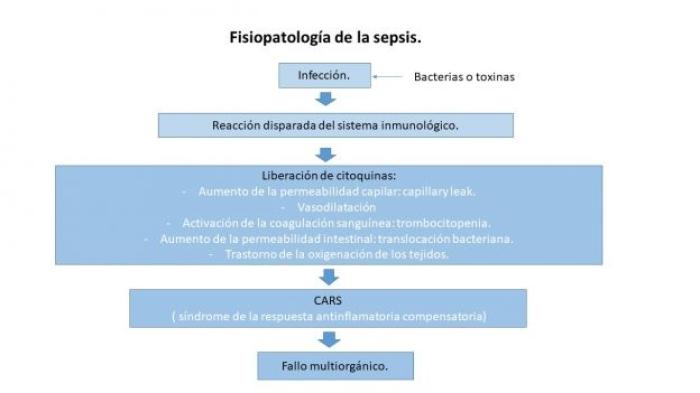
Figura 1. Fisiopatología de la sepsis. Blog Virginia, enfermera en UCI y Anestesia. SIRS, síndrome de respuesta inflamatoria sistémica (2 de junio de 2020).
Perfusión tisular
Antes de profundizar en cada uno de los tipos de shock, se hablará sobre las bases fisiológicas de la perfusión tisular, conocimiento esencial para abordar de manera adecuada esta afección.
Para entender de manera correcta el shock y sus distintas variantes es de suma importancia tener en cuenta y comprender los mecanismos que participan en la homeostasis de la perfusión tisular. Para ello se adjunta el siguiente diagrama, teniendo en cuenta que la causa del estado de shock se debe encontrar en uno o varios de estos puntos (Figura 2).
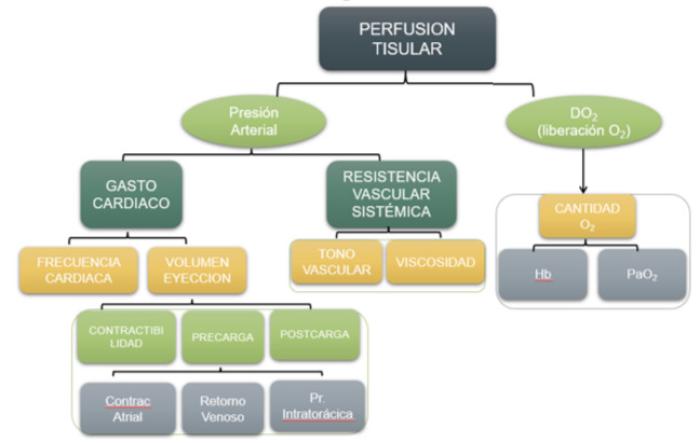
Figura 2. Mecanismos que participan en la homeostasis de la perfusión tisular.
La perfusión tisular consiste en el paso de fluidos a través del sistema circulatorio o sistema linfático hacia un órgano o un tejido, refiriéndose normalmente al suministro de sangre a un lecho, para garantizar requerimientos energéticos como el aporte de oxígeno o la eliminación de productos de desecho.
La perfusión tisular depende principalmente de la presión arterial (flujo sanguíneo) y la liberación de oxígeno a los tejidos (suministro de oxígeno). Cualquier alteración en alguno de estos marcadores, generará cambios en la perfusión tisular. Dependiendo de dónde se produzca dicha alteración, se estará ante a un tipo de shock u otro.
¿Cómo detectar el shock?
Para saber si el paciente se encuentra en estado de shock, se debe realizar una exploración física completa y pruebas analíticas complementarias. La sintomatología del paciente en shock se presenta en la siguiente tabla según si el shock es compensado, descompensado precoz o descompensado tardío. La evolución de estos parámetros será independiente del tipo de shock al que hay que enfrentarse (Figura 3).
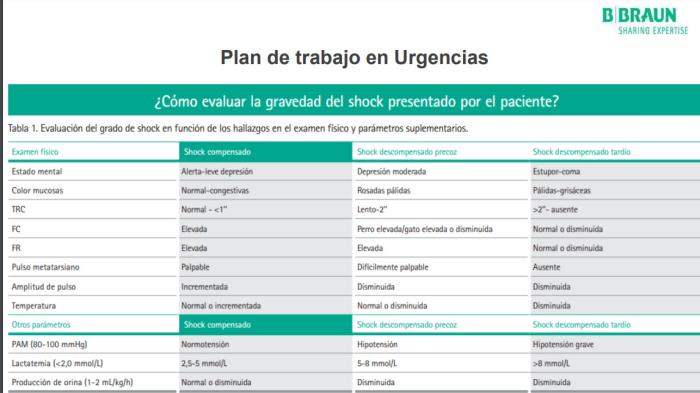
Figura 3. Protocolo de fluidoterapia de BBraun.
Tipos de shock
Existen diferentes clasificaciones de tipos de shock dependiendo de la bibliografía que hay. Se debe tener en cuenta que un paciente en estado crítico puede presentar diferentes tipos de shock de manera concomitante.
Shock circulatorio:
- Hipovolémico
- hemorrágico
- No hemorrágico
- Cardiogénico
- Distributivo:
- Séptico
- Anafiláctico
Shock no circulatorio:
- Hipoxémico
- Metabólico
Shock hipovolémico
Estado de inadecuada producción energética a nivel celular secundaria a hipoperfusión, comúnmente asociada a perdidas internas o externas de sangre y/o fluidos corporales (vómitos, diarreas, poliuria, etc.).
Antes de meterse en el tratamiento de shock hipovolémico, hay que intentar entender la distribución de fluidos en el cuerpo.
El 60 % del peso vivo de un animal es agua, y dentro del organismo está repartida en diferentes cavidades. El 40 % del fluido se encuentra dentro de la célula (espacio intracelular) y el 20 % fuera de la célula (espacio extracelular). El espacio extracelular se divide a su vez en el espacio intersticial (15 %) y el espacio intravascular (5 %). Estos compartimentos intercambian agua y solutos continuamente (Figura 4).
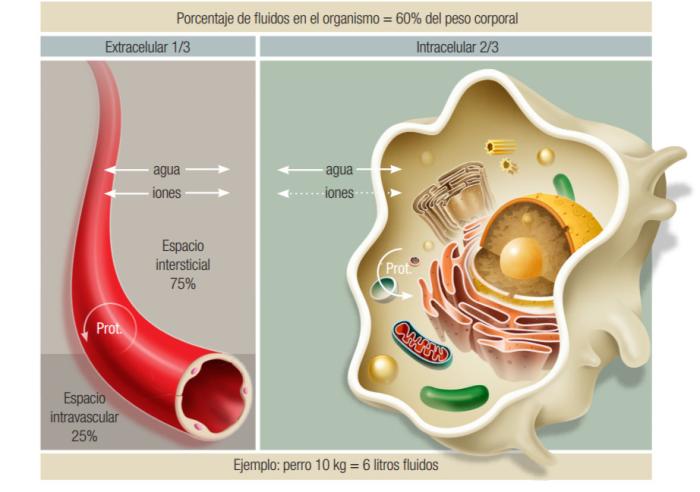
Figura 4. Shock hipovolémico (Manual de Fluidoterapia en pequeños animales, C. Fragío, Multimédica Edicones Veterinarias).
En un shock hipovolémico se puede estar ante un shock hipovolémico hemorrágico (pérdida de fluidos del compartimento intravascular) o, hipovolémico no hemorrágico (pérdida de fluidos en los compartimentos intersticial, intravascular, intracelular), cuyas causas pueden ser internas y/o externas.
Hemorrágico (déficit compartimento intravascular):
- Internas: traumatismos, lesiones vasculares cerradas, hemoperitoneo.
- Externas: hemorragias digestivas, hemorragias pulmonares, hematuria grave, lesiones vasculares abiertas.
No hemorrágicas: depleción de líquidos (déficit c. intravascular + c. intersticial + c. intracelular):
- Internas: pancreatitis, obstrucción intestinal, ascitis.
- Externas: deshidratación, vómitos, diarreas, poliuria, quemaduras de alto grado, etc.
Tratamiento: la base de la terapéutica del shock hipovolémico se basa en la administración de fluidos.
Shock hemorrágico
El principal objetivo en pacientes con shock hemorrágico es aumentar el volumen de sangre en el lecho venoso, es decir reponer las pérdidas de sangre al vaso.
La expansión agresiva de fluidos puede generar un aumento de sangrado en algunas regiones, por lo que se recomienda expandir sólo a los pacientes que presenten hipotensión arterial, buscando como objetivo PAS en el límite inferior (80-90 mmHg). En casos de shock hemorrágico asociados con traumatismo craneoencefálico, se recomienda mantener PAS 100 mmHg para no disminuir la presión de perfusión cerebral y no afectar de manera reversible la función cerebral.
Fluidos de elección
- Sangre entera fresca (resurrección hemostática) como primera elección, (valorar autotransfusiones).
- Concentrado globular + plasma (relación 1:1 o 1:2).
- Si no se dispone de hemoderivado: solución electrolítica balanceada (RL) hasta llegar a objetivo PAS + frenar el sangrado.
Consideraciones
- Empleo temporal de vendajes comprensivos ya sean abdominales o torácicos para de esta manera aumentar la presión en la cavidad y al mismo tiempo aumenta la reabsorción de fluido.
- Empleo de antifibrinolíticos:
- Ácido tranexámico: dosis de carga 10-15 mg/kg, seguido por infusión continua a 1-5 mg/kg/hora.
- Ácido épsilon amino caproico: dosis de carga 100-150 mg/kg seguido de 15 mg/kg/hora.
Shock no hemorrágico
Se debe tener en cuenta que la respuesta hemodinámica al shock hipovolémico es diferente en el perro y en el gato, ya que estos últimos están predispuestos a desarrollar edema pulmonar durante la expansión de fluidos. Aunque las indicaciones son diferentes para cada especie, en ambos casos se recomiendan bolos de solución electrolítica balanceada, generalmente RL.
- Cristaloides isotónicos: agua + iones. Corta permanencia en IV (tras 1 hora 25 % en IV y 75 % en intersticial).
- Ventajas: necesarios en deshidratados, fácilmente disponibles, larga vida en almacenamiento.
- Desventajas: tiempo de resucitación prolongado, puede requerir múltiples vías, riesgo de hipotermia, de edema intersticial y hemodilución.
Se recomienda RL o Isofundín. El exceso de cloro en solución salina puede promover el efecto de vasoconstricción a nivel renal. En necesario revaluar la variable fisiológica tras cada bolo.
Es muy importante tener en cuenta que una reposición muy agresiva con fluidos puede ocasionar una sobrecarga de volumen y empeorar el pronóstico del paciente.
- Cristaloides hipertónicos: atrae agua del compartimento intersticial y compartimento celular, por lo que está contraindicado en deshidratación. Deberá administrarse junto a terapia cristaloidea isotónicos.
- Ventajas: resucitación rápida con volúmenes mínimos. Mínimo riesgo de edemas intersticiales, disminución de la presión intracraneal.
- Desventajas: efecto a corto plazo, hipernatremia transitoria, hipotensión, broncoconstricción o arritmias con administración rápida, riesgo de sobrecarga de volumen, riesgo de flebitis.
- Coloides. agua + moléculas grandes. Indicado en hipoproteinemia (disminución presión oncótica) e hipovolemia marcada (restauración de la volemia de manera rápida cuando no haya compromiso intersticial). Aumenta presión oncótica, atraen líquido del intersticio, larga permanencia en IV. (uso controvertido debido a posibles efectos secundarios).
- Ventajas: resolución rápida de volúmenes mínimos, mínimo riesgo de edema intersticial, mayor prolongación del efecto, menor hemodilución.
- Desventajas/contraindicaciones:
- Coagulopatías: diluyen los factores de coagulación.
- Disminuyen TFG: predisposición a IRA.
- Hemorragias activas: aumentan la volemia y la presión arterial potenciando el sangrado.
- Cardiopatías: sobrecarga cardíaca.
- Interferencias en pruebas sanguíneas cruzadas.
Shock cardiogénico
Estado de metabolismo celular inadecuado secundario a la presencia de disfunción cardíaca a pesar de la existencia de un volumen intravascular adecuado.
En el shock caridogénico se pueden encontrar otros signos clíncos a parte de los nombrados anteriormente como soplo, ritmo de galope, disnea, tos, cianosis, anomalías en asucultación, arritmias, déficits de pulso, ascitis, derrame pleural y/o distensión yugular.
Tratamiento
El tratamiento del shock cardiogénico dependerá principalmente de la patología que lo genere y el tratamiento de soporte que necesite el paciente. Según la patología cardiaca que presente el animal el tratamiento irá enfocado a mejorar la contractibilidad, disminuir la precargar, controlar arritmias etc. A continuación, expondremos algunas de las patologías cardiacas que pueden generar un shock cardiogénico:
- Cardiomiopatía dilatada: el objetivo en el tratamiento de un paciente en shock cardiogénico por una cardiomiopatía dilatada consiste en oxigenar al paciente (mediante sonda nasal, mascarilla, jaula de oxígeno, etc.), aumentar la contractibilidad, disminuir la precarga y tratar las arritmias si las tuviera. A continuación, dejamos una lista con los fármacos y dosis recomendadas:
Aumentar contractibilidad
- Agonista adrenérgico β1: Dobutamina
- Inhibidores Fosfodiesterasa III: Pimobendan (0.4-0.6 mg/kg 24h)
- Digitalicos: Digoxina (5 μg/kg 12h)
Disminución Precarga VI:
- Diuréticos: Furosemida (1-4 mg/kg 6-12h; Ver CRI)
- Vasodilatadores: Benaceprilo (0.5 mg/kg 12-24h)
- Venodilatadores: Nitropusiato (solo urgencia)
Arritmias:
- Fibrilación atrial:
- Diltiazem 0.12-0.35 mg/kg bolo lento
- Procainamida: 6-8 mg/kg bolo lento (CRI)
- Taquicardia ventricular:
- Lidocaína 2 mg/kg Bolo (CRI)
- Procainamida 6-8 mg/kg bolo lento (CRI)
- Cardiomiopatía hipertrófica: por el contrario, en una cardiomiopatía hipertrófica el tratamiento va a estar enfocado a mejorar la relajación cardíaca (función diastólica), disminuir la precarga, prevenir del tromboembolismo pulmonar felino y el tratamiento de arritmias si las presentase.
Mejorar función diastólica
- Vasodilatadores: Benaceprilo (0.5 mg/kg 12-24h)
- β-Bloqueantes:
- Esmolol (CRI)
- Atenolol 6.25-12.5 mg/gato 12h
- Bloqueantes canales Calcio:
- Diltiazem 7.5 mg/kg 8h
- Diltiazem retard 45 mg/kg PO cada 24 h
Disminución precarga
- Pleurocentesis ante derrame pleural
- Diuréticos: Furosemida (1-4 mg/kg 6-24h)
- Venodilatadores: Nitropusiato (solo urgencia)
Tromboembolismo distal felino
- Prevención y tratamiento: Fraxiparina 100UI /12h
Taquicardia supraventricular
- Esmolol (CRI)
Taponamiento cardíaco: en el taponamiento cardíaco el pericardio se encuentra lleno de líquido, lo que impide una buena funcionalidad y contracción cardíaca. El tratamiento consiste en realizar una pericardiocentesis (drenar el pericardio) o una pericardiectomía.
Shock distributivo
Estado de metabolismo celular inadecuado asociado a la presencia de fallo circulatorio e hipotensión arterial persistente a pesar de un volumen intravascular adecuado. Se puede dividir en shock séptico y shock anafiláctico.
Es de vital importancia diferenciar el estado en el que llega el paciente. Puede encontrarse con los siguientes casos:
Shock séptico
Síndrome causado por la infección del huésped por microorganismos y su respuesta inflamatoria sistémica (SIRS).
Los pacientes con mayor riesgo de padecer sepsis/shock séptico son los que sufren politraumatismos severos, procedimientos quirúrgicos complicados, inmunodeficiencias y los que estén en condiciones médicas debilitantes.
Tratamiento: el tratamiento de un shock séptico es multifactorial e implica un examen riguroso y continuo del animal, valorando la respuesta al tratamiento continuamente.
Los principales puntos a seguir en un shock séptico son:
- Administración de oxígeno: mediante mascarillas, gafas nasales, sondas nasales, etc. Algunos pacientes que no son capaces de mantener una ventilación efectiva, será necesaria la ventilación mecánica.
- Fluidoterapia: hay valorar los electrolitos del paciente y decidir qué tipo de fluido es necesario. (Ver sección fluidoterapia shock hipovolémico).
- Antibioterapia: será necesario localizar el lugar de la infección y si es posible tomar una muestra para la realización de un cultivo y antibiograma y poder dar el antibiótico específico para ese paciente.
- Soporte hemodinámico:
- Vasopresores: noradrenalina, dopamina, dobutamina, etc.
- Ionotrópicos: si mediante ecocardiografía se ha estimado que la contractibilidad cardíaca no es buena y se sospecha de un bajo gasto cardíaco, se podrían administrar fármacos ionotrópicos positivos.
- Hemoderivados: se podrían utilizar en pacientes con anemias o hipoproteinemia para mejorar la perfusión tisular. La elección del tipo de hemoderivado dependerá de las alteraciones analíticas que se encuentren.
- Plasma fresco congelado: aumentar volumen sanguíneo, soporte oncótico, coagulopatías, etc.
- Transfusión albumina.
-
- Concentrado eritrocitos.
- Trastorno de la coagulación: los pacientes con shock séptico pueden desarrollar trastornos de la coagulación, dependiendo de si lo ha desarrollado o no pondremos un tipo de tratamiento y otro.
- Prevención: Fraxiparina 100 UI / 24h
- Terapéutico: Fraxiparina 500 UI/24h + transfusión de plasma
- Otras terapias complementarias:
- Trastornos digestivos: para prevenir la úlcera por estrés.
- Omeprazol 0.3-1 mg/kg 24h
- Sucralfato
- Alimentación oral cuanto antes o en su defecto nutrición parenteral (muy importante).
- Analgesia: en función del paciente y la causa es necesario administrar analgesia: Metadona, buprenorfina, fentanilo, CRI lidocaína, etc.
- Control glucemia: ei hipoglucemia: administrar de 0.5 a 1 ml de glucosa al 50 % en bolo lento.
- Trastornos digestivos: para prevenir la úlcera por estrés.
Shock anafiláctico
Reacción inflamatoria exagerada liderada por IG-E, asociada a la liberación masiva de mediadores inflamatorios, causada por medicaciones, vacunas, contrastes yodados, trasfusiones, picaduras de insectos, etc.
Tratamiento: en estos casos el tratamiento está enfocado a disminuir la reacción inflamatoria generalizada. Para ello se puede administrar corticosteroides como la metilprednisolona 4-10 mg/kg y antihistamínicos Difenhidramina 1mg/kg. Estos pacientes deben ir monitorizados, si se mantienen hipotensos a pesar de la administración de fluidoterapia se deberá administrar vasopresores en infusión continua.
Shock hipoxémico
En este tipo de shock se genera por una disminución de cantidad de oxígeno en sangre. Las causas son: anemia, enfermedad pulmonar severa, intoxicación monóxido carbono, metahemoglobinemia (Paracetamol en gatos).
Shock metabólico
En este caso existe una mala utilización del oxígeno ofrecido a las células. Caracterizado por un metabolismo anormal celular. Las causas más frecuentes son la hipoglucemia, disfunción mitocondrial (cianuro) o intoxicación por chocolate, etc.
Tratamiento: el tratamiento de shock hipoxémico y metabólico dependerá de la causa subyacente.
Monitorización de un paciente en shock
Como SE ha mencionado anteriormente los pacientes que se encuentran en shock tienen que ser evaluados y monitorizados continuamente. Estos pacientes deberían de ir conectados a monitores multiparamétricos para poder actuar rápidamente ante cualquier empeoramiento del paciente. Se va a especificar algunos de los parámetros a monitorizar.
Presión arterial sistémica no invasiva e invasiva
Tradicionalmente se han usado equipos de Doppler para medir la tensión de manera no invasiva, sin embargo, actualmente existen equipos de última generación que ofrecen una mayor fiabilidad en sus resultados. El inconveniente principal de los equipos Doppler es que solo mide la presión sistólica.
Es muy importante elegir bien el manguito a usar, ya que si el tamaño no es el adecuado los resultados pueden salir falseados (manguito pequeño: presión erróneamente alta; manguito grande: presión erróneamente baja).
Por otro lado, el método invasivo para la medicación de la presión sanguínea se realiza colocando un catéter arterial a un transductor de presión y una conexión a monitor. Es de gran utilidad en pacientes con shock hipovolémico o shock séptico ya que permite determinar los volúmenes de reemplazo y los vasopresores a emplear para lograr una buena presión (>95 mmHg presión sistólica; >50mmHg presión diastólica; > 65mmHg de presión media).
Índice de shock
Los pacientes con shock hemorrágico con pérdidas superiores al 15 % del volumen se van a identificar fácilmente pues presentan signos clínicos evidentes, como mucosas pálidas, taquicardia, etc. El problema es cuando hay que enfrentarse a un shock oculto o a una hemorragia aguda pues en estos casos los parámetros vitales su pueden mostrar relativamente normales.
Ante esto, hay que utilizar el índice de shock, es decir, el cociente entre la frecuencia cardíaca y la presión arterial. En perros el límite superior es entre 0.9-1, con un grado de precisión alto, sobre todo en el caso de shock hemorrágico. En cuanto a felinos los estudios a día de hoy, no son determinantes.
Variables dinámicas de monitoreo hemodinámico
La monitorización hemodinámica permite obtener información sobre el funcionamiento cardiovascular del paciente crítico, siendo fundamental para una aproximación diagnóstica y para la guía terapéutica del paciente con hipoperfusión tisular.
Tanto la hipervolemia como la hipovolemia han demostrado ser perjudiciales en pacientes hospitalizados en cuidados intensivos, por lo que es de vital importancia mantener a los pacientes críticos en estados euvolémicos.
La expansión de volumen constituye la principal terapia en las situaciones de inestabilidad hemodinámica, aunque sólo un 50 % de los pacientes responden al aporte de fluidos, incrementando el volumen sistólico.
Lactato
La medición de la lactemia en pacientes en estado de shock, se utiliza como una herramienta importante que proporciona datos pronósticos y que puede ayudar en el control de la respuesta a un tratamiento. Las anormalidades circulatorias pueden llevar a un desequilibrio entre la oferta y el consumo de O2, dando lugar a una hipoxia tisular global, lo cual se verá reflejado con un aumento en las concentraciones de lactato en sangre. Los niveles de lactato también pueden verse alterados por otros mecanismos no hipóxicos, sobre todo en caso de sepsis. Hay que tener en cuenta que este biomarcador debe de ser interpretado en el contexto clínico del paciente y cotejado con otros parámetros para poder general así un monitoreo integral. La disminución del lactato con el transcurso de las horas se conoce como aclaramiento del lactato, lo que se considera un factor pronóstico positivo. Sin embargo, si los niveles de lactato se mantienen o se incrementan, se podría considerar un factor pronóstico negativo. Es importantes ser conscientes que las concentraciones altas de lactato iniciales no son un factor pronóstico negativo.
Ecocardiología
Sin entrar en demasiados formalismos, apuntar que la ecocardiografía es una herramienta muy útil a la hora de diagnosticar el tipo de shock, el tratamiento y el seguimiento de los pacientes con inestabilidad hemodinámica, ya que nos permite valorar múltiples aspectos sobre el funcionamiento cardíaco y circulatorio del animal de una manera cero invasiva.
Saturación en oxígeno de sangre venosa
La saturación venosa de oxígeno (SvO2) es un marcador que refleja el equilibrio entre la disponibilidad de oxígeno hacia los tejidos (DO2) y las necesidades de consumo con los mismos (VO2). Podríamos decir que una SVO2 baja refleja un desequilibrio entre la DO2 y la VO2. Por tanto, la detección de niveles de SVO2 inferiores a 68-70 % en pacientes hospitalizados debería de preocuparnos y ser investigada y tratada.
Electrolitos, y equilibrio ácido base
Los pacientes en shock se encuentran generalmente en estado de acidosis metabólica, debido a la acumulación de ácido láctico por la falta de perfusión celular. Conocer el valor de los electrolitos (Na, K, Ca y Cl) sirve para elegir de manera correcta el fluido adecuado a administrar al animal.
Glucemia
Los estados iniciales de shock son hiperdinámicos y consumen mucha energía, ya que la glucosa es liberada de inmediato como elemento energético. Sin embargo, en cuadros finales de shock se suelen producir hipoglucemias extremas, las cuales deberán de ser corregidas de forma inmediata.
Otras mediciones
Unas de las mediciones en pacientes de shock que siempre deberían de hacerse son: mediciones de hematocrito, sólidos totales y hemoglobina, sobre todo en pacientes con shock traumático hemorrágico. También se puede valorar la serie blanca y ver la evolución de los glóbulos blancos. De la misma manera se deberían de hacer análisis de orina, diuresis, sedimento urinario y creatinina.
Otros sistemas de monitoreo más avanzados
Tromboelastografía, calcio iónico, amiloide sércio A, proteína C reactiva, etc.
Conclusión
Como se puede deducir tras la lectura de este artículo, la aproximación a un paciente en shock y su tratamiento es algo muy complejo, pues a raíz de esta afección se desencadenan distintas patologías, las cuales habrá que tratar de una manera u otra según su naturaleza. Sin embargo, para llegar a este tratamiento hay un proceso previo, el cual requiere de la realización de distintos tipos de pruebas y monitoreos.
Como se ve, el hecho de aplicar un tipo de tratamiento u otro, es determinante y crucial para la recuperación o el empeoramiento del animal, sobre todo a nivel de fluidoterapia. Por lo que es de vital importancia que tanto el veterinario, como en este caso el/la auxiliar tengan unas bases sólidas y actualizadas sobre perfusión tisular y los distintos tipos de fluidos a aplicar en cada una de las patologías a las que se podrían enfrentar.
Destacar que, como ciencia, la veterinaria es una disciplina que está en constante evolución y renovación. Por ello, es muy importante estar al día en cuando a las nuevas publicaciones e ir revisando y modificando los datos con los que se maneja. A raíz de esto es destacable señalar que, la mayoría de los estudios sobre los que se ha basado para escribir este artículo están enfocados al mundo canino. A día de hoy, los estudios sobre shock felino, si se comparan con el shock en perros, son ínfimos por lo que aún queda un largo camino y mucho por conocer en este sentido.
Bibliografía
- Castro J., Hernández G., Bruhn A. et Romero C. Sepsis y falla multiorgánica. 3ª Edición. Editorial Mediterráneo. 2011. España.
- Cortés García C. et Castillo Magán N. Procedimientos en medicina de urgencas para el clínico de pequeños animales. 2ª edición. Multimédica ediciones veterinarias. 2019. Barcelona.
- Engel Manchado J. et García Guasch L. Manual del ATV. 2ª edición. Multimédica ediciones veterinarias. 2019. Barcelona.
- Engel Manchado, J. et Salom Morell, J. Manual de protocolos de urgencias de los signos clínicos al tratamiento. Multimédica ediciones veterinarias. 2019. Barcelona.
- Fragío Arnold C. Manual de fluidoterapia en pequeños animales. Multimédica ediciones veterinarias. 2018. Barcelona.
- Mouly J. et Donati P. Manejo integral del shock en perros y gatos. Multimédica ediciones veterinarias.2020. Barcelona.
- Mouly J. Emergencias y cuidados en pequeños animales. Multimédica ediciones veterinarias.2018. Barcelona.
- Thompson M.S. Diagnóstico diferencial clínico en pequeños animales 3ª Edición. Multimédica ediciones veterinarias. 2019. Barcelona.
 by Multimédica
by Multimédica