Citología hepática en el perro y el gato
Resumen breve
El hígado es un órgano complejo y es un punto clave del metabolismo de carbohidratos y lípidos, de la síntesis de proteínas, la desintoxicación de componentes endógenos y exógenos, de fármacos y de toxinas1.Índice de contenidos
Introducción
El hígado es un órgano complejo y es un punto clave del metabolismo de carbohidratos y lípidos, de la síntesis de proteínas, la desintoxicación de componentes endógenos y exógenos, de fármacos y de toxinas1.
La mayoría de las patologías hepáticas requiere una evaluación microanatómica que oriente el daño tisular o el infiltrado celular respecto a las estructuras portal y centrolobulillar. Mediante citología esta determinación no es posible, y el examen se centra principalmente en la evaluación de cambios citoplasmáticos y nucleares de los hepatocitos, en la morfología de estos, en la presencia de células inflamatorias o en la búsqueda de material extraño o de indicios de neoplasia2.
Toma de muestras
Los signos clínicos y los parámetros bioquímicos y hematológicos no siempre tienen correlación con los hallazgos micropatológicos2. Sin embargo, las principales indicaciones para realizar citología hepática son:
- el incremento de enzimas hepáticas de forma persistente
- anomalías en los marcadores de funcionalidad hepática
- hepatomegalia (detectada mediante palpación o por pruebas de imagen)
- alteraciones del parénquima (alteraciones en la ecogenicidad o lesiones nodulares)1.
La ecografía es muy sensible detectando patologías hepáticas pero poco específica para determinar la causa. Se ha demostrado que el área de muestreo influencia mucho los hallazgos citológicos, e idealmente para solventar esta limitación deberían muestrearse diferentes áreas, incluyendo diferentes lóbulos hepáticos. En caso de encontrar lesiones focales (p. ej., nódulos) estas deben puncionarse2.
La punción con aguja fina es el método utilizado para preparar las extensiones citológicas, utilizando jeringas de 6 a 12 ml y agujas de entre 20-23 G1, o de hasta 27 G. Generalmente, en órganos con un elevado componente vascular, se prefiere realizar punción sin aspiración para minimizar la hemodilución, sin embargo, también se describe el uso de punción con aspiración utilizando una jeringa parcialmente precargada con aire1. Aunque este procedimiento es seguro en la mayoría de los casos, algunas de las posibles complicaciones incluyen hemorragia, perforación accidental de vías biliares de gran calibre y posible diseminación de lesiones (p. ej., siembra e implantación de células neoplásicas en cavidad o pared abdominal, o rotura de un absceso)2. El riesgo de sangrado debería evaluarse de forma previa a la realización del procedimiento (p. ej., concentración plaquetaria, tiempos de coagulación, o idealmente tromboelastografía) y en pacientes con riesgo elevado de sangrado, se recomienda monitorización posterior a la toma de muestras.
Arquitectura tisular y tipos celulares
La unidad funcional del hígado es el lobulillo hepático. Se trata de una estructura tridimensional con forma de prisma hexagonal. Por el centro discurre la vena centrolobulillar y en los vértices se encuentran los espacios porta. Entre ambas estructuras se encuentran los sinusoides hepáticos y los hepatocitos. En los espacios porta o tríadas se encuentra una rama de la arteria hepática, una rama de la vena porta y un conducto biliar. La sangre arterial y venosa discurre desde el espacio porta hacia el centro del lobulillo, desembocando en la vena centrolobulillar2.
Se encuentran diferentes células de forma normal en el examen citológico del hígado2.
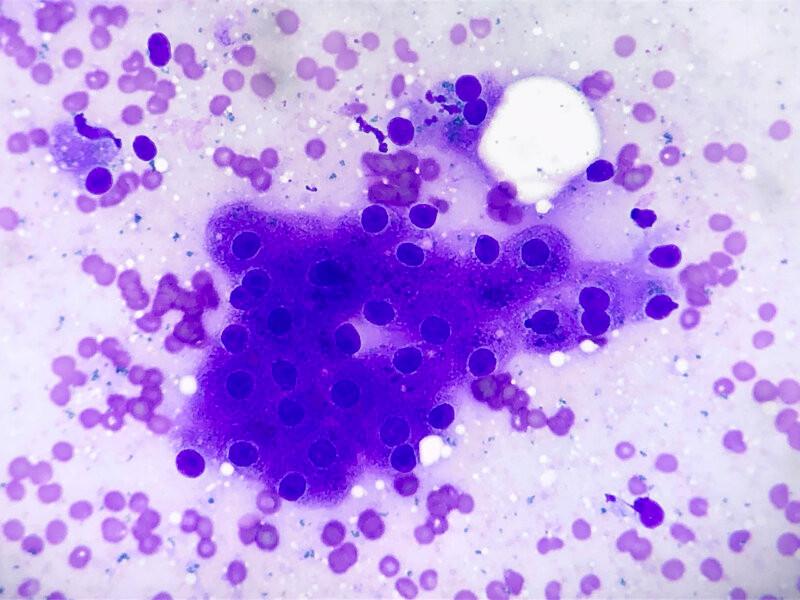
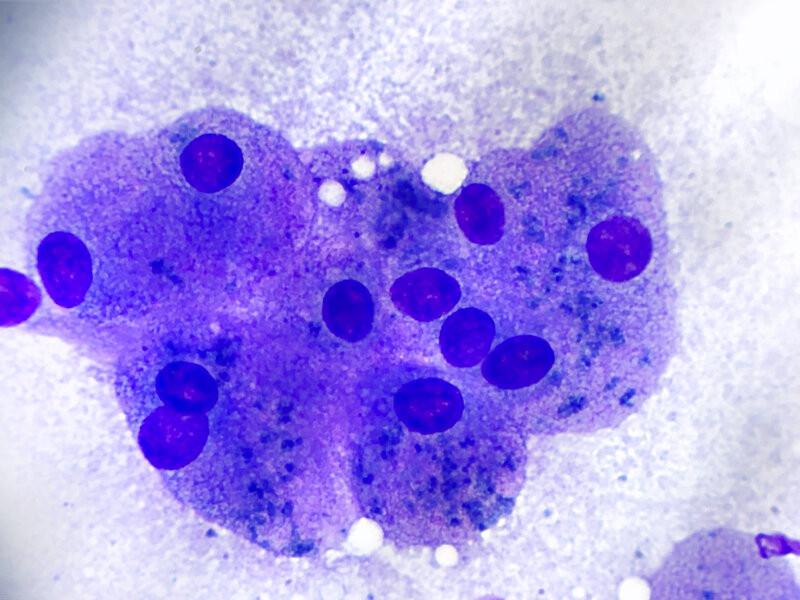
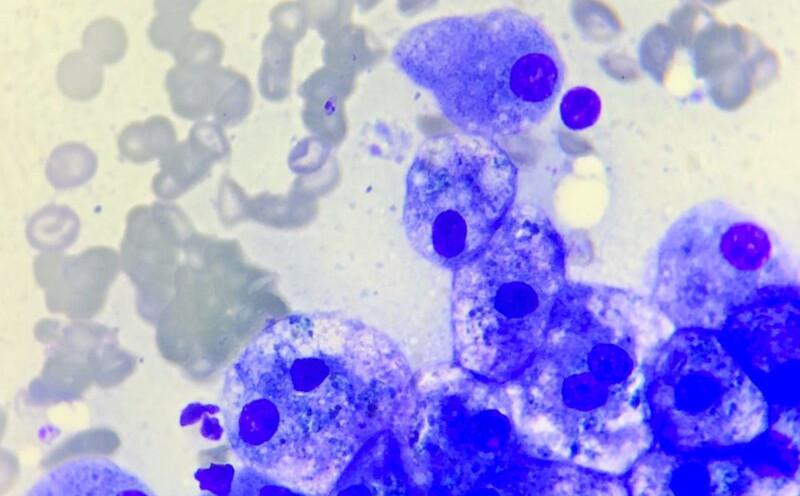
- Hepatocitos: son la célula predominante. Generalmente exfolian en grupos cohesivos de gran tamaño que en ocasiones tienen estructura trabecular. Se trata de células epiteliales con morfología redondeada a poligonal y una abundante cantidad de citoplasma anfofílico (rosa-azul). Con frecuencia tienen un pigmento azul verdoso y granular consistente con lipofuscina (ver apartado de pigmentos más adelante). Los núcleos son redondos, se encuentran en posición central o paracentral, con cromatina finamente punteada a granular y un único nucleolo prominente (Figura 1A).
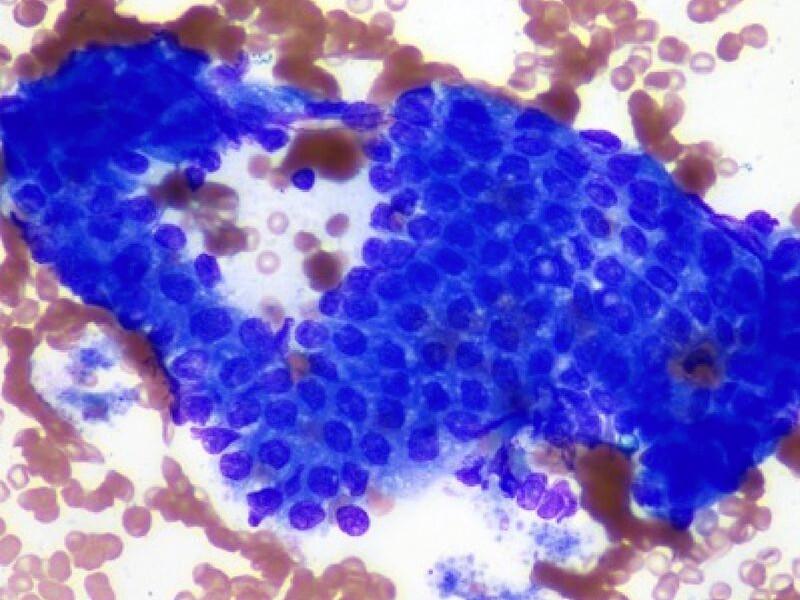
- Células de epitelio biliar (colangiocitos): se observan de forma esporádica en los aspirados de hígado. Son pequeñas células cuboidales con una escasa cantidad de citoplasma azul claro, un núcleo central hipercromático y se disponen en grupos bidimensionales (Figura 1B). Los colangiocitos de vías biliares de gran tamaño o de vesícula biliar tienen morfología columnar y se disponen en empalizada. Cuando contienen pequeñas vacuolas claras en el citoplasma puede indicar hiperplasia reactiva o incremento de la actividad secretora. Su número aumenta en procesos hepáticos reactivos e inflamatorios, con mínimas atipias nucleares. Al contrario, en procesos neoplásicos sí se observan atipias nucleares de forma significativa.
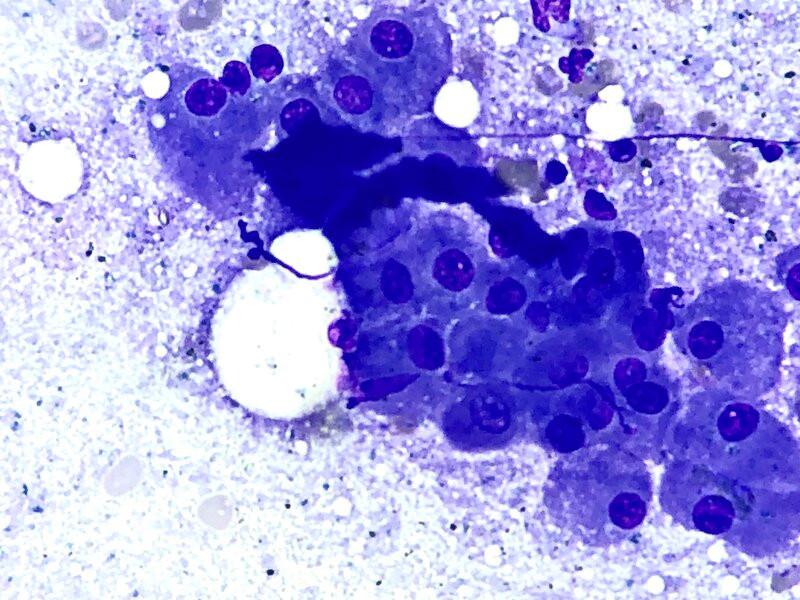
- Células de Ito: también llamadas células estrelladas hepáticas o lipocitos hepáticos, son células redondas con una abundante cantidad de citoplasma que contiene lípidos con una alta concentración de vitamina A. Se encuentran en bajo número, solitarios y dispersos entre los hepatocitos (Figura 1C). También son las encargadas de producir la matriz extracelular y colágeno en el proceso de fibrosis hepática.
- Células de Kupffer: son macrófagos hepáticos. En su forma quiescente no se identifican fácilmente por su escasa cantidad de citoplasma y núcleo hipercromático. Son fácilmente detectables cuando se encuentran activados, mostrando un citoplasma abundante con vacuolas citoplasmáticas y actividad fagocítica.
- Mastocitos: se encuentran de forma normal en el hígado, aunque en muy bajo número. La morfología es la de los mastocitos de otras localizaciones, con gránulos citoplasmáticos metacromáticos en grado variable.
- Linfocitos: se considera normal encontrar de forma aislada linfocitos pequeños bien diferenciados, ya que hay linfocitos T en el espacio de Disse y en la tríada portal de forma fisiológica.
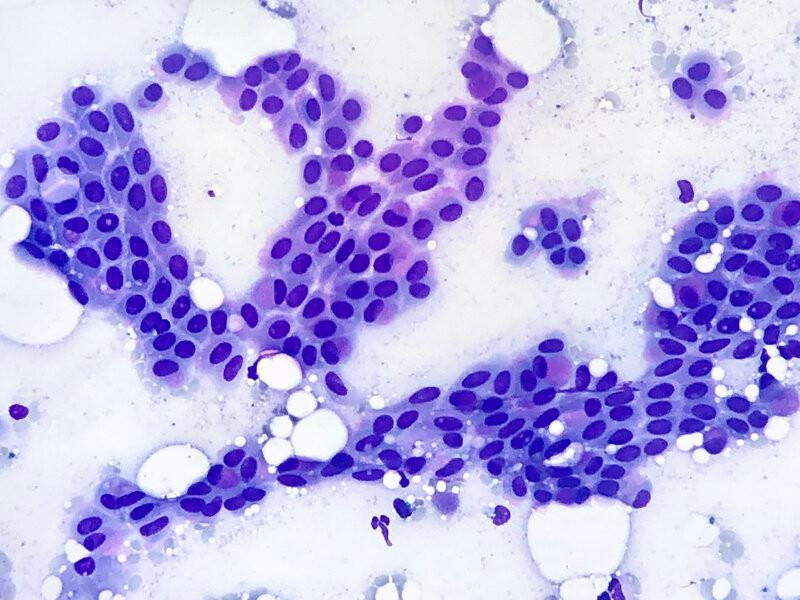
- Células mesoteliales: proceden del peritoneo parietal y/o visceral. Se reconocen como células poliédricas, con una moderada cantidad de citoplasma azul medio y frecuente disposición en lámina (Figura 1D).
Pigmentos
Son varios los pigmentos que pueden observarse en los hepatocitos de forma normal o patológica. La lipofuscina es el pigmento que se observa con mayor frecuencia en comparación con la bilis, el cobre o la hemosiderina. Aunque la mayoría de las veces se puede aproximar la etiología del pigmento mediante las tinciones de tipo Romanowsky, para una confirmación certera se recomienda realizar tinciones especiales, como se detalla a continuación1–3.
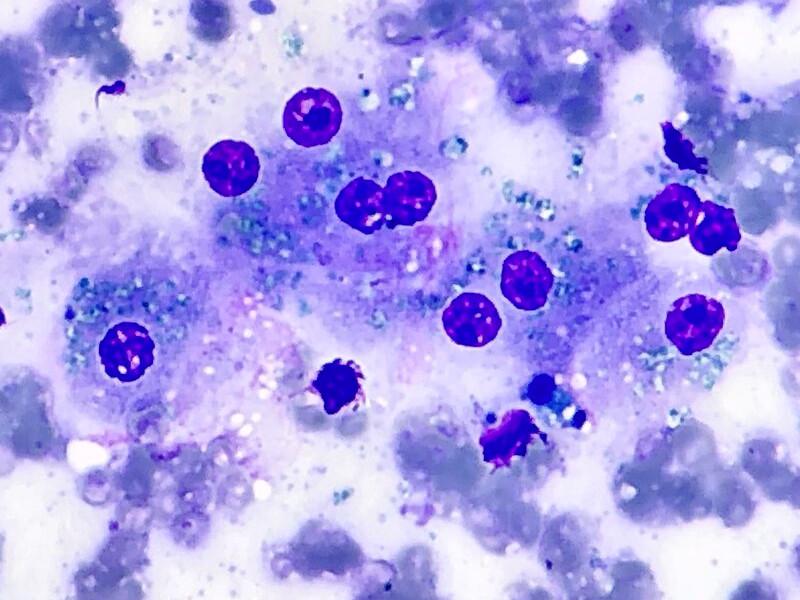
- Lipofuscina: citológicamente se reconoce como pequeños gránulos citoplasmáticos irregulares en el interior de los hepatocitos de color azul o azul verdoso. Es un pigmento no patológico que refleja el envejecimiento normal de las células. Está formada por productos de deshecho que la célula no puede eliminar y que se acumulan en el interior de lisosomas. Este pigmento puede verse en grandes cantidades en perros y gatos mayores (Figura 2A). Para su confirmación puede utilizarse la tinción de Schmorl, aunque debido a la alta prevalencia no suele ser necesario.
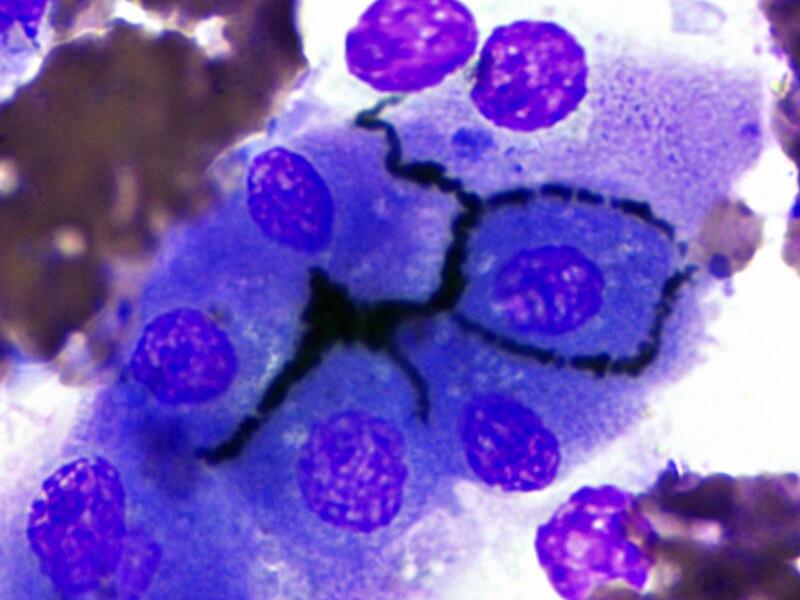
- Bilis: este pigmento es de color verde oscuro a negro y puede observarse tanto en el interior de los hepatocitos como alrededor de ellos en el interior de los canalículos biliares (Figura 2B). En este último caso se encuentra formando acúmulos con morfología linear. Ambos hallazgos indican colestasis y pueden preceder a la hiperbilirrubinemia. Las causas de colestasis biliar pueden agruparse en hemólisis prehepática, alteraciones hepáticas o posthepáticas. Aunque no se utiliza de forma rutinaria en citología, la tinción de Hall o la tinción Fouchet-Van Gieson pueden utilizarse para confirmar su presencia.
- Hemosiderina: es un pigmento granular que contiene hierro, y resulta de la rotura del grupo hemo tras la fogocitosis de eritrocitos. La apariencia citológica es similar a la observada en otras localizaciones, como bazo o médula ósea, con un color que varía entre marrón amarillento hasta azul-negruzco. Puede verse tanto en el interior de hepatocitos como en el citoplasma de macrófagos (con eritrofagia concurrente o sin ella). El aumento de hemosiderina puede observarse en condiciones inflamatorias crónicas, en anemia hemolítica, en deficiencia de piruvato quinasa, tras transfusiones repetidas o inyecciones de hierro. La tinción especial que se utiliza para demostrar la presencia de hemosiderina es el azul de Prusia.
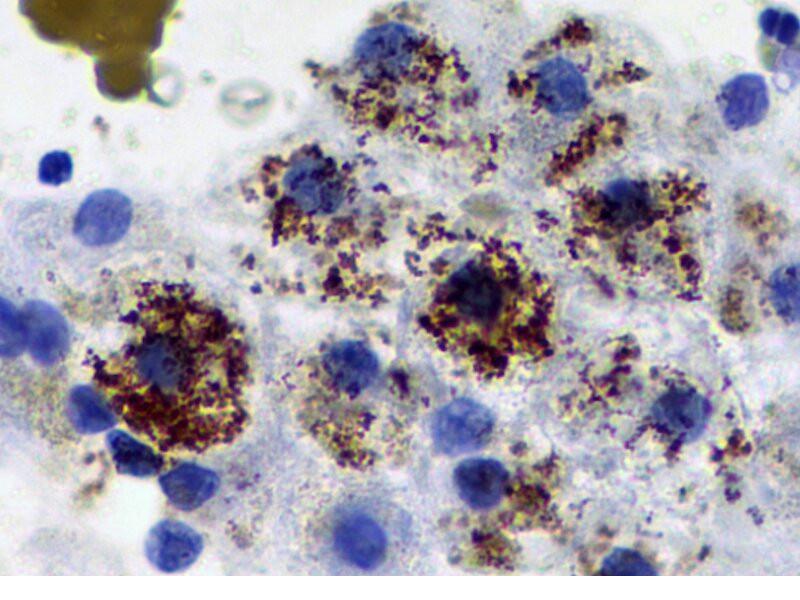
- Cobre: su acúmulo dentro de los hepatocitos puede apreciarse al visualizar estructuras granulares, cristalinas, gruesas, con una sutil tinción azul pálido (Figura 2C). Para una confirmación se pueden utilizar tinciones especiales como la tinción de rodamina (Figura 2D) o mediante el ácido rubeánico. Sin embargo, más importante que determinar si existe acúmulo de cobre o no, es la cuantificación, que se puede realizar utilizando estas tinciones en secciones histológicas o mediante el análisis de cobre mediante espectroscopia de absorción atómica utilizando tejido fresco. En el gato, el acúmulo de cobre es un fenómeno muy poco frecuente. En el perro se describe con relativa frecuencia como consecuencia de hepatopatías crónicas o como causa de disfunción hepática en razas predispuestas genéticamente al acúmulo patológico de cobre como el Bedlington terrier, el doberman, el West Highland White terrier, el Skye terrier y el labrador retriever.
Condiciones no neoplásicas
Cambios degenerativos vacuolares
Si bien no es técnicamente correcto, el término “cambio/degeneración vacuolar” está ampliamente aceptado para referirse a un acúmulo de material que no se tiñe en el interior del citoplasma de hepatocitos, siendo un daño inespecífico y hasta cierto punto reversible. Los tipos de degeneración citoplasmática se clasifican como lipídica o no lipídica2.
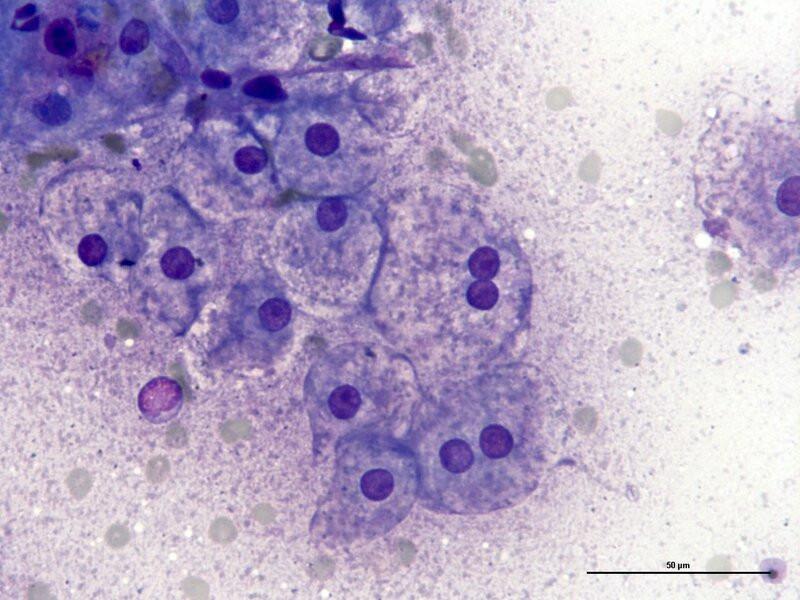
La degeneración vacuolar no lipídica se identifica como una disminución de la densidad del citoplasma (rarefacción) de grado variable, generalmente más marcada en la periferia celular (Figura 3A). Puede deberse a un acúmulo de glucógeno o de agua intracelular.
- Glucógeno: el acúmulo de glucógeno se observa como un material citoplasmático con límites mal definidos que no se tiñe mediante tinciones de tipo Romanowsky. Para diferenciar entre el acúmulo de glucógeno o el de agua se utiliza la tinción de PAS (Periodic Acid-Schiff). Se trata de un cambio inespecífico que de forma frecuente en perros y raramente en gatos puede deberse a exposición crónica a corticosteroides endógenos (p. ej., hiperadrenocorticismo) o exógenos. Otras causas incluyen exposición a algunos fármacos, por enfermedad crónica (p. ej., inflamación), secundario a una neoplasia o puede encontrarse en la hiperplasia nodular regenerativa, frecuente en perros mayores. De forma congénita se ha encontrado en algunas razas, incluyendo bichón maltés, pastor alemán y retriever de pelo rizado1–3.
- Agua: el acúmulo de agua intracelular (cambio hidrópico) se produce cuando las células no son capaces de mantener la homeostasis debido a una disminución en la integridad de la membrana celular. Es el principal cambio de daño hepatocelular secundario a sustancias hepatotóxicas o a hipoxia2.
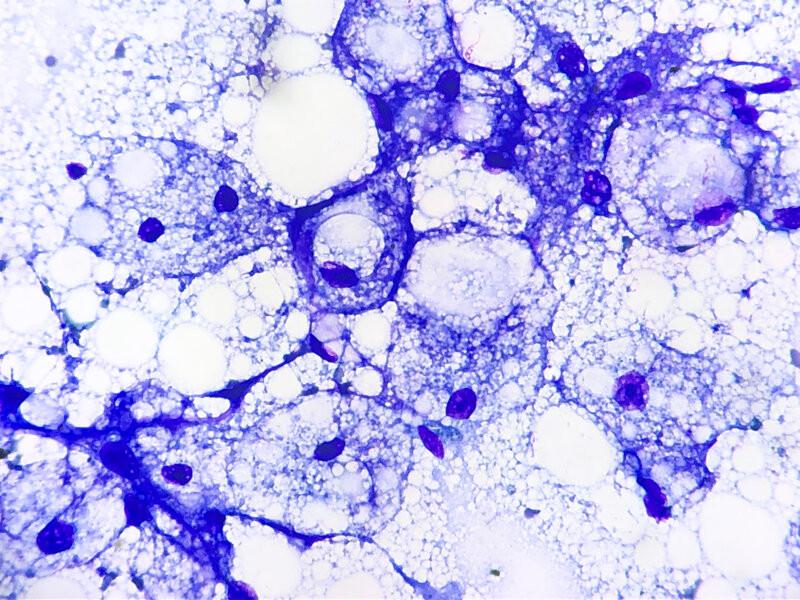
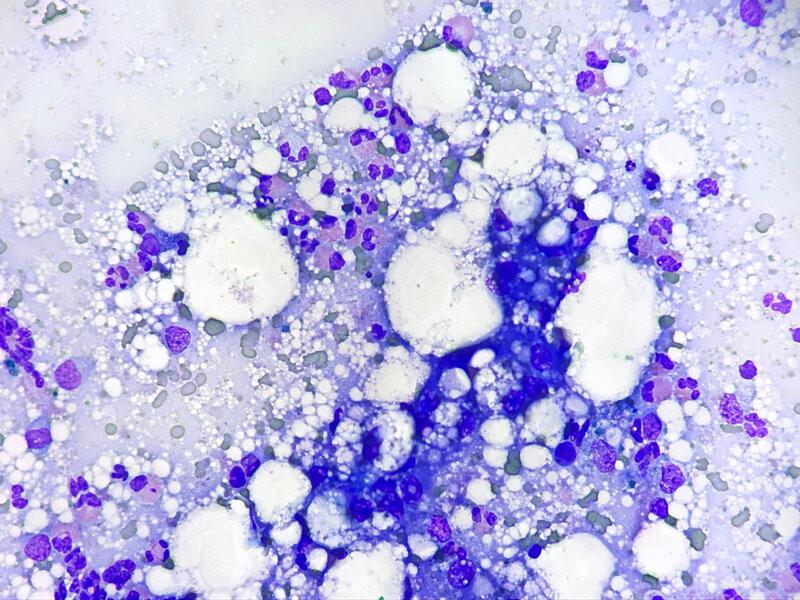
La degeneración vacuolar lipídica, también denominada lipidosis o esteatosis, es el acúmulo de triglicéridos en el citoplasma de los hepatocitos. Morfológicamente puede diferenciarse entre esteatosis micro- o macrovesicular en función de si el tamaño de las vacuolas citoplasmáticas es menor o mayor al tamaño del núcleo, respectivamente. Para diferenciarlo con certeza de la degeneración vacuolar no lipídica puede utilizarse tinciones especiales como la tinción de rojo aceite O (Oil Red O en inglés) que detecta grasas neutras. Sin embargo, esta tinción no se utiliza de manera rutinaria debido a que las preparaciones no pueden haber sido fijadas con soluciones alcohólicas previamente, ya que estas disuelven los lípidos. Además, este cambio degenerativo es fácilmente identificable citomorfológicamente en la mayoría de los casos (Figura 3B)2. Es preciso visualizar las vacuolas lipídicas en el interior de los hepatocitos, ya que detectar una cantidad variable de estas en el fondo de la preparación podría reflejar un muestreo de grasa mesentérica3.
Las causas de este tipo de degeneración incluyen disminución en la utilización de triglicéridos o alteraciones en el metabolismo de lipoproteínas como consecuencia de problemas metabólicos, tóxicos, hipóxicos o degenerativos. Una de las principales causas es la diabetes mellitus, tanto en perros como en gatos. La anorexia puede causar este tipo de degeneración como consecuencia de la movilización de lípidos desde tejido adiposo hacia los hepatocitos. Esto es especialmente frecuente en gatos, en los que la disminución de la ingesta puede ocurrir de forma primaria (idiopática), o ser secundaria a otras enfermedades como pancreatitis crónica, diabetes mellitus, colangitis, enfermedad inflamatoria intestinal, linfoma u otras neoplasias. En cachorros muy jóvenes de razas pequeñas se asocia a hipoglucemia severa y anorexia. Por efecto de drogas o toxinas se produce un daño mitocondrial y la lipidosis frecuentemente es microvesicular, al igual que la resultante de la disminución en la síntesis de apoproteína y por problemas en la secreción de lipoproteínas1,2.
Cambios nucleares
El principal cambio observable a nivel nuclear es la anisocariosis. La variación del tamaño nuclear suele deberse a cambios regenerativos, consecuencia de hiperplasia nodular o secundarios a un daño hepatocelular. Sin embargo, no es un método fiable para diferenciar entre estas condiciones y neoplasia hepatocelulares bien diferenciadas. Al aumentar la edad, se observa un aumento de hepatocitos binucleados (probablemente por hiperplasia nodular regenerativa); así como un ratio núcleo:citoplasma disminuido, que se debe al aumento del volumen citoplasmático sin aumento del tamaño nuclear2.
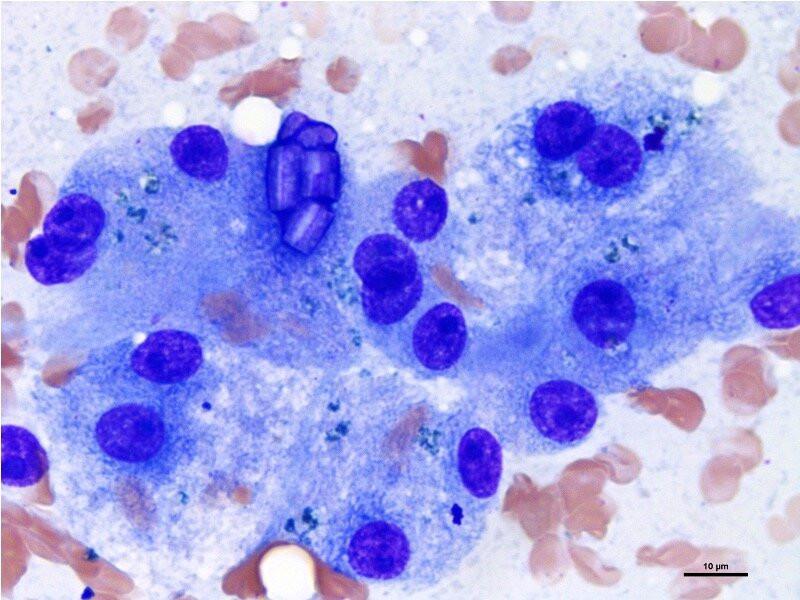
Un incremento en el número de nucleolos se ha visto asociado a colestasis. Con relativa frecuencia se observan cristales intranucleares rectangulares, de relevancia desconocida (Figura 4)2. En el núcleo se pueden ver invaginaciones citoplasmáticas, que contienen glucógeno y mitocondrias. Se trata de un hallazgo inespecífico que se ha descrito en casos de diabetes mellitus, en neoplasia hepatocelular o en enfermedad hepática crónica2,3. También se describen inclusiones nucleares víricas (por adenovirus canino tipo 1 o por herpesvirus) o tóxicas (por acúmulo de plomo)2.
Inflamación
La citología es un método poco fiable para la evaluación de cambios inflamatorios, aunque algunos estudios refieren una sensibilidad muy elevada de esta técnica4. Como se ha comentado previamente ofrece una imagen parcial, ya que no puede establecerse ni la localización ni la magnitud de la inflamación1,4,5. Algunos factores confusores que interfieren con esta son la presencia de una leucocitosis periférica o infiltrados neutrofílicos y linfocíticos asociados a hiperplasia nodular regenerativa en perros.
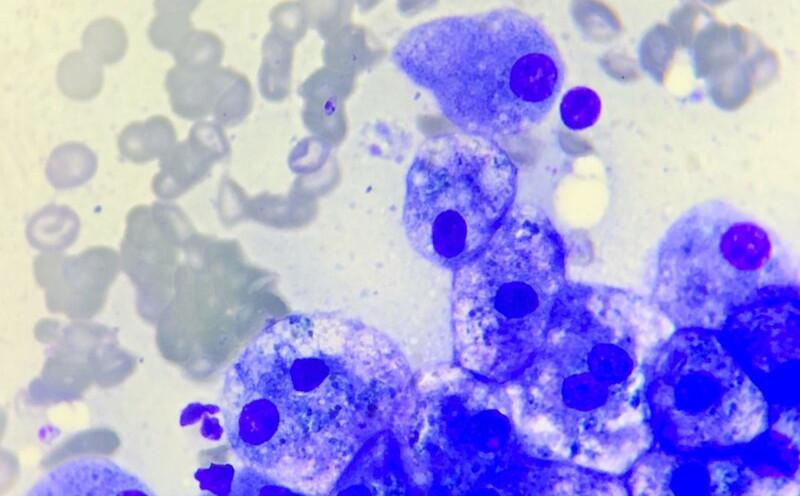
- Inflamación neutrofílica o supurativa: se identifica al observar un número elevado de neutrófilos que no sea atribuible al grado de hemodilución de la preparación. Además, los neutrófilos deben distribuirse asociados o dentro de los grupos de hepatocitos. La colangitis neutrofílica es el proceso inflamatorio más frecuente tanto en perros como en gatos1. Sin embargo, la citología no permite diferenciar entre un proceso inflamatorio del parénquima hepático (hepatitis), del tracto biliar (colangitis), o que afecte a ambos (colangiohepatitis). El patrón de elevación de las enzimas hepáticas puede dar una idea del tejido afectado, esperándose un aumento más marcado de ALP y GGT en casos de colangitis y de ALT y AST en casos de hepatitis. Con este tipo de inflamación debe prestarse especial atención a agentes infecciosos, especialmente si se encuentran neutrófilos degenerados, ya que es un hallazgo frecuente en hepatitis/colangiohepatitis bacterianas (Figura 5A). Las bacterias pueden llegar a hígado tanto por vía hematógena desde circulación portal como vía retrógrada a través de las vías biliares. Los géneros que se asocian a hepatitis con mayor frecuencia son Escherichia, Streptococcus, Staphylococcus, Enterococcus, Clostridium, Helicobacter y Leptospira. Otras causas de este tipo de inflamación incluyen inflación en órganos cercanos (p. ej., enteritis, pancreatitis aguda) o peritonitis infecciosa felina1,2.
- Inflamación histiocítica o macrofágica: en hígado los macrófagos provienen tanto de monocitos circulantes como de células Kupffer inactivas. El incremento de macrófagos se observa de manera aislada o asociado a incremento de otras líneas celulares, como neutrófilos, linfocitos y/o células plasmáticas. Este tipo de inflamación se asocia frecuentemente a agentes infecciosos como Mycobacterium, Leishmania (Figura 5B), Cytauxzoon (en gatos), hongos o virus (adenovirus canino tipo 1, causante de la hepatitis infecciosa canina; o el Coronavirus felino causante de la peritonitis infecciosa felina). Aunque la eritrofagocitosis es un proceso que ocurre de manera normal en el hígado, un incremento de este fenómeno puede deberse a hemorragia, congestión, o procesos inmunomediados1.
- Inflamación linfoplasmocitaria: la presencia de linfocitos pequeños junto con células plasmáticas con frecuencia se asocia a otros tipos de células inflamatorias, siendo un hallazgo poco específico en enfermedad hepática crónica (colangitis, colangiohepatitis o colangitis). En un alto número de casos se asocia con procesos extrahepáticos (p. ej., pancreatitis, enteritis, neoplasia), por lo que en primera instancia deben investigarse, y sólo en caso de no encontrar causas extrahepáticas puede atribuirse a un problema hepático primario. Otras causas de este tipo de inflamación incluyen estimulación antigénica del tejido (p. ej., infección por Leishmania, o inespecífica, sin una causa conocida). En gatos mayores, un predominio de linfocitos pequeños posiblemente indica colangitis (colangitis linfocítica felina crónica). En algunos casos no se puede diferenciar de forma certera entre una marcada inflamación linfocítica de un linfoma de células pequeñas o intermedias1,2.
- Inflamación mixta: en perros, la inflamación mixta con componente neutrofílico, linfocítico y macrofágico es un hallazgo común que puede reflejar patología hepática o extrahepática. En perros mayores de forma frecuente se asocia a hiperplasia nodular regenerativa. En gatos, un elevado número de neutrófilos junto con un componente linfoplasmocitario puede sugerir tanto una colangiohepatitis neutrofílica de curso crónico como una peritonitis infecciosa felina. Tanto en perros como en gatos, la inflamación mixta con neutrófilos, macrófagos, linfocitos y/o células plasmáticas pueden asociarse a una infección fúngica, por bacterias (p. ej., Mycobacterium) o protozoos (p. ej., Leishmania)1,2.
- Inflamación eosinofílica: aunque es un tipo de inflamación poco frecuente, al igual que en otras localizaciones puede indicar proceso alérgico o de hipersensibilidad, migración parasitaria a través del hígado (p. ej., trematodosis en zonas endémicas), enteritis eosinofílica, o en gatos reflejar un síndrome hipereosinofílico (Figura 5C). Los eosinófilos pueden verse tanto de forma aislada como junto con otras células inflamatorias. En algunos casos, la relevancia clínica de este tipo de inflamación es incierta2.
Hiperplasia nodular
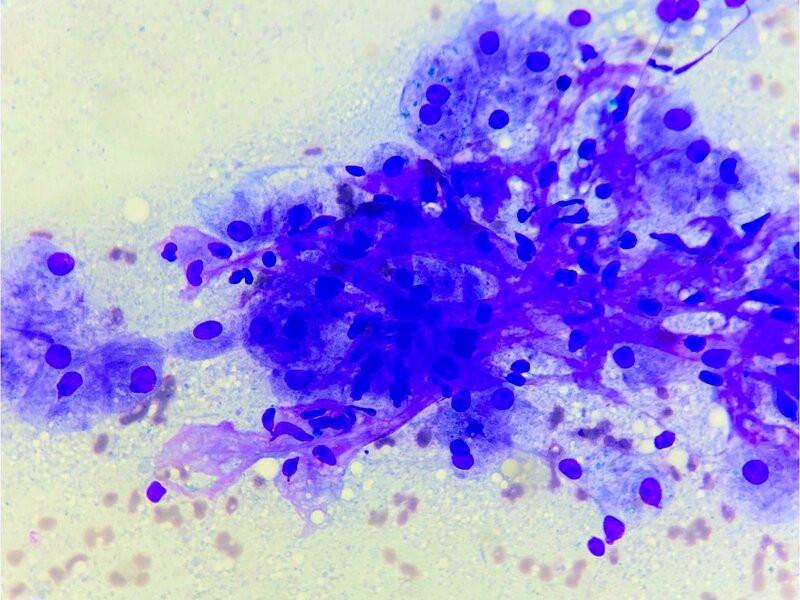
La hiperplasia nodular es un hallazgo frecuente en perros mayores, generalmente de más de 8 años. El número y el tamaño de los nódulos es muy variable, pueden ser únicos, múltiples, microscópicos o de gran tamaño. El principal hallazgo es la degeneración vacuolar no lipídica, y en menor grado, lipídica. Además, es frecuente encontrar células binucleadas, anisocitosis y anisocariosis leves, hematopoyesis extramedular y leve inflamación por aumento de macrófagos, neutrófilos y linfocitos1,3.
La hiperplasia nodular regenerativa también ocurre con mayor frecuencia en perros que en gatos, y a diferencia de la anterior no está relacionada con la edad. Se trata de una hiperplasia compensatoria secundaria a un daño hepatocelular. En estos caso la hematopoyesis extramedular no es una característica típica. Se recomienda un seguimiento de estas lesiones ya que, si las lesiones progresan o existe sospecha clínica de neoplasia, lo indicado es realizar biopsia de estas para diferenciar nódulos de hiperplasia de un adenoma hepatocelular o incluso de un carcinoma hepatocelular bien diferenciado1.
Fibrosis
La fibrosis se produce generalmente como respuesta a un daño hepatocelular sostenido en el tiempo y puede ir acompañada de inflamación o necrosis2. Los hallazgos citológicos más consistentes son la presencia de células mesenquimales con núcleo alargado que se dispone en finas bandas que conectan grupos de hepatocitos (Figura 6). Existe un incremento (tanto relativo como absoluto) de las células fusiformes y de los mastocitos. Como punto de corte se establece 10.7 células mesenquimales y 4 mastocitos por cada por cada 100 hepatocitos para realizar un diagnóstico presuntivo de fibrosis, aunque resulta poco práctico y los resultados de este estudio son controvertidos6. Sin embargo, las evidencias citológicas de fibrosis requieren de biopsia para establecer un diagnóstico definitivo, que no solo confirme su presencia, sino que además valore su extensión1.
Amiloidosis
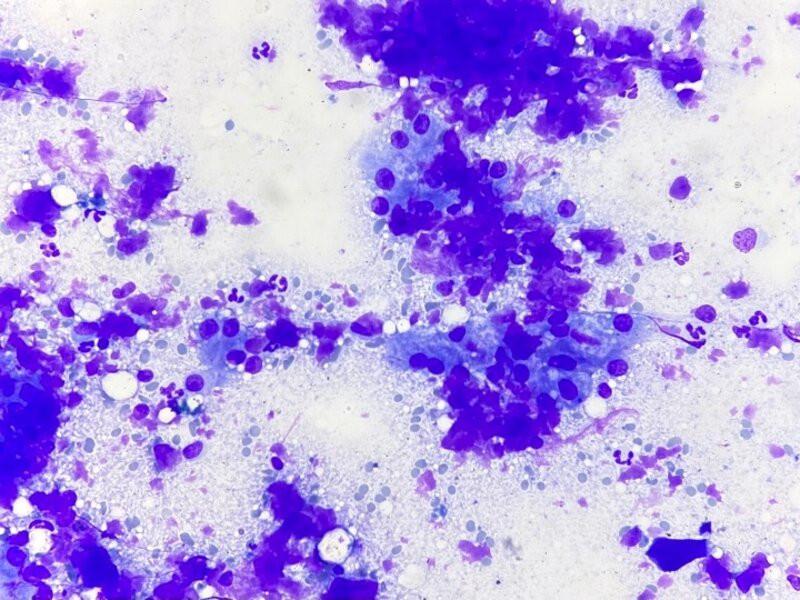
El amiloide A sérico es una proteína de fase aguda producida mayoritariamente en el hígado. Su producción es secundaria a inflamación crónica (sistémica o localizada), infección o destrucción tisular, aunque también se reconoce una predisposición familiar en gatos de raza abisinio y siamés, y en perros de raza Shar Pei. Puede formar precipitados en hígado (en el espacio de Disse) o en otros órganos, como riñón, páncreas o bazo. En la mayoría de los casos, la amiloidosis es un proceso reactivo (secundario), en respuesta a una inflamación hepática o extrahepática crónica (p. ej., osteomielitis)1–3.
Citológicamente el amiloide se identifica como un material extracelular, rosa, amorfo a fibrilar, que se distribuye generalmente cercano a los grupos de hepatocitos (Figura 7). A menudo, este material va acompañado de un grado variable de inflamación mixta. Para confirmar su presencia, la tinción rojo Congo lo tiñe de color rojo anaranjado y bajo luz polarizada muestra birrefringencia1–3.
Hematopoyesis extramedular
El hígado es un órgano hematopoyético durante la vida fetal2. En perros y gatos adultos, la hematopoyesis extramedular puede ocurrir en respuesta a un incremento de la demanda periférica de células sanguíneas, como una anemia marcada o en un estímulo inflamatorio grave. Generalmente, la línea celular que predomina es aquella con una mayor demanda en el organismo, si bien en todos los casos la maduración debe ser sincrónica, completa y ordenada1.
En el perro, en casos de hiperplasia nodular regenerativa puede observarse hematopoyesis extramedular, con un mayor componente granulocítico, mayoritariamente neutrófilos en banda y segmentados y en menor proporción otros precursores3. Sin embargo, en muchos de los casos este proceso es idiopático y carece de relevancia clínica.
Condiciones neoplásicas
En hígado, las neoplasias pueden ser primarias o secundarias, entre las que se incluyen metastáticas y multicéntricas. Los tumores primarios más frecuentes son los epiteliales (hepatocelulares o con origen en los hepatocitos y hepatobiliares con origen en el epitelio biliar). Menos frecuentes son las neoplasias mesenquimales primarias y, de forma anecdótica, se ha descrito la ocurrencia de hepatoblastoma tanto en perros como en gatos1. Los tumores que metastatizan a hígado generalmente llegan vía hematógena, linfática o por diseminación directa desde localizaciones cercanas7. Entre los tumores hemolinfáticos el más frecuente es el linfoma, que generalmente tiene una presentación multicéntrica1, aunque también pueden tratarse de linfomas hepáticos primarios7.
Neoplasia hepatocelular
El adenoma hepatocelular o hepatoma, es un tumor benigno con origen en los hepatocitos. Es menos frecuente que el carcinoma hepatocelular y existe un solapamiento morfológico significativo entre adenoma y carcinoma hepatocelular bien diferenciado o incluso con los nódulos de hiperplasia. Citológicamente los cambios del adenoma hepatocelular son sutiles, incluyendo leve anisocitosis, cambios degenerativos (degeneración vacuolar no lipídica) y aumento de la basofilia citoplasmática. Se requiere de examen histológico para realizar un diagnóstico definitivo1,7. No se ha demostrado que tengan una progresión hacia carcinoma hepatocelular3.
El carcinoma hepatocelular es la neoplasia primaria más frecuente en el perro, y la segunda más frecuente en el gato7. Citológicamente, los hepatocitos pueden mostrar un grado variable de diferenciación, desde bien diferenciados siendo difíciles de diferenciar de procesos benignos, hasta marcadamente pleomórficos (Figura 8A)1. Las características citológicas de los carcinomas hepatocelulares bien diferenciados son la disociación de hepatocitos con una disposición acinar o en empalizada, la presencia de abundantes núcleos desnudos, células rotas y capilares, anisocitosis y anisocariosis leves, células bi- y multinucleadas en número significativo y un incremento del ratio núcleo:citoplasma. Además, es más probable encontrar lipofuscina en un mayor porcentaje de hepatocitos en las lesiones no neoplásicas comparado con los carcinomas8.
Neoplasia hepatobiliar
Las neoplasias colangiocelulares se originan del epitelio de las vías biliares. Los adenomas colangiocelulares (adenoma biliar) son extremadamente raros, mientras que los carcinomas colangiocelulares (colangiocarcinoma) son la neoplasia más frecuente y la segunda más frecuente en gatos y perros respectivamente1,3,7.
En gatos se ha confundido con frecuencia la enfermedad poliquística congénita con los cistoadenomas biliares, que suelen ser masas sólidas, únicas y bien circunscritas con pequeños quistes1. En los cistoadenomas biliares, la punción suele dar como resultado un fluido acelular, mucinoso, hemorrágico o claro, en el que se encuentra un número variable de células inflamatorias, células de epitelio biliar o pequeños grupos de hepatocitos3,7.
Citológicamente, tanto adenomas como carcinomas colangiocelulares se caracterizan por la presencia de una población epitelial con morfología cuboidal, escasa cantidad de citoplasma claro y disposición en grupos celulares cohesivos y formaciones tubulares (Figura 8B). Las atipias celulares suelen ser leves a moderadas1,3 o marcadas7. Generalmente, el diagnóstico final requiere de examen histopatológico.
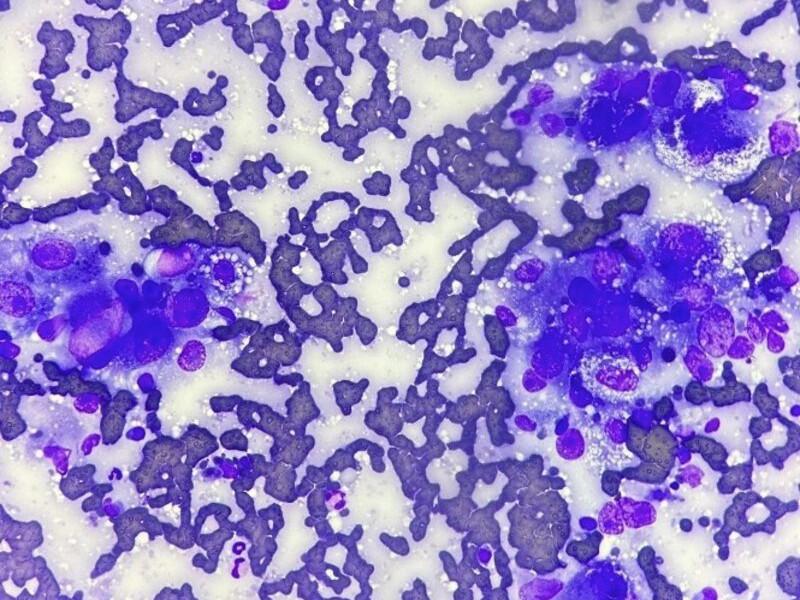
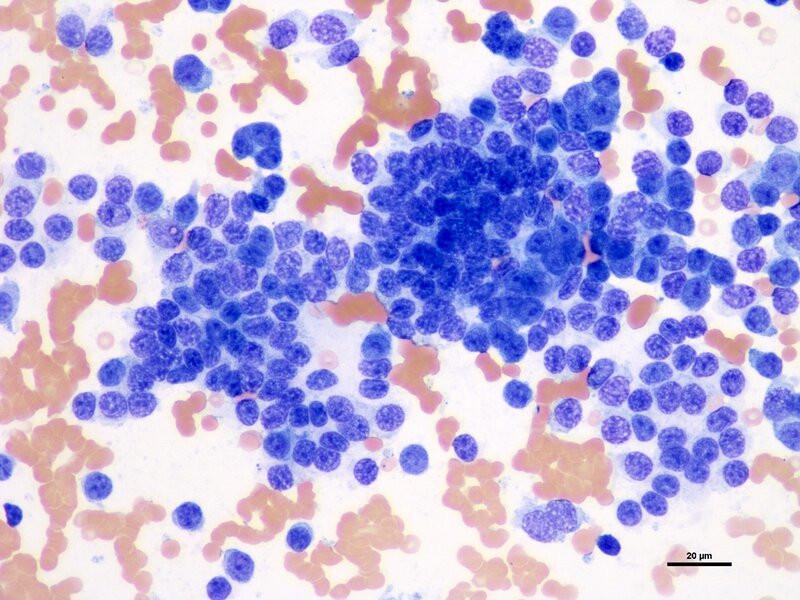
Carcinoide hepático
Es un tumor agresivo primario poco común en perros y gatos con origen en células neuroendocrinas localizadas en el epitelio biliar y posiblemente en el parénquima hepático. Citológicamente son similares a otras neoplasias de tipo neuroendocrino, son de elevada celularidad, con numerosas células rotas y núcleos desnudos, células distribuidas en pequeños grupos celulares, elevada relación núcleo:citoplasma y atipias celulares leves. No es posible diferenciarlos citológicamente de neoplasias neuroendocrinas metastáticas1,3,7. En algunos casos puede ser difícil diferenciarlo de otras neoplasias epiteliales metastáticas, para lo cual podrían utilizarse tinciones de plata (p. ej., Churukian-Schenk) demostrando gránulos finos neuroendocrinos3.
Neoplasias mesenquimales primarias
En esta categoría se encuentran los sarcomas y los mielolipomas. Estos últimos son una neoplasia hepática primaria benigna en gatos. Aunque en perros también puede ocurrir, se encuentran con mayor frecuencia en otras localizaciones como glándula adrenal o bazo. Citológicamente se observan precursores de varias líneas celulares (precursores eritroides, mieloides y megacariocitos), junto con adipocitos bien diferenciados1,3,7.
Los sarcomas hepáticos primarios son muy poco frecuentes en ambas especies. Entre ellos se describen fibrosarcoma, hemangiosarcoma, leiomiosarcoma, liposarcoma, rabdomiosarcoma, condrosarcoma y osteosarcoma. El leiomiosarcoma y el hemangiosarcoma son los más comunes en perros y gatos respectivamente7.
Carcinomas y sarcomas metásticos
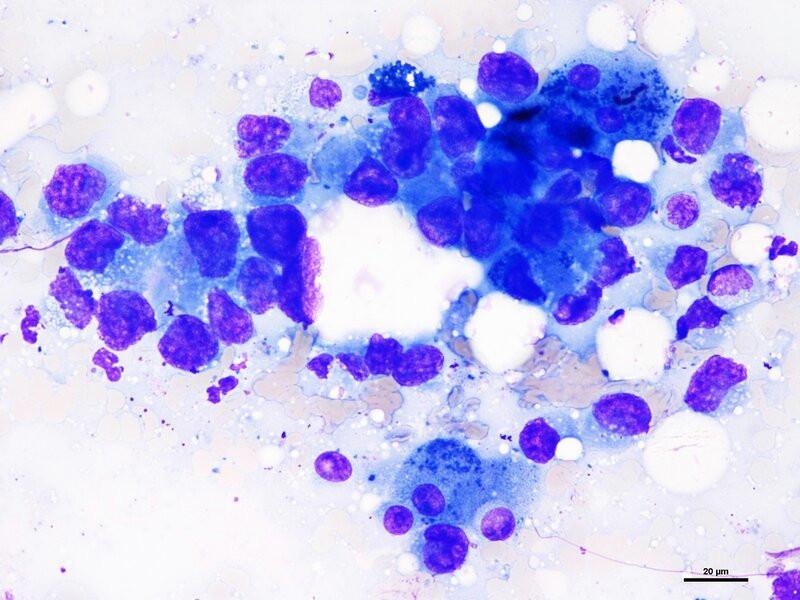
Las metástasis a hígado pueden llegar por vía hematógena, linfática o por diseminación directa desde localizaciones cercanas (páncreas o intestino). Hemangiosarcomas esplénicos y carcinomas pancreáticos y gastrointestinales son las lesiones metastáticas más frecuentes1,3,7.
Un número significativo de células epiteliales con origen no hepático es generalmente diagnóstico de carcinoma metastático (Figura 9), si bien el origen no puede establecerse mediante citología y se requerirá examen histológico1,3,7. El grado de atipia es variable y no tiene por qué ser la característica predominante de lesiones metastáticas, como ocurre en los tumores neuroendocrinos. La sensibilidad de detectar lesiones metastáticas es generalmente más baja que la especificidad o el valor predictivo positivo, especialmente para sarcomas7.
Neoplasias de células redondas
La mayoría de las neoplasias de células redondas que afectan a hígado forman parte de un proceso multiorgánico, aunque no puede excluirse por completo un origen hepático primario. Pueden encontrarse neoplasias de linfocitos, células plasmáticas, mastocitos o histiocitos entre otras7.
En los perros, los linfomas de células grandes que afectan a hígado generalmente se deben a un linfoma multicéntrico clásico, mientras que en los gatos suele tratarse de una afectación por un linfoma del tracto gastrointestinal. En algunas ocasiones, el linfoma encontrado en hígado también puede tener un origen hepático primario1,3,7.
Los linfomas de células grandes suelen exfoliar un número elevado de linfocitos de tamaño mayor a 2.5 veces el diámetro de un eritrocito y tienen una escasa cantidad de citoplasma azul (Figura 10A). También se encuentran linfomas de células grandes granulares, más frecuentes en gatos. Se caracterizan por la presencia de linfocitos de tamaño intermedio a grande, con característicos gránulos citoplasmáticos de color rosa o magenta que generalmente se agrupan en una zona cercana al núcleo.1
Se han identificado dos subtipos de linfoma que afectan a hígado, el linfoma hepatoesplénico y el hepatocitotrópico1,3,7,9. Son dos subtipos de linfomas de células T que cursan sin linfadenopatía periférica e infiltran los sinusoides hepáticos (y el hepatocitotrópico además infiltra los cordones hepáticos). El linfoma hepatoesplénico es agresivo en perros, se cree que tiene origen en bazo.
Citológicamente se observan linfocitos de tamaño intermedio a grande, con citoplasma azul medio y un número variable de gránulos citoplasmáticos magenta, en ocasiones localizados próximos al núcleo, que tiene un nucleolo prominente. Se caracteriza por una actividad eritrofagocítica de los linfocitos, junto con un número variable de macrófagos que también tienen actividad hemofagocítica9. El linfoma hepatocitotrópico en ambas especies tiene probablemente origen en hígado. Los linfocitos neoplásicos causan una invaginación en los hepatocitos, fenómeno de emperipolesis, que en citología puede dar la impresión de que los linfocitos se encuentran en el interior de los hepatocitos. Ambos subtipos, aunque tienen características citológicas singulares, requieren de confirmación histológica e inmunofenotipado para su confirmación diagnóstica1.
Las leucemias (linfoide o mieloide) agudas también puede involucrar al hígado, causando hepatomegalia3. Por el contrario, si se encuentra un número muy elevado de linfocitos pequeños o intermedios es complicado establecer la causa, y los diagnósticos diferenciales deben incluir un linfoma de células pequeñas o intermedias, leucemia linfocítica crónica (en caso de haber linfocitosis concurrente) e inflamación linfocítica grave1.
Para un diagnóstico final en estos procesos, es necesario realizar pruebas complementarias, incluyendo biopsia con inmunohistoquímica, citometría de flujo o un test de clonalidad, e idealmente una combinación de varias de ellas. En gatos, los mastocitomas afectando a hígado generalmente representan un mastocitoma visceral (esplénico), mientras que en los perros lo más frecuente es que se trate de una metástasis de mastocitoma cutáneo1. En hígado, las metástasis de mastocitoma representan un reto diagnóstico, ya que los mastocitos se encuentran de forma normal en este órgano. Para llegar a un diagnóstico de metástasis, es necesario encontrar un número moderado o elevado de mastocitos, que se distribuyen ocasionalmente en grupos celulares no cohesivos, con un variable grado de granulación y en ocasiones morfología alterada7.
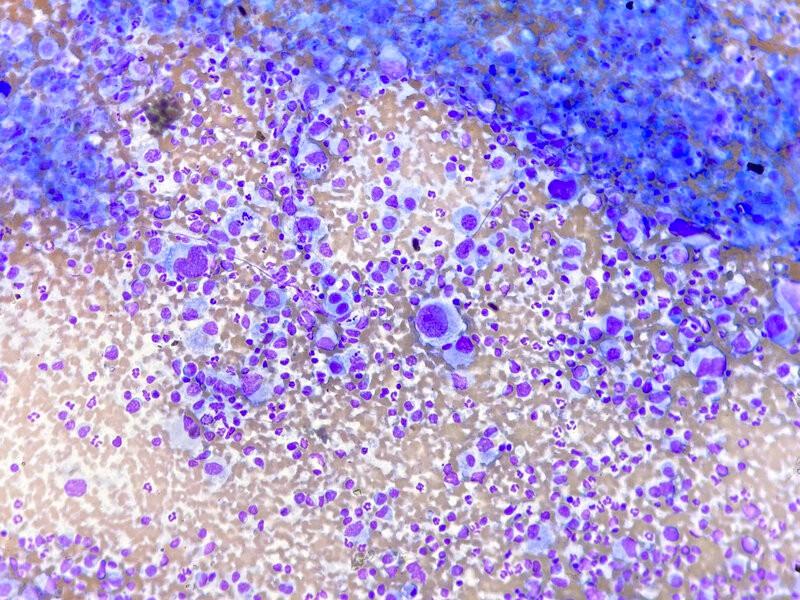
El sarcoma histiocítico es una neoplasia maligna con origen en célula dendríticas, que se disemina de forma rápida a múltiples órganos, incluyendo bazo, hígado, pulmones o linfonodos entre otros1,7. El sarcoma histiocítico con diseminación a hígado se encuentra de forma más frecuente en perros que en gatos. Las preparaciones suelen ser de elevada celularidad. Las células son de gran tamaño, con morfología redondeada, ovalada o irregular, citoplasma azul claro y de forma frecuente con vacuolas claras ocasionales. Los núcleos son de gran tamaño, redondos o irregulares, con cromatina finamente punteada y uno o varios nucleolos prominentes (Figura 10B)1.
Otra neoplasia histiocítica es el sarcoma histiocítico hemofagocítico, que tiene origen en macrófagos esplénicos de la pulpa roja o de médula ósea. Las células neoplásicas muestran eritrofagia marcada y pueden variar desde formas bien diferenciadas hasta un pleomorfismo celular moderado, generalmente menor al observado en el sarcoma histiocítico clásico1.
De entre las neoplasias de células redondas, las de células plasmáticas son las que se encuentran con menor frecuencia afectando a hígado, y se agrupan bajo el término “desorden/alteración relacionada con mieloma”.
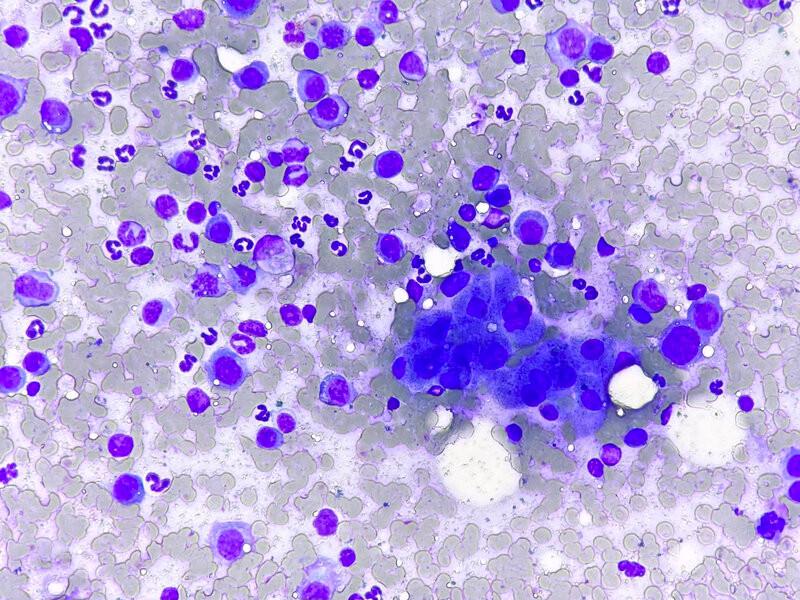
En perros es más frecuente encontrar un mieloma múltiple con afectación hepática, así como otras localizaciones extramedulares; mientras que en gato se observan con mayor frecuencia neoplasias de células plasmáticas con origen en hígado o bazo (forma extramedular primaria). La gammapatía monoclonal es una característica compartida por ambas especies. Citológicamente, las células plasmáticas suelen estar bien diferenciadas, aunque en ocasiones pueden llegar a mostrar atipias moderadas a marcadas. Se caracterizan por tener una morfología redonda a ovoide, el núcleo se encuentra en posición excéntrica con cromatina agregada a granular y el citoplasma es azul oscuro, con una zona perinuclear clara compatible con el aparato de Golgi (Figura 10C)1.
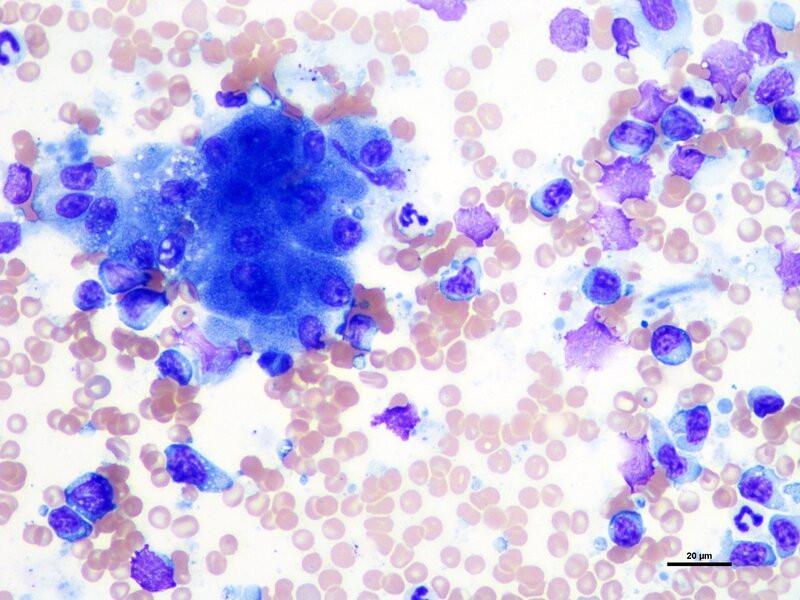
Estudio de la bilis
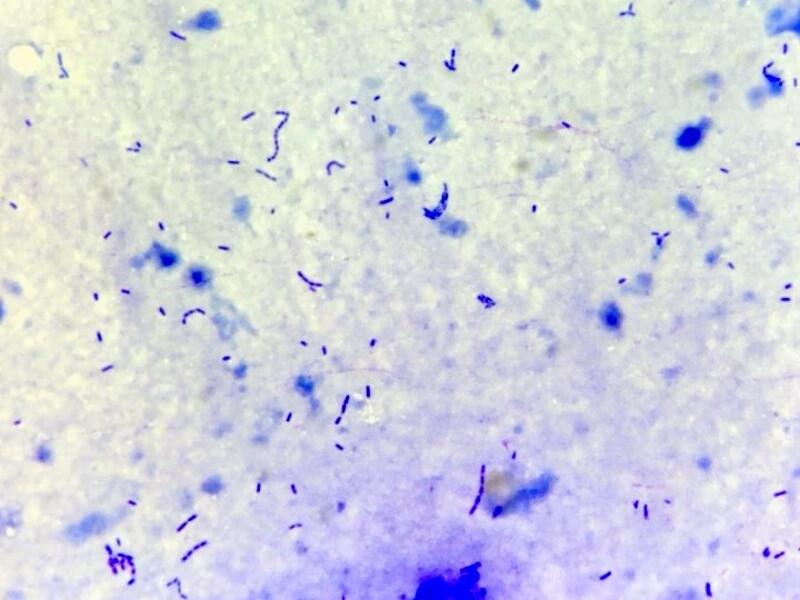
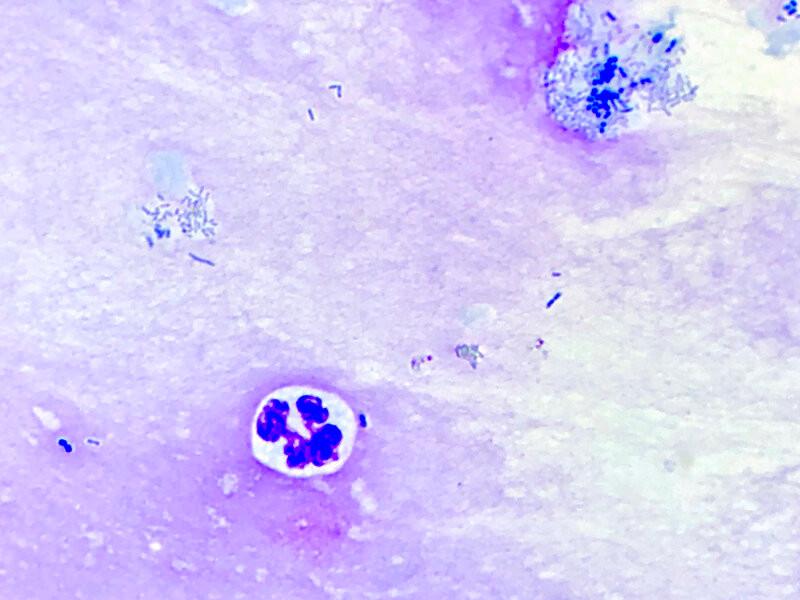
El muestreo de bilis generalmente se realiza tras observar alteraciones ecográficas. Tiene como objetivos principales determinar la presencia o ausencia de bacterias (bactibilia) (Figura 11A), cristales, pigmentos y células inflamatorias (Figura 11B). De forma normal las pérdidas de bilis hacia cavidad abdominal son raras tras la punción y vaciado de la vesícula biliar. Algunas condiciones como la colelitiasis o el mucocele pueden predisponer a una posible rotura iatrogénica de la pared de la vesícula biliar7. La colecistitis puede observarse en colangitis bacteriana o estéril, obstrucción del tracto biliar (por colelitiasis u otras causas), mucocele o por una combinación de los anteriores1. Aunque generalmente la bilis es estéril, de forma ocasional algunos perros clínicamente sanos pueden presentar cultivos de bilis positivos10.
Macroscópicamente, la bilis es verde oscura. En citología se observa un material amorfo a granular, generalmente azulado, con detritus celular agregado en cantidad variable. En ocasiones se encuentran cristales de bilirrubina, con morfología en aguja, de color amarillo a marrón o rojizo1,7. Como parte del estudio de bilis, siempre que sea posible debe recomendarse realizar cultivo y antibiograma, ya que si se han observado bacterias estas pruebas caracterizarán mejor el proceso, y en caso de no haberlas encontrado no puede descartarse con certeza la presencia de estas.
Curiosamente, en un estudio retrospectivo con 140 muestras de bilis, se encontraron agentes infecciosos en el 30 % y el 19 % de los casos caninos y felinos respectivamente, e inflamación en un 5 % de los casos de perros y un 19 % de los de gatos. Mediante citología se detectaron más casos con presencia de agentes infecciosos (24 %) que mediante cultivo (21 %)11. Teniendo en cuenta únicamente perros sanos, la prevalencia de bactibilia fue del 10,8 %. De nuevo, no siempre un cultivo positivo se asoció a diagnóstico citológico de bactibilia y viceversa, un 9,2 % de los casos se diagnosticó mediante citología y un 4,6 % mediante cultivo12.
Conclusión
Aunque las limitaciones de la citología en el examen hepático son evidentes, esta técnica ofrece en muchos casos un valioso abordaje al diagnóstico si dichas limitaciones son tenidas en cuenta. El abordaje citológico es de especial interés en procesos infecciosos, en aquellos en los que se produce acúmulo de pigmentos o en procesos neoplásicos.
Bibliografía
- Siegel A, Wiseman MD. 20 The Liver. In: Valenciano AC, Cowell RL, eds. Cowell and Tyler’s Diagnostic Cytology and Hematology of. the Dog and Cat. 5th ed. Elsevier; 2019:329-345.
- Masserdotti C. 34 Nonneoplastic Disorders of the Liver. In: Sharkey LC, Radin MJ, Seelig D, eds. Veterinary Cytology. 1st ed. Wiley-Blackwell; 2020:413-431.
- Meyer DJ. 9 The Liver. In: Raskin RE, Meyer DJ, eds. Canine and Feline Cytology: A Color Atlas and Interpretation Guide. 3rd ed. Elsevier; 2015:259-283.
- Weiss DJ, Blauvelt M, Aird B. Cytologic Evaluation of Inflammation in Canine Liver Aspirates. Veterinary Clinical Pathology. 2001;30(4):193-196.
- Bahr KL, Sharkey LC, Murakami T, Feeney DA. Accuracy of US-guided FNA of focal liver lesions in dogs: 140 cases (2005-2008). Journal of the American Animal Hospital Association. 2013;49(3):190-196.
- Masserdotti C, Bertazzolo W. Cytologic features of hepatic fibrosis in dogs: a retrospective study on 22 cases. Veterinary Clinical Pathology. 2016;45(2):361-367.
- Wiedmeyer CE, Bryan J. 35 Hepatobiliary Neoplasia and Cancer Staging. In: Sharkey LC, Radin MJ, Seelig D, eds. Veterinary Cytology. 1st ed. Wiley-Blackwell; 2020:432-444.
- Masserdotti C, Drigo M. Retrospective study of cytologic features of well-differentiated hepatocellular carcinoma in dogs. Veterinary Clinical Pathology. 2012;41(3):1-9.
- Keller SM, Vernau W, Hodges J, et al. Hepatosplenic and Hepatocytotropic T-Cell Lymphoma: Two Distinct Types of T-Cell Lymphoma in Dogs. Veterinary Pathology. 2012;50(2):281-290.
- Kook PH, Schellenberg S, Grest P, Reusch CE, Corboz L, Glaus TM. Microbiologic evaluation of gallbladder bile of healthy dogs and dogs with iatrogenic hypercortisolism: A pilot study. Journal of Veterinary Internal Medicine. 2010;24:224-228.
- Peters LM, Glanemann B, Garden OA, Szladovits B. Cytological Findings of 140 Bile Samples from Dogs and Cats and Associated Clinical Pathological Data. Journal of Veterinary Internal Medicine. 2016;30(1):123-131.
- Verwey E, Gal A, Kettner F, Botha WJ, Pazzi P. Prevalence of subclinical bactibilia in apparently healthy shelter dogs. Journal of Small Animal Practice. Published online 2021:1-11.
 by Multimédica
by Multimédica